US Pharm. 2009;34(11):26-39.
Jistota při výběru vhodného antidepresiva pro pacienty s diagnózou velké depresivní poruchy (MDD) je vysoká, a to nejen proto, že studie nezaznamenaly žádné rozdíly v účinnosti jednotlivých látek, ale také proto, že pouze 11-30 % pacientů dosáhne při počáteční léčbě remise, a to i po roce.1,2 To následně vedlo lékaře k tomu, že při léčbě deprese postupují metodou pokus-omyl.3 Poslední velká revize Diagnostického a statistického manuálu duševních poruch (DSM-IV-TR) byla navíc vypracována v roce 2000.4 V roce 2005 byly publikovány pokyny pro sledování, které přezkoumaly důležité obavy o bezpečnost, jež se objevily u některých látek, jako je nefazodon, a také přezkoumaly dvě nová antidepresiva schválená v tomto roce, escitalopram a duloxetin.5 Revize a aktualizace DSM-IV-TR (rukopis DSM-V) má být provedena až v květnu 2012. Proto je zapotřebí aktuální přehled, který by klinickým lékařům pomohl při rozhodování o vhodných látkách pro léčbu jednotlivých pacientů.
Studie Sequenced Treatment Alternatives to Relieve Depression (STAR*D) z roku 2007 se pokusila vyvinout a vyhodnotit proveditelné léčebné strategie ke zlepšení klinických výsledků u pacientů s depresí rezistentní na léčbu, u nichž byla zjištěna aktuální epizoda velké deprese.6 Cílem studie STAR*D bylo konkrétně určit, který z několika způsobů léčby je nejúčinnějším „dalším krokem“ pro pacienty, kteří nedosáhnou remise při počáteční nebo následné léčbě nebo kteří léčbu netolerují. Celkové výsledky této studie ukázaly, že farmakologické rozdíly mezi psychotropními léky se nepromítly do podstatných klinických rozdílů, ačkoli snášenlivost se lišila.6
Účelem tohoto článku je podat přehled důkazů o léčbě dostupných v literatuře s cílem poskytnout rychlý odkaz, který pomůže klinickým lékařům rozhodnout se pro vhodný přípravek s ohledem na nežádoucí účinky, lékové interakce a bezpečnost léků, jakož i na charakteristiky pacienta.
Co je to deprese?“
Deprese může být chronická nebo opakující se duševní porucha, která se projevuje několika příznaky, jako je depresivní nálada, ztráta zájmu nebo potěšení, pocity viny, poruchy spánku nebo chuti k jídlu, nízká energie a potíže s myšlením.7 Deprese může vést k podstatnému zhoršení schopnosti jedince zvládat každodenní povinnosti. Deprese může také vést k sebevraždě, což je tragédie, která má každoročně na svědomí přibližně 850 000 životů na celém světě.7
Prevalence a rizikové skupiny obyvatel
Podle odhadů je na celém světě postiženo depresí 121 milionů lidí.7 V roce 2000 byla deprese čtvrtým nejvýznamnějším přispěvatelem k celosvětovému zatížení nemocemi mezi všemi nemocemi a předpokládá se, že do roku 2020 vzroste na druhé místo mezi nejvýznamnějšími přispěvateli k celosvětovému zatížení nemocemi, hned po srdečních onemocněních.7
Populace s vyšším rizikem vzniku deprese zahrnují ženy, osoby ve věku 24 až 45 let a osoby s příbuznými prvního stupně s depresí. Ženy jsou vystaveny zvýšenému riziku deprese až do svých 50 let a jejich celoživotní riziko je dvakrát vyšší než u mužů. Nejčastěji se s depresí setkávají lidé ve věku 24 až 45 let. A konečně, příbuzní prvního stupně pacientů s depresí mají 1,5 až 3krát vyšší pravděpodobnost výskytu deprese než ostatní.4,8
Patofyziologie a farmakoterapeutické zdůvodnění
Ve snaze popsat patofyziologii deprese byly vysloveny hypotézy o biologických a psychosociálních příčinách. Farmakologické přípravky se zaměří na biologické příčiny spojené s dysregulací neurotransmiterů. Tato dysregulace je často popisována jako nedostatek hladin mozkových neurotransmiterů. Hladiny noradrenalinu, serotoninu a dopaminu mohou být u pacientů s depresí snížené, a tak se snížené množství neurotransmiterů spojuje s touto poruchou.8 Smyslem farmakoterapie bylo posílit tyto nedostatky blokováním zpětného vychytávání nebo zabráněním enzymatickému metabolismu neurotransmiterů prostřednictvím antidepresiv. Celkově se tyto mechanismy zaměřují na zvýšení hladiny neurotransmiterů buď tím, že nutí neuron častěji střílet a produkovat více neurotransmiterů, nebo tím, že zabraňují degradaci samotného neurotransmiteru.
Farmakologické látky
V současné době je k dispozici několik tříd látek pro léčbu deprese. Patří mezi ně mimo jiné selektivní inhibitory zpětného vychytávání serotoninu (SSRI), tricyklická antidepresiva (TCA), inhibitory monoaminooxidázy (MAOI) a inhibitory zpětného vychytávání serotoninu a noradrenalinu (SNRI).
Antidepresiva byla v krátkodobých placebem kontrolovaných studiích MDD spojena se zvýšeným rizikem sebevražedného myšlení a sebevražednosti u dětí, dospívajících a mladých dospělých. Každý, kdo zvažuje použití jakéhokoli antidepresiva u dítěte, dospívajícího nebo mladého dospělého, musí zvážit toto riziko s klinickou potřebou. Krátkodobé studie neprokázaly zvýšení rizika sebevražednosti u antidepresiv ve srovnání s placebem u dospělých ve věku nad 24 let a u dospělých ve věku 65 let a starších došlo ke snížení rizika u antidepresiv ve srovnání s placebem. Deprese a další psychiatrické poruchy jsou samy o sobě spojeny se zvýšeným rizikem sebevraždy. Pacienti všech věkových kategorií, kteří zahájili léčbu antidepresivy, by měli být náležitě monitorováni a pečlivě sledováni, zda nedochází ke klinickému zhoršení, sebevražednosti nebo neobvyklým změnám chování.9
Selektivní inhibitory zpětného vychytávání serotoninu4,10: SSRI jsou považovány za látky první volby, pokud jde o léčbu pacientů s depresí. Mezi tyto léky patří citalopram, escitalopram, fluoxetin, fluvoxamin, paroxetin a sertralin (TABULKA 1). Mezi hlavní nežádoucí účinky této skupiny patří nevolnost, zvracení a průjem, které jsou závislé na dávce a mají tendenci odeznít po prvních týdnech léčby. U některých pacientů mohou SSRI způsobovat agitovanost a poruchy spánku, které časem rovněž odezní. Sexuální dysfunkce je nežádoucí účinek přítomný u všech antidepresiv, ale zdá se, že nejčastější je u SSRI.
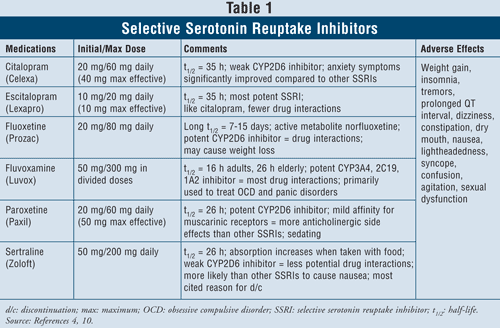
Serotoninový syndrom (tj. bolesti břicha, průjem, pocení, změna duševního stavu, selhání ledvin, kardiovaskulární šok a případně smrt) je vzácným nežádoucím účinkem SSRI. Serotoninový syndrom se může objevit při zvýšení dávky SSRI nebo při užívání SSRI s bylinami, jako je třezalka tečkovaná, nebo s nelegálními drogami. Konečně kombinace SSRI s MAOI může také vést ke smrtelným lékovým interakcím s rozvojem serotoninového syndromu. Pokud lékaři cítí potřebu přejít z jedné třídy látek na druhou, doporučuje se, aby mezi vysazením SSRI a nasazením MAOI uplynulo alespoň pět poločasů.4 Ze všech látek této třídy má fluvoxová mina nejvyšší míru lékových interakcí, protože inhibuje několik jaterních enzymů, jako jsou CYP450 1A2, 2C19, 2C9, 2D6 a 3A4. Fluoxetin těsně následuje míru lékových interakcí fluvoxaminu s inhibicí CYP 2C9, 2D6 a 3A4. Konečně nejméně lékových interakcí mají citalopram a escitalopram, protože v menší míře inhibují enzymy 2D6.
Při zvážení charakteristik a bezpečnosti pacientů je použití SSRI bezpečné u většiny skupin pacientů, včetně pacientů s již existujícím srdečním onemocněním, astmatem, demencí a hypertenzí. Starší lidé, kteří jsou obzvláště náchylní k ortostatické hypotenzi a také ke ztrátě hmotnosti, mohou mít z užívání SSRI největší prospěch, protože tyto látky způsobují nárůst hmotnosti a postrádají anticholinergní aktivitu.
Tricyklická antidepresiva4,10: TCA blokují zpětné vychytávání noradrenalinu a serotoninu, ale mají také afinitu k alfa1, H1 a muskarinovým receptorům, čímž způsobují anticholinergní nežádoucí účinky. V rámci této třídy jsou k dispozici dvě podtřídy látek, terciární a sekundární aminové TCA (TABULKA 2). Sekundární aminové TCA (desipramin, maprotilin, nortriptylin) mají menší afinitu k alfa1, H1 a muskarinovým receptorům, a proto způsobují méně anticholinergních nežádoucích účinků než terciární aminové TCA (např. amitriptylin, amoxapin, klomipramin, doxepin, imipramin).
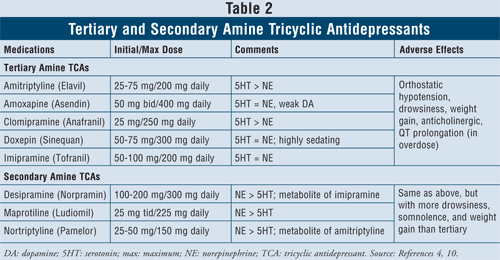
Hlavními nežádoucími účinky této skupiny látek jsou ortostatická hypotenze, prodloužení QT intervalu, ospalost, sucho v ústech, rozmazané vidění, zácpa a přírůstek hmotnosti. Obecně platí, že terciární aminové TCA mají větší serotoninovou aktivitu oproti sekundárním aminovým TCA, které mají větší norepinefrinovou aktivitu, a způsobují tak menší ospalost, somnolenci a přírůstek hmotnosti.
Je známo, že TCA inhibují enzymy CYP 2C19 i 2D6.11 V menší míře jsou také metabolizovány enzymy CYP 1A2 a 3A4.12 Z tohoto důvodu, i když lékové interakce u těchto látek nemusí být primárním problémem, se doporučuje opatrnost při kombinaci TCA se SSRI, protože plazmatická hladina léku TCA má potenciál se zvýšit až čtyřnásobně, což může vést k toxickým účinkům.13,14
Při zvažování charakteristik a bezpečnosti pacientů jsou TCA kontraindikovány u některých specifických kardiálních stavů, jako jsou pacienti s anamnézou arytmií, dysfunkcí sinusového uzlu nebo poruchami vedení. Opatrnost se doporučuje u starších osob, protože jsou citlivější na cholinergní blokádu i ortostatickou hypotenzi. Navíc jedinci trpící také demencí budou obzvláště citliví na toxické účinky muskarinové blokády na paměť a pozornost a obecně by pro ně bylo nejlepší, kdyby dostávali antidepresiva s co nejnižším stupněm anticholinergních účinků. A konečně, při zvažování nasazení TCA u pacientů se sebevražednými myšlenkami je třeba dbát opatrnosti vzhledem k vysokému riziku letality při předávkování. Smrtelná dávka je pouze osminásobkem terapeutické dávky, takže při předávkování mohou TCA zablokovat sinoatriální uzel v srdci.
Inhibitory monoaminooxidázy4,10: Mezi dostupné inhibitory MAOI patří isokarboxazid, fenelzin, selegilin a tranylcypromin (TABULKA 3). Kromě selegilinu, který je selektivním inhibitorem MAO B, všechny ostatní látky inhibují enzymy MAO A i B zodpovědné za metabolismus serotoninu, noradrenalinu a dopaminu v mozku. Vzhledem k závažným nežádoucím účinkům a nutným dietním omezením jsou MAOI obecně vyhrazeny pro pacienty, u kterých selhala jiná antidepresiva.
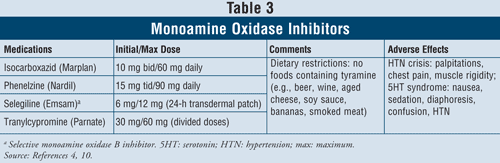
Hypertenzní krize může nastat, pokud pacienti užívající MAOI požijí potraviny obsahující tyramin, jako je pivo, víno, stařené sýry a uzené maso. Tato reakce se projevuje akutním nástupem silné bolesti hlavy, nevolnosti, ztuhlosti šíje, bušení srdce, bolesti na hrudi a zmatenosti. MAOI mohou také způsobit serotoninový syndrom. Jak již bylo zmíněno, tento syndrom se nejčastěji vyskytuje, pokud jsou MAOI užívány současně s jinými serotoninergními látkami, jako jsou SSRI, nebo pokud je brzy po MAOI podán venlafaxin, SNRI. Při přechodu pacientů ze SSRI s krátkým poločasem na MAOI je důležité, aby mezi ukončením podávání SSRI a zahájením podávání MAOI bylo dodrženo dvoutýdenní vymývací období. Pokud je SSRI fluoxetin, který má dlouhý poločas, mělo by být vymývací období 5 týdnů.4 U MAOI se mohou objevit další nežádoucí účinky, jako je ortostatická hypotenze, přibývání na váze, sexuální dysfunkce a nespavost.
Vzhledem k vysoké míře lékových interakcí s těmito látkami je třeba dbát opatrnosti při jejich předepisování pacientům s astmatem užívajícím sympatomimetické bronchodilatancia. U pacientů s hypertenzí mohou MAOI vyvolat ortostatickou hypotenzi, zejména při současné léčbě diuretiky.
Inhibitory zpětného vychytávání serotoninu a noradrenalinu4,10: SNRI, jako jsou desvenlafaxin, duloxetin a venlafaxin, lze rovněž použít jako léky první volby (TABULKA 4). Tyto léky jsou bezpečnější než TCA a jejich nežádoucí účinky jsou podobné jako u SSRI, včetně nevolnosti, zvracení a sexuální dysfunkce, stejně jako zvýšeného krevního tlaku.
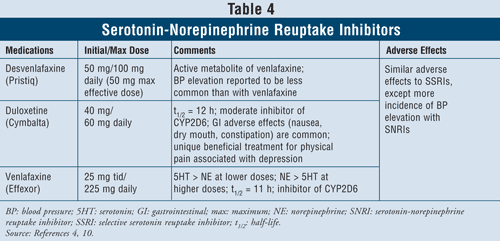
Bylo prokázáno, že venlafaxin způsobuje zvýšení krevního tlaku ve 3 až 13 % případů, zatímco u desvenlafaxinu bylo hlášeno zvýšení krevního tlaku pouze v 1 až 2 % případů.10 Proto se doporučuje vyhnout se užívání venlafaxinu u pacientů s nekontrolovanou hypertenzí, protože přípravek může tento stav zhoršit. Duloxetin má větší noradrenalinovou aktivitu než obě výše uvedené látky, a je tak užitečný při tělesných příznacích, jako jsou bolesti svalů, hlavy, žaludeční problémy a generalizovaná bolest, které se často vyskytují u pacientů s těžkou depresí. Díky své účinnosti u symptomů bolesti byl duloxetin schválen i pro další indikace, jako je fibromyalgie a diabetická periferní neuropatická bolest.15 A konečně, všechny tři látky mají při nižších dávkách větší aktivitu serotoninu než noradrenalinu a při vyšších dávkách větší aktivitu noradrenalinu než serotoninu, a mají tedy nežádoucí účinky závislé na dávce.
Jiná antidepresiva4,10: K dispozici je několik dalších antidepresiv, která se svým mechanismem účinku liší od dříve popsaných tříd léků.
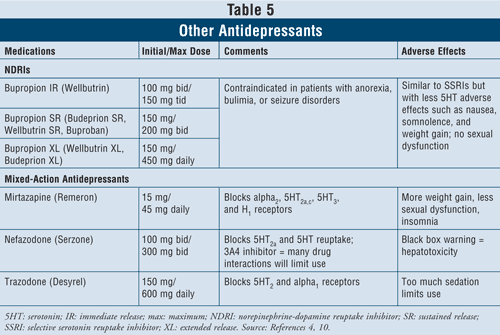
Inhibitory zpětného vychytávání noradrenalinu a dopaminu (NDRI), jako je bupropion s okamžitým uvolňováním (IR) značky Wellbutrin (dostupný také v dlouhodobě působících lékových formách jako Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL a Buproban), lze použít jako léky první volby k léčbě deprese (TABULKA 5). Jejich nežádoucí účinky jsou podobné jako u SSRI, s minimálními serotoninovými účinky, jako je nevolnost a přibývání na váze, a s malou nebo žádnou sexuální dysfunkcí. Ukázalo se, že bupropion má u některých pacientů příznivé účinky na příznaky Parkinsonovy choroby, ale může také vyvolávat některé psychotické příznaky, možná kvůli svému agonistickému působení na dopaminergní systém.16
Nakonec jsou k dispozici ještě tři antidepresiva se smíšeným účinkem: mirtazapin, nefazodon a trazodon (TABULKA 5). Všechny tři látky blokují různé serotoninové receptory, a mají tak odlišné účinky. Mirtazapin způsobuje větší přírůstek hmotnosti tím, že zvyšuje chuť k jídlu. Nefazodon má omezené použití kvůli hepatotoxicitě a inhibici enzymu CYP3A4, což vede k lékovým interakcím. Trazodon ve velké míře blokuje serotoninové receptory, se slabou vazbou na muskarinové receptory. Mohou se objevit nežádoucí účinky, jako je sedace, bolest hlavy, poruchy paměti, sucho v ústech a zácpa. Opatrnost se doporučuje také při užívání trazodonu u mužů kvůli riziku priapismu.
Závěr
Všeobecně se ukázalo, že antidepresiva jsou stejně účinná; proto by měl být výběr léků založen na nežádoucích účincích, lékových interakcích, bezpečnosti a preferencích pacienta. K dispozici je několik algoritmů, kterými se může lékař při léčbě pacienta řídit, zejména nedávno aktualizovaný algoritmus texaského ministerstva zdravotnictví pro léčbu MDD (aktualizovaný v červenci 2008).17 Pokud pacienti vykazují částečnou odpověď, mohou se lékaři rozhodnout zvýšit dávku, přejít na alternativní lék nebo podat kombinaci antidepresiv. Naopak pokud pacienti neodpovídají nebo lék netolerují, je také vhodné přejít na alternativní látku, přičemž je třeba vzít v úvahu, že terapeutický účinek se obvykle dostaví mezi 4. až 6. týdnem, i když nežádoucí účinky se mohou objevit již po 1. týdnu léčby.4,17 Kromě toho, i když se nežádoucí účinky objeví na počátku léčby, zpravidla po 2 až 3 týdnech odezní.4,17 Nicméně antidepresivum, které s největší pravděpodobností zajistí pacientovi zlepšení a bezpečnost, lze alespoň částečně určit metodou pokusu a omylu. Vzhledem k tomu, že je obtížné předpovědět, jaký lék bude pro konkrétního pacienta účinný a zároveň ho bude tolerovat, je obeznámenost se širokým spektrem antidepresiv rozumná a užitečná.
1. Song F, Freemantle N, Sheldon TA a kol. Selektivní inhibitory zpětného vychytávání serotoninu: metaanalýza účinnosti a přijatelnosti. BMJ. 1993;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRI versus ostatní antidepresiva u depresivní poruchy. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selecting among second-step antidepressant medication monotherapies: predictive value of clinical, demographic, or first-step treatment features. Arch Gen Psychiatry. 2008;65:870-881.
4. American Psychiatric Association. Diagnostický a statistický manuál duševních poruch, čtvrté vydání, revize textu (DSM-IV-TR). Washington, DC: American Psychiatric Association; 2000.
5. Pracovní skupina pro velkou depresivní poruchu. Guideline Watch (Sledování pokynů): Practice Guidelines for the Treatment of Patients with Major Depressive Disorder (Praktické pokyny pro léčbu pacientů s velkou depresivní poruchou). 2nd ed. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigace ve studii Sequenced Treatment Alternatives to Relieve Depression (STAR*D): praktické výsledky a důsledky pro léčbu deprese v primární péči. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Světová zdravotnická organizace. www.who.int/mental_health/management/depression/definition/en. Přístup 5. října 2009.
8. Dipiro JT, Talbert RL, Yee GC, et al. Pharmacotherapy: Patofyziologický přístup. Vydání šesté. New York, NY: McGraw-Hill; 2005.
9. Revize označování přípravků. Sebevražednost a antidepresiva. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Přístup 5. října 2009.
10. Informace o léčivých přípravcích. Řada Micromedex Healthcare. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Přístup 5. října 2009.
11. Shin J-G, Park J-Y, Kim M-J, et al. Inhibiční účinky tricyklických antidepresiv na lidské enzymy cytochromu P450 in vitro: mechanismus lékové interakce mezi TCA a fenytoinem. Drug Metab Dispos. 2002;30:1102-1107.
12. Brown CH. Přehled lékových interakcí se SSRI. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Metabolické lékové interakce s novými psychotropními látkami. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. Kvantifikace a mechanismus interakce fluoxetinu a tricyklických antidepresiv. Clin Pharmacol Ther. 1992;51:239-248.
15. Příbalová informace přípravku Cymbalta (duloxetin-hydrochlorid). Indianapolis, IN: Eli Lilly and Company; únor 2009. http://pi.lilly.com/us/cymbalta-pi.pdf. Dostupné 5. října 2009.
16. Goetz CG, Tanner CM, Klawans HL. Bupropion u Parkinsonovy nemoci. Neurologie. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Algoritmy pro velkou depresivní poruchu. Texas Department of State Health Services; červenec 2008. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Dostupné 5. října 2009.
Chcete-li se k tomuto článku vyjádřit, kontaktujte [email protected].
.