US Pharm. 2009;34(11):26-39.
Usikkerheden er stor, når det drejer sig om at vælge det rette antidepressivt middel til patienter, der er diagnosticeret med en større depressiv lidelse (MDD), ikke kun fordi undersøgelser ikke har rapporteret om nogen forskelle i effektivitet mellem midlerne, men også fordi kun 11 % til 30 % af patienterne opnår remission med den indledende behandling, selv efter et år.1,2 Dette har derfor fået klinikere til at praktisere på en trial-and-error-måde til behandling af depression.3 Desuden blev den sidste større revision af Diagnostic and Statistical Manual of Mental Disorders (DSM-IV-TR) udarbejdet i 2000.4 I 2005 blev der offentliggjort en vejledende overvågning for at gennemgå vigtige sikkerhedsproblemer, der var opstået i forbindelse med nogle midler, f.eks. nefazodon, samt for at gennemgå to nye antidepressiva, der blev godkendt det år, escitalopram og duloxetin.5 Revision og opdatering af DSM-IV-TR (DSM-V-manuskriptet) er ikke planlagt før maj 2012. Der er derfor behov for en ajourført gennemgang for at hjælpe klinikere med at træffe beslutning om, hvilke midler der er egnede til behandling af de enkelte patienter.
Undersøgelsen Sequenced Treatment Alternatives to Relieve Depression (STAR*D) fra 2007 forsøgte at udvikle og evaluere gennemførlige behandlingsstrategier for at forbedre de kliniske resultater for patienter med behandlingsresistent depression, som blev identificeret med en aktuel større depressiv episode.6 Specifikt sigtede STAR*D mod at afgøre, hvilken af flere behandlinger der er det mest effektive “næste skridt” for patienter, som ikke opnår remission med en indledende eller efterfølgende behandling, eller som ikke kan tolerere behandlingen. De overordnede resultater af denne undersøgelse viste, at farmakologiske forskelle mellem psykotrope lægemidler ikke udmøntede sig i væsentlige kliniske forskelle, selv om tolerabiliteten var forskellig.6
Sigtet med denne artikel er at gennemgå behandlingsbeviser, der er tilgængelige i litteraturen, med henblik på at give en hurtig reference, der kan hjælpe klinikere med at træffe beslutning om det passende middel under hensyntagen til bivirkninger, lægemiddelinteraktioner og lægemiddelsikkerhed samt patientkarakteristika.
Hvad er depression?
Depression kan være en kronisk eller tilbagevendende psykisk lidelse, der viser sig med flere symptomer såsom deprimeret stemning, tab af interesse eller glæde, skyldfølelse, forstyrret søvn eller appetit, lav energi og vanskeligheder med at tænke.7 Depression kan føre til betydelig forringelse af en persons evne til at tage sig af hverdagens forpligtelser. Depression kan også føre til selvmord, en tragedie, som hvert år koster ca. 850.000 mennesker på verdensplan livet.7
Frekvens og risikopopulationer
Der skønnes at være 121 millioner mennesker på verdensplan, der er ramt af depression.7 I 2000 var depression den fjerde største bidragyder til den globale sygdomsbyrde blandt alle sygdomme, og i 2020 forventes det, at den vil stige til den næststørste bidragyder til den globale sygdomsbyrde, kun overgået af hjertesygdomme.7
Populationer med højere risiko for at udvikle depression omfatter kvinder, personer mellem 24 og 45 år og personer med førstegradsslægtninge med depression. Kvinder har en øget risiko for depression indtil 50’erne, og deres livstidsrisiko er to gange større end mænds. Personer mellem 24 og 45 år har den højeste risiko for at få en depression. Endelig er førstegradsslægtninge til deprimerede patienter 1,5 til 3 gange mere tilbøjelige til at opleve depression end andre.4,8
Patofysiologi og farmakoterapi Rationale
Biologiske og psykosociale årsager er blevet opstillet som hypoteser i et forsøg på at beskrive depressionens patofysiologi. Farmakologiske midler vil være rettet mod de biologiske årsager, der er knyttet til dysregulering af neurotransmitterne. Denne dysregulering beskrives ofte som en mangel på neurotransmitterniveauer i hjernen. Norepinephrin-, serotonin- og dopaminniveauerne kan være nedsat hos patienter med depression, hvorved en nedsat mængde af neurotransmittere forbindes med lidelsen.8 Rationalet for farmakoterapi har været at styrke disse mangler ved at blokere genoptagelsen eller forhindre enzymatisk metabolisme af neurotransmittere via antidepressiva. Samlet set sigter disse mekanismer mod at øge niveauet af neurotransmittere enten ved at tvinge neuronet til at fyre oftere og producere flere neurotransmittere eller ved at forhindre nedbrydning af selve neurotransmitteren.
Pharmakologiske midler
Der findes i øjeblikket flere klasser af midler til behandling af depression. De omfatter bl.a. selektive serotonin-genoptagelseshæmmere (SSRI), tricykliske antidepressiva (TCA), monoaminoxidasehæmmere (MAOI) og serotonin-norepinephrin-genoptagelseshæmmere (SNRI).
Antidepressiva er blevet forbundet med en øget risiko for selvmordstanker og selvmordstanker hos børn, unge og unge voksne i kortvarige placebokontrollerede undersøgelser af MDD på kort sigt. Enhver, der overvejer at anvende et antidepressivt middel til et barn, en teenager eller en ung voksen, skal afveje denne risiko mod det kliniske behov. Korttidsundersøgelser viste ikke en stigning i risikoen for selvmord med antidepressiva sammenlignet med placebo hos voksne over 24 år, og der var en reduktion i risikoen med antidepressiva sammenlignet med placebo hos voksne på 65 år og derover. Depression og andre psykiatriske lidelser er i sig selv forbundet med øget risiko for selvmord. Patienter i alle aldre, der påbegyndes antidepressiv behandling, bør overvåges på passende vis og observeres nøje for klinisk forværring, selvmordstanker eller usædvanlige adfærdsændringer.9
Selektive serotonin genoptagelseshæmmere4,10: SSRI’er anses for at være førstevalgsmidler, når det gælder behandling af patienter med depression. Disse lægemidler omfatter citalopram, escitalopram, fluoxetin, fluvoxamin, paroxetin og sertralin (TABEL 1). De vigtigste bivirkninger i denne klasse omfatter kvalme, opkastninger og diarré, som er dosisafhængige virkninger og har tendens til at forsvinde efter de første ugers behandling. Hos nogle patienter kan SSRI’er forårsage agitation og søvnforstyrrelser, som også forsvinder med tiden. Seksuel dysfunktion er en bivirkning, der er til stede med alle antidepressiva, men synes at være mest almindelig med SSRI’er.
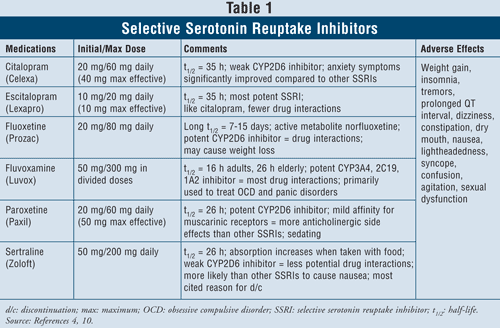
Serotoninsyndrom (dvs. mavesmerter, diarré, svedtendens, ændring af mental status, nyresvigt, kardiovaskulært chok og muligvis død) er en sjælden bivirkning ved SSRI’er. Serotoninsyndrom kan forekomme ved en forøgelse af SSRI-dosis eller ved indtagelse af SSRI’er sammen med urtemedicin såsom perikum eller med ulovlige stoffer. Endelig kan kombinationen af SSRI’er med MAOI’er også føre til dødelige lægemiddelinteraktioner med udvikling af serotoninsyndrom. Når klinikere føler behov for at skifte fra den ene klasse af midler til den anden, foreslås det, at der går mindst fem halveringstider mellem det tidspunkt, hvor SSRI’en stoppes, og MAOI’en startes.4 Af alle midler i klassen har fluvoxa mine den højeste rate af lægemiddelinteraktioner, da det hæmmer flere leverenzymer såsom CYP450 1A2, 2C19, 2C9, 2D6 og 3A4. Fluoxetin følger fluvoxamin’s lægemiddelinteraktionsrate tæt med hæmning af CYP 2C9, 2D6 og 3A4. Endelig har citalopram og escitalopram de mindste lægemiddelinteraktioner, da de hæmmer 2D6-enzymer i mindre grad.
Når man tager patientkarakteristika og sikkerhed i betragtning, er SSRI’er sikre at anvende i de fleste patientgrupper, herunder dem med allerede eksisterende hjertesygdomme, astma, demens og hypertension. De ældre, som er særligt udsat for ortostatisk hypotension samt vægttab, kan have størst fordel af at bruge SSRI’er, da disse midler giver vægtøgning og mangler antikolinergisk aktivitet.
Tricykliske antidepressiva4,10: TCA’er blokerer genoptagelse af noradrenalin og serotonin, men de har også affinitet for alfa1-, H1- og muskarinreceptorer og forårsager således antikolinergiske bivirkninger. Der findes to underklasser af midler inden for denne klasse, de tertiære og sekundære amin-TCA’er (TABEL 2). De sekundære amin-TCA’er (desipramin, maprotilin, nortriptylin) har mindre affinitet for alfa1-, H1- og muscarinreceptorer og forårsager derfor færre antikolinergiske bivirkninger end de tertiære amin-TCA’er (f.eks. amitriptylin, amoxapin, clomipramin, doxepin, imipramin).
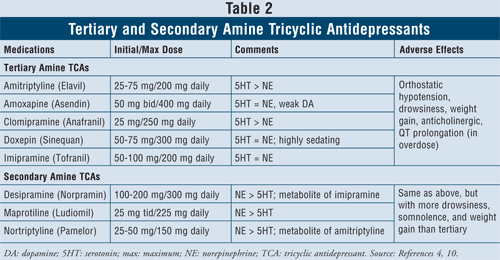
De vigtigste bivirkninger ved denne klasse af midler er ortostatisk hypotension, QT-forlængelse, døsighed, mundtørhed, sløret syn, forstoppelse og vægtøgning. Generelt har tertiære amin-TCA’er mere serotoninaktivitet i forhold til sekundære amin-TCA’er, som har mere noradrenalinaktivitet, hvilket medfører mindre døsighed, somnolens og vægtøgning.
Det er kendt, at TCA’er hæmmer både CYP 2C19- og 2D6-enzymerne.11 De metaboliseres også i mindre grad af CYP 1A2- og 3A4-enzymerne.12 Selv om lægemiddelinteraktioner med disse midler måske ikke er den primære bekymring, anbefales det derfor at udvise forsigtighed ved kombination af TCA’er med SSRI’er, da TCA’ernes plasmaindhold kan stige op til fire gange, hvilket muligvis kan føre til toksiske virkninger.13,14
Når man ser på patientkarakteristika og sikkerhed, er TCA’er kontraindiceret ved nogle specifikke hjertetilstande, såsom patienter med en historie med arytmier, sinusknude dysfunktion eller konduktionsfejl. Forsigtighed tilrådes hos ældre, da de er mere følsomme over for kolinerge blokade samt ortostatisk hypotension. Endvidere vil personer, der også lider af demens, være særligt modtagelige for de toksiske virkninger af muskarinblokade på hukommelse og opmærksomhedsspændvidde og vil generelt klare sig bedst, hvis de får antidepressiva med den laveste grad af antikolinergiske virkninger. Endelig bør der udvises forsigtighed, når man overvejer at starte TCA’er hos patienter med selvmordstanker på grund af den høje letalitetsrisiko ved overdosering. Den dødelige dosis er kun otte gange den terapeutiske dosis, så hvis TCA’er indtages i en overdosis, kan de blokere sinoatrialknuden i hjertet.
Monoaminoxidasehæmmere4,10: De MAOI’er, der er til rådighed, omfatter isocarboxazid, phenelzin, selegilin og tranylcypromin (TABEL 3). Bortset fra selegilin, som er en selektiv MAO B-hæmmer, hæmmer alle andre midler både MAO A- og B-enzymerne, der er ansvarlige for serotonin-, noradrenalin- og dopaminmetabolismen i hjernen. På grund af alvorlige bivirkninger og nødvendige diætrestriktioner er MAOI’er generelt forbeholdt patienter, der har fejlet med andre antidepressiva.
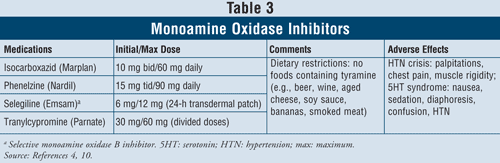
Hypertensiv krise kan opstå, når patienter, der tager MAOI’er, indtager fødevarer, der indeholder tyramin, som f.eks. øl, vin, lagret ost og røget kød. Denne reaktion viser sig som en akut indsættende alvorlig hovedpine, kvalme, nakkestivitet, hjertebanken, brystsmerter og forvirring. MAOI’er kan også forårsage serotoninsyndrom. Som tidligere nævnt opstår dette syndrom oftest, når MAOI’er tages samtidig med andre serotonerge midler såsom SSRI’er, eller hvis venlafaxin, en SNRI, indgives kort efter en MAOI. Når patienter skifter fra et SSRI med kort halveringstid til et MAOI, er det vigtigt, at der overholdes en 2-ugers vaskeperiode mellem ophør af SSRI’et og start af MAOI’et. Hvis fluoxetin er SSRI’et, som har en lang halveringstid, bør udskylningsperioden være 5 uger.4 Andre bivirkninger kan forekomme med MAOI’er såsom ortostatisk hypotension, vægtøgning, seksuel dysfunktion og søvnløshed.
På grund af den høje frekvens af lægemiddelinteraktioner med disse midler bør man være forsigtig, når de ordineres til patienter med astma, der bruger sympathomimetiske bronkodilatatorer. Hos patienter med hypertension kan MAOI’er fremkalde ortostatisk hypotension, især ved samtidig diuretisk behandling.
Serotonin-Norepinepinephrin-genoptagelseshæmmere4,10: SNRI’er såsom desvenlafaxin, duloxetin og venlafaxin kan også anvendes som førstevalgsmidler (TABEL 4). Disse lægemidler er mere sikre end TCA’er, og deres bivirkninger svarer til SSRI’ernes, herunder kvalme, opkastning og seksuel dysfunktion samt forhøjet blodtryk.
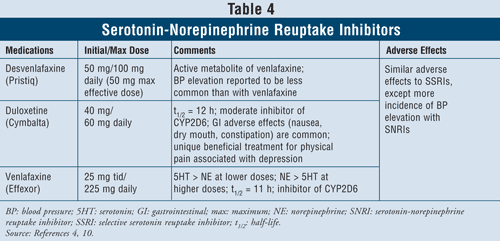
Venlafaxin har vist sig at forårsage en stigning i blodtrykket i 3 % til 13 % af tilfældene, mens desvenlafaxin blev rapporteret at forårsage en stigning i blodtrykket i kun 1 % til 2 % af tilfældene.10 Det anbefales således at undgå at anvende venlafaxin til patienter med ukontrolleret hypertension, da midlet kan forværre tilstanden. Duloxetin har mere noradrenalinaktivitet end begge de førnævnte midler og er således nyttigt ved fysiske symptomer såsom muskelsmerter, hovedpine, maveproblemer og generaliserede smerter, der ofte forekommer hos svært deprimerede patienter. På grund af dets effektivitet i forbindelse med smertesymptomer er duloxetin også blevet godkendt til andre indikationer såsom fibromyalgi og diabetiske perifere neuropatiske smerter.15 Endelig har alle tre midler mere serotonin- end noradrenalinaktivitet ved lavere doser og mere noradrenalin- end serotoninaktivitet ved højere doser, og de har således dosisafhængige bivirkninger.
Andre antidepressiva4,10: Der findes flere andre antidepressiva, som i deres virkningsmekanisme adskiller sig fra de tidligere beskrevne klasser af lægemidler.
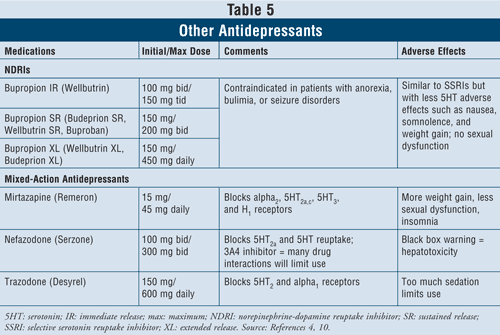
Norepinephrin-dopamin-genoptagelseshæmmere (NDRI’er) såsom bupropion med øjeblikkelig frigivelse (IR) af mærket Wellbutrin (fås også i langtidsvirkende doseringsformer såsom Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL og Buproban) kan anvendes som førstevalgsmidler til behandling af depression (TABEL 5). Deres bivirkninger svarer til SSRI’ernes bivirkninger, med minimale serotoninvirkninger såsom kvalme og vægtøgning og ringe eller ingen seksuel dysfunktion. Bupropion har vist sig at udøve gavnlige virkninger på Parkinsons sygdomssymptomer hos nogle patienter, men det kan også fremkalde nogle psykotiske symptomer, måske på grund af dets agonistiske virkning på det dopaminerge system.16
Endelig er der yderligere tre antidepressiva med blandet virkning til rådighed: mirtazapin, nefazodon og trazodon (TABEL 5). Alle tre midler blokerer forskellige serotoninreceptorer og har således forskellige virkninger. Mirtazapin forårsager mere vægtøgning ved at øge appetitten. Nefazodon har begrænset anvendelse på grund af hepatotoksicitet og CYP3A4-enzymhæmning, hvilket fører til lægemiddelinteraktioner. Trazodon blokerer i stor udstrækning serotoninreceptorer med ringe binding til muscarinreceptorer. Der kan forekomme bivirkninger såsom sedation, hovedpine, hukommelsesforstyrrelser, mundtørhed og forstoppelse. Forsigtighed tilrådes også ved brug af trazodon hos mænd på grund af risiko for priapisme.
Konklusion
Generelt har antidepressive lægemidler vist sig at være lige effektive; Derfor bør valget af medicin være baseret på bivirkninger, lægemiddelinteraktioner, sikkerhed og patientens præferencer. Der findes flere algoritmer til at vejlede klinikeren under patientens behandling, især den nyligt opdaterede algoritme fra Texas Department of State Health Services til behandling af MDD (opdateret juli 2008).17 Hvis patienter viser delvis respons, kan klinikere vælge at øge dosis, skifte til et alternativt middel eller give en kombination af antidepressiva. Hvis patienterne derimod ikke reagerer eller ikke kan tåle lægemidlet, er det også hensigtsmæssigt at skifte til et alternativt middel, idet det tages i betragtning, at terapeutiske virkninger normalt vil indtræde mellem 4 og 6 uger, selv om bivirkninger kan forekomme efter 1 uges behandling.4,17 Desuden, selv om bivirkningerne forekommer tidligt i behandlingen, forsvinder de generelt efter 2 til 3 uger.4,17 Ikke desto mindre kan det antidepressivt middel, der mest sandsynligt vil sikre en patients forbedring og sikkerhed, i det mindste delvist bestemmes ved forsøg og fejltagelser. I betragtning af vanskeligheden ved at forudsige, hvilken medicin der både vil være effektiv for og tolereres af den enkelte patient, er det klogt og nyttigt at kende et bredt spektrum af antidepressiva.
1. Song F, Freemantle N, Sheldon TA, et al. Selektive serotonin-genoptagelseshæmmere: metaanalyse af effektivitet og acceptabilitet. BMJ. 1993;306;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRI’er versus andre antidepressiva til behandling af depressive lidelser. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selecting among second-step antidepressant medication monotherapies: predictive value of clinical, demographic, or first-step treatment features. Arch Gen Psychiatry. 2008;65;65:870-881.
4. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition, Text Revision (DSM-IV-TR). Washington, DC: American Psychiatric Association; 2000.
5. Arbejdsgruppe om svær depressiv lidelse. Guideline Watch: Practice Guidelines for the Treatment of Patients with Major Depressive Disorder. 2nd ed. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigating the Sequenced Treatment Alternatives to Relieve Depression (STAR*D)-undersøgelsen: praktiske resultater og konsekvenser for depressionsbehandling i primærsektoren. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Verdenssundhedsorganisationen. www.who.int/mental_health/management/depression/definition/en. Besøgt den 5. oktober 2009.
8. Dipiro JT, Talbert RL, Talbert RL, Yee GC, et al. Farmakoterapi: A Pathophysiologic Approach. 6th ed. New York, NY: McGraw-Hill; 2005.
9. Revisioner af produktmærkning. Selvmordstanker og antidepressive lægemidler. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Besøgt den 5. oktober 2009.
10. Lægemiddelinformation. Micromedex Healthcare Series. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Besøgt den 5. oktober 2009.
11. Shin J-G, Park J-Y, Kim M-J, et al. Inhiberende virkninger af tricykliske antidepressiva på humane cytokrom P450-enzymer in vitro: mekanisme for lægemiddelinteraktion mellem TCA’er og phenytoin. Drug Metab Dispos. 2002;30:1102-1107.
12. Brown CH. Oversigt over lægemiddelinteraktioner med SSRI’er. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Metaboliske lægemiddelinteraktioner med nye psykotrope stoffer. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. Kvantificering og mekanisme for interaktion mellem fluoxetin og tricykliske antidepressiva. Clin Pharmacol Ther. 1992;51:239-248.
15. Cymbalta (duloxetinhydrochlorid) indlægsseddel. Indianapolis, IN: Eli Lilly and Company; februar 2009. http://pi.lilly.com/us/cymbalta-pi.pdf. Tilgået den 5. oktober 2009.
16. Goetz CG, Tanner CM, Klawans HL. Bupropion ved Parkinsons sygdom. Neurology. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Major Depressive Disorder Algorithms. Texas Department of State Health Services; juli 2008. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Besøgt den 5. oktober 2009.
For at kommentere denne artikel bedes du kontakte [email protected].