1 – Definición
La DAVD es una enfermedad del músculo cardíaco asociada a arritmias ventriculares y muerte súbita. Se caracteriza por anomalías estructurales y funcionales del ventrículo derecho causadas por la sustitución del miocardio por tejido graso y fibroso. Los lugares de afectación de las anomalías anatómicas se encuentran en el denominado triángulo de la displasia (las áreas subtricuspídeas del ventrículo derecho, el ápex y el infundíbulo)(4).
La displasia arritmogénica del ventrículo derecho (DAVD) es una enfermedad hereditaria, que se hereda típicamente como un rasgo autosómico dominante con penetrancia variable y expresión incompleta(1). Existe una variante autosómica recesiva asociada a la queratosis palmoplantar y al vello de la mano, denominada enfermedad de Naxos.
2 – Prevalencia
La prevalencia en la población general es aproximadamente de 1:2500 a 1:5000
No obstante, depende de las circunstancias geográficas, por ejemplo en ciertas regiones de Italia (Padua, Venecia) y Grecia (isla de Naxos), la prevalencia está aumentada(2). Representa entre el 5% y el 10% de las muertes cardíacas súbitas inexplicables en individuos menores de 65 años(3).
Se presenta en adultos jóvenes con una relación hombre/mujer de 2,7/1. Después de la cardiopatía hipertrófica, es la primera causa de muerte súbita cardíaca en los jóvenes.
3 – Diagnóstico
El diagnóstico de la DAVD suele ser difícil porque no existe una prueba única. El diagnóstico se basa en la presencia de factores estructurales, histológicos, electrocardiográficos y genéticos según el informe de la Task Force de 1994 de McKenna et al (5) (tabla 1) y una modificación de la Task Force de Homid et al (6) (tabla 2) para aumentar la sensibilidad diagnóstica de los familiares de primer grado para la detección precoz de la enfermedad.
A) Historia clínica
En primer lugar, empezaremos por la herramienta más fácil, que es la historia clínica.
La presentación clínica varía desde las formas asintomáticas hasta las palpitaciones, la fatiga, el síncope o incluso el paro cardíaco generalmente durante el ejercicio. Estos síntomas se deben a latidos ectópicos ventriculares, taquicardia ventricular sostenida de configuración de bloqueo de rama izquierda o insuficiencia ventricular derecha(4).
Podemos identificar cuatro etapas en la historia natural de esta enfermedad(7):
a) la fase temprana o silenciosa, es una fase subclínica con anomalías estructurales ocultas
b) la fase inestable con trastorno eléctrico
c) la fase de insuficiencia ventricular derecha
d) la fase final con insuficiencia biventricular progresiva, imitando una miocardiopatía dilatada
B) Prueba diagnóstica
1.- Electrocardiograma
Hay varias características del ECG en el criterio diagnóstico de la DAVD:
a) Inversiones de la onda T en V1 a V3 (criterio diagnóstico menor, pero una de las anomalías más comunes del ECG presente en el 85% de los pacientes (8)
b) Duración del QRS = 110 ms en V1 a V3
c) Onda épsilon (potenciales eléctricos después del final del complejo QRS). Es un criterio diagnóstico importante que se encuentra hasta en el 30% de los casos de DAVD.
Se han descrito otros marcadores ECG de DAVD: Dispersión del QRS y del QT, bloqueo parietal definido como una duración del QRS en las derivaciones V1 a V3 que supera la duración del QRS en la derivación V6 en > 25 ms, un recorrido ascendente de la onda S prolongado en V1 a V3 = 55 ms (se observó como la característica del ECG más prevalente en el 95% de los casos de DAVD8
2.- Imágenes miocárdicas
2.1 Ecocardiografía
Es la técnica de imagen no invasiva más utilizada, pero no siempre es la técnica de imagen óptima en pacientes obesos y en pacientes con enfisema pulmonar.
La ecocardiografía es la aproximación diagnóstica inicial en pacientes con sospecha de DAVD. Los principales hallazgos son (9):
– dilatación e hipocinesia del ventrículo derecho
– dilatación aislada del tracto de salida del ventrículo derecho
– aumento de la reflectividad de la banda moderadora
– aneurismas de fin de diástole
– acinesis-discinesia del segmento inferobasal y del ápex del ventrículo derecho
– trabéculas apicales prominentes
2.2 Angiografía de contraste del ventrículo derecho
Esta técnica se considera el estándar de referencia para el diagnóstico de la DAVD (10). Consiste en áreas acinéticas-discinéticas localizadas en el triángulo anatómico de la displasia. Sin embargo, debido a una técnica invasiva, a la exposición a los rayos X y a la variabilidad interobservador, este método no se utiliza ampliamente (9).
2.3 Tomografía computarizada
La tomografía computarizada es capaz de diagnosticar a los pacientes con DAVD. Dery et al11, fueron los primeros en demostrar un ventrículo derecho hipocinético dilatado en un paciente con DAVD.
Los hallazgos de la DAVD en la tomografía computarizada con haz de electrones son7:
– la presencia de grasa epicárdica o depósitos de grasa intramiocárdica
– trabeculaciones conspicuas con baja atenuación
– ventrículo derecho dilatado e hipocinético
– aspecto festoneado de la pared del ventrículo derecho
Actualmente, la tomografía computarizada no es la modalidad de imagen opcional para el cribado inicial debido a la elevada carga de radiación.
2.4 Resonancia magnética cardiovascular
La resonancia magnética (RM) es una herramienta excelente para visualizar el ventrículo derecho, permite una evaluación tridimensional de la anatomía ventricular, de los volúmenes y, en comparación con otras técnicas, puede reconocer mejor la sustitución del tejido graso y fibroso del miocardio, aunque la infiltración grasa del ventrículo derecho no es exclusiva de la DAVD, ya que se produce en más del 50% de los corazones normales en personas de edad avanzada. Sin embargo, la presencia de una sustitución grasa transmural o un adelgazamiento difuso del miocardio del ventrículo derecho debe considerarse un criterio importante para el diagnóstico de la DAVD.
La RM puede utilizarse también para evaluar la función sistólica y diastólica. Varios estudios han abordado la presencia de disfunción diastólica del ventrículo derecho como un marcador temprano de la enfermedad (12)
Los criterios típicos que pueden demostrarse con la RM son:
– presencia de áreas de alta intensidad de señal que indican la sustitución del miocardio por grasa (criterio mayor)
– sustitución fibroadiposa que conduce a un adelgazamiento difuso del miocardio del ventrículo derecho (criterio mayor)
– aneurisma del ventrículo derecho y del tracto de salida del ventrículo derecho (criterio mayor)
– dilatación del ventrículo derecho y del tracto de salida del ventrículo derecho (cuando es grave, criterio mayor; cuando es leve, criterio menor)
– anomalías regionales de la contracción (criterio menor)
– disfunción sistólica global (criterio mayor) y disfunción diastólica global (criterio menor)
La resonancia magnética cardiovascular proporciona importantes criterios anatómicos, morfológicos, funcionales y fluidodinámicos para el diagnóstico de la DAVD, aunque el diagnóstico de la DAVD debe realizarse basándose en los criterios de la Task Force y no sólo en las anomalías estructurales.
2.5 Biopsia endomiocárdica
El diagnóstico histológico es definitivo, sin embargo la biopsia endomiocárdica es controvertida debido a la naturaleza segmentaria de la enfermedad y a que las muestras suelen obtenerse del septo (13). Pueden producirse complicaciones como el taponamiento y la perforación.
4 – Manejo de los pacientes con DAVD
Antes del tratamiento, hay que conocer los predictores de mortalidad y la estratificación del riesgo. El estudio de Hulot et al (14) encontró que al menos 1 episodio de taquicardia ventricular por bloqueo de rama izquierda, los signos clínicos de insuficiencia ventricular derecha y la disfunción ventricular izquierda se asociaban a muertes cardiovasculares.
El problema es que la aparición de la muerte súbita no está relacionada con la progresión de la enfermedad y la muerte súbita podría ser la primera manifestación de la enfermedad.
1.- Fármacos antiarrítmicos
Los fármacos antiarrítmicos son la terapia inicial y más utilizada. Se recomiendan los agentes bloqueantes beta-adrenérgicos para reducir la arritmia estimulada por los adrenérgicos.
El fármaco más eficaz es el sotalol. El sotalol fue más eficaz que los agentes betabloqueantes o la amiodarona en pacientes con taquicardia ventricular (TV) inducible y no inducible, administrado en dosis que oscilan entre 320 y 480 mg/día (el sotalol evitó la TV durante la estimulación ventricular programada en el 68%, mientras que la amiodarona lo hizo en el 26% y las clases Ia y Ib en el 5,6% y la clase Ic sólo en el 3% de los pacientes) (15).
2.- Ablación con catéter
La ablación por radiofrecuencia (RF) se utiliza en casos de taquicardia ventricular refractaria/intolerante a fármacos o incesante. El objetivo de la ablación por RF es eliminar las vías de conducción. Se asocia con un éxito completo sólo en el 30 al 65% de los casos. Debido a la naturaleza progresiva y difusa de la enfermedad, es difícil abolir múltiples focos arritmogénicos16.
El sustrato patológico se registra durante el estudio electrofisiológico como una señal endocárdica fraccionada de baja amplitud que refleja una disminución de la velocidad de conducción endocárdica local7.
3.- Tratamiento con desfibrilador cardioversor implantable
Los pacientes considerados de alto riesgo de muerte súbita cardíaca deben recibir un desfibrilador cardioversor implantable (DCI). Son aquellos que 1) han sido reanimados de una parada cardiaca con antecedentes de síncope, 2) tienen arritmias amenazantes que no se suprimen completamente con el tratamiento farmacológico antiarrítmico y 3) con antecedentes familiares de parada cardiaca en parientes de primer grado (prevención primaria).
Los DIC funcionan proporcionando estimulación antitaquicardia y descargas de desfibrilación cuando se producen arritmias.
El tratamiento con DIC es factible y seguro en pacientes con DAVD con una baja incidencia de complicaciones a corto y largo plazo. Esta herramienta tiene un papel importante en el tratamiento de las arritmias ventriculares, más de tres cuartas partes de los pacientes con DAVD recibieron un tratamiento adecuado con DCI durante una media de 3,5 años de seguimiento (17)
Sin embargo, puede haber complicaciones del tratamiento con DCI como resultado de la sustitución del miocardio del ventrículo derecho por grasa y tejido fibrótico. Entre ellas se encuentran la perforación causada por el adelgazamiento de la pared del ventrículo derecho, la dificultad en la colocación de los cables por amplitudes inadecuadas de la onda R o umbrales de estimulación elevados, la detección o estimulación inadecuada durante el seguimiento como consecuencia de la progresión de la enfermedad y el fracaso en la terminación de las arritmias ventriculares por el aumento de los umbrales de desfibrilación (18).
4.- Tratamiento de la insuficiencia cardíaca
Cuando aparece insuficiencia ventricular derecha o biventricular, el tratamiento consiste en la terapia actual para la insuficiencia cardíaca, que incluye diuréticos, betabloqueantes, inhibidores de la enzima convertidora de la angiotensina y anticoagulantes.
La terapia curativa en caso de insuficiencia cardíaca congestiva refractaria y/o arritmias es el trasplante cardíaco.
Figura 1. Registro de una onda épsilon post-excitación (flechas) en las derivaciones precordiales derechas.
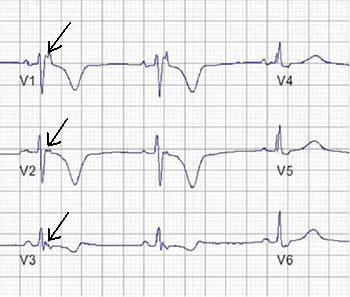
Figura 2. Registro de ECG de 12 derivaciones de TV con morfología de bloqueo de rama izquierda
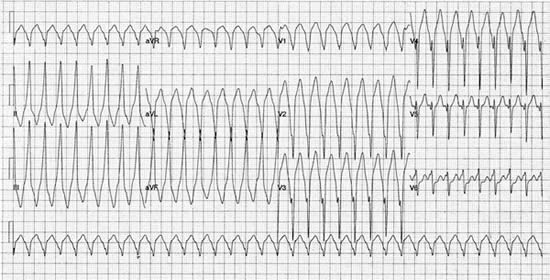
Tabla 1. Criterios para el diagnóstico de displasia ventricular derechaI Disfunción global y/o regional y alteraciones estructurales
| Mayor | Dilatación severa y reducción de la fracción de eyección del ventrículo derecho sin afectación del VI (o con afectación leve) |
| Aneurismas localizados del ventrículo derecho (áreas acinéticas o discinéticas con abombamiento diastólico) | |
| Dilatación segmentaria grave del ventrículo derecho | |
| Menor | Dilatación global leve del ventrículo derecho y/o reducción de la fracción de eyección con ventrículo izquierdo normal |
| Dilatación segmentaria leve del ventrículo derecho | |
| Hipoquinesia regional del ventrículo derecho |
II Caracterización tisular de las paredes
| Mayor | Reemplazo fibrograso del miocardio en la biopsia endomiocárdica |
III Anomalías de la repolarización
| Menor | Ondas T invertidas en las derivaciones precordiales derechas (V2 y V3) personas de más de 12 años; en ausencia de bloqueo de rama derecha |
IV Anomalías de despolarización/conducción
| Mayor | Ondas épsilon o prolongación localizada (>110 ms) del complejo QRS en las derivaciones precordiales derechas (V1-V3) |
| Menor | Potenciales tardíos (ECG de señal promediada) |
V Arritmias
| Menor | Taquicardia ventricular tipo bloqueo de rama izquierda (sostenida y no sostenida) (ECG, Holter, prueba de esfuerzo). |
| Extrasístoles ventriculares frecuentes (más de 1000/24h) |
VI Antecedentes familiares
| Mayores | Enfermedad familiar confirmada en la necropsia o en la cirugía |
| Menor | Antecedentes familiares de muerte súbita prematura (< 35 años) por sospecha de displasia ventricular derecha. |
| Antecedentes familiares (diagnóstico clínico basado en los criterios actuales) |
Tabla 2. Propuesta de modificación del Grupo de Trabajo para el diagnóstico de la DAVD familiar
DIAVD en un familiar de primer grado más uno de los siguientes:
| 1.- ECG | Inversión de la onda T en las derivaciones precordiales derechas (V2 y V3) |
| 2.- SAECG | Potenciales tardíos observados en el ECG de señal media (SAECG) |
| 3.- Arritmia | TV tipo LBBB en el ECG, en la monitorización Holter o durante la prueba de esfuerzo. Extrasístoles >200 en un período de 24 horas |
| 4.- Anomalía estructural o funcional del VD | Dilatación global leve del VD y/o reducción de la FE con VI normal Dilatación segmentaria leve del VD Hipoquinesia regional del VD |
El contenido de este artículo refleja la opinión personal del autor/es y no es necesariamente la posición oficial de la Sociedad Europea de Cardiología
.