Generikus név: naftifin-hidroklorid
Adagolási forma: krém
A Drugs.com által orvosilag felülvizsgált. Utolsó frissítés: 2021. január 1.
- Áttekintés
- Mellékhatások
- Adagolás
- Ellenőrzés
- Terhesség
- Tovább
A Naftifine krém javallatai és alkalmazása
A naftifine hidroklorid krém az interdigitális tinea pedis kezelésére javallt, tinea cruris és tinea corporis kezelésére, amelyet a Trichophyton rubrum szervezet okoz.
Naftifin krém adagolása és alkalmazása
Kizárólag helyi alkalmazásra. A Naftifin-hidroklorid krém nem szemészeti, orális vagy intravaginális alkalmazásra. A naftifin-hidroklorid krémet naponta egyszer vékony rétegben kell felvinni az érintett területekre, valamint a környező egészséges bőr ½ hüvelyknyi margójára 2 héten keresztül.
Adagolási formák és hatáserősségek
Minden gramm 20 mg naftifin-hidrokloridot (2%) tartalmaz fehér vagy törtfehér alapanyagban.
Ellenejavallatok
Nincs
Figyelmeztetések és óvintézkedések
Lokális mellékhatások
A kezelést meg kell szakítani, ha a naftifin-hidroklorid krém alkalmazása során irritáció vagy érzékenység alakul ki. Utasítsa a betegeket, hogy forduljanak orvosukhoz, ha ezek az állapotok a naftifin-hidroklorid krém alkalmazását követően alakulnak ki.
Mellékhatások
Klinikai vizsgálatok tapasztalatai
Mivel a klinikai vizsgálatokat igen eltérő körülmények között végzik, egy gyógyszer klinikai vizsgálataiban megfigyelt mellékhatások aránya nem hasonlítható össze közvetlenül egy másik gyógyszer klinikai vizsgálataiban megfigyelt arányokkal, és nem feltétlenül tükrözi a klinikai gyakorlatban megfigyelt arányokat.
A klinikai vizsgálatok során 903 alanyon alkalmazták a naftifin 1% és 2% krémformulákat. Összesen 564 interdigitális tinea pedisben, tinea crurisban vagy tinea corporisban szenvedő alanyt kezeltek naftifin-hidroklorid krémmel.
Két randomizált, hatóanyag-kontrollált vizsgálatban (400 alanyt kezeltek naftifin-hidroklorid krémmel). A populáció 12 és 88 év közötti, elsősorban férfi (79%), 48% kaukázusi, 36% fekete vagy afroamerikai, 40% spanyolajkú vagy latinó volt, és vagy túlnyomórészt interdigitális tinea pedisben vagy tinea crurisban szenvedett. A legtöbb alany naponta egyszer, helyileg, 2 héten keresztül kapott adagokat az érintett bőrfelületekre, valamint a környező egészséges bőr ½ hüvelyknyi margójára. A két, vivőanyaggal kontrollált vizsgálatban a naftifin-hidroklorid krémmel kezelt alanyok 17,5%-ánál jelentkezett mellékhatás, szemben a vivőanyaggal kezeltek 19,3%-ával. A leggyakoribb mellékhatás (nagyobb vagy egyenlő 1%-kal) a viszketés. A legtöbb mellékhatás enyhe súlyosságú volt. A mellékhatások előfordulása a naftifin-hidroklorid krémmel kezelt populációban nem különbözött szignifikánsan a vivőanyaggal kezelt populációtól.
Egy harmadik randomizált, vivőanyaggal kontrollált vizsgálatban 116 gyermekkorú, tinea corporisban szenvedő személyt kezeltek naftifin-hidroklorid krémmel. A populáció 2 évnél idősebb és 18 évnél fiatalabb (átlagéletkor 9 év), túlnyomórészt férfi (61%), 47% fehér, 51% fekete vagy afroamerikai, 92% spanyolajkú vagy latin-amerikai, és tinea corporisszal fertőzött volt. A naftifin-hidroklorid krémet 2 héten keresztül naponta egyszer helyileg alkalmazták a tinea corporisban szenvedő összes érintett testfelületen, valamint az érintett elváltozásokat körülvevő egészséges bőr ½ hüvelyknyi szélén. A mellékhatások előfordulása a naftifin-hidroklorid krémmel kezelt populációban nem különbözött jelentősen a vivőanyaggal kezelt populációtól.
Két nyílt gyermekgyógyászati farmakokinetikai és biztonsági vizsgálatban 49, 2 és 18 év közötti, interdigitális tinea pedisben, tinea crurisban és tinea corporisban szenvedő gyermek részesült naftifin-hidroklorid krémben. A gyermekpopulációban a mellékhatások előfordulása hasonló volt a felnőtt populációban megfigyelthez.
Marketing utáni tapasztalatok
A naftifin-hidroklorid engedélyezés utáni alkalmazása során a következő mellékhatásokat azonosították: bőrpír/irritáció, gyulladás, maceráció, duzzanat, égés, hólyagok, savós lefolyás, kérgesedés, fejfájás, szédülés, leukopénia, agranulocitózis.
Mivel ezeket a reakciókat önként jelentették egy bizonytalan méretű populációból, nem mindig lehet megbízhatóan megbecsülni a gyakoriságukat vagy megállapítani az okozati összefüggést a gyógyszer-expozícióval.
EGYEDI POPULÁCIÓKBAN ALKALMAZOTT ALKALMAZÁS
Várandósság
Kockázat összefoglalása
Nincsenek rendelkezésre álló adatok a naftifin-hidroklorid krémmel kapcsolatban terhes nőknél, amelyek tájékoztatnának a súlyos születési rendellenességek és vetélés gyógyszerrel összefüggő kockázatáról. Az állatokon végzett reprodukciós vizsgálatokban nem észleltek káros hatást az embrió magzati fejlődésére az organogenezis időszakában vemhes patkányoknál a maximálisan ajánlott humán dózis (MRHD) 18-szorosáig, illetve az organogenezis időszakában vemhes patkányoknál a MRHD 2-szereséig vagy vemhes nyulaknál a MRHD 4-szereséig szájon át beadott dózisoknál .
A súlyos születési rendellenességek és vetélés becsült háttérkockázata a jelzett populációra vonatkozóan nem ismert. Minden terhességnek megvan a születési rendellenesség, elvesztés vagy egyéb káros kimenetel háttérkockázata. Az Egyesült Államok általános populációjában a klinikailag felismert terhességekben a súlyos születési rendellenességek és a vetélés becsült háttérkockázata 2-4%, illetve 15-20%.
Adatok
Adatok állatokon
Szisztémás embrió- és magzati fejlődési vizsgálatokat végeztek patkányokon és nyulakon. Az állati és emberi dózisok testfelület-összehasonlításon alapuló összehasonlításához (mg/m2) az MRHD-t napi 8 g 2%-os krémben határozták meg (2,67 mg/kg/nap egy 60 kg-os egyén esetében).
30, 100 és 300 mg/kg/nap naftifin-hidroklorid orális dózisokat adtak vemhes nőstény patkányoknak az organogenezis időszakában. A 300 mg/kg/nap (az MRHD 18-szorosa) dózisig nem észleltek a kezeléssel összefüggő hatást az embrió magzati fejlődésére. A naftifin-hidroklorid 10 és 30 mg/kg/nap szubkután dózisát adták be vemhes nőstény patkányoknak az organogenezis időszakában. A 30 mg/kg/nap (az MRHD 2-szerese) adagolásnál nem észleltek a kezeléssel összefüggő hatást az embrió magzati fejlődésére. A naftifin-hidroklorid 3, 10 és 30 mg/kg/nap szubkután dózisát adták be vemhes nőstény nyulaknak az organogenezis időszakában. 30 mg/kg/nap (az MRHD 4-szerese) adagolásnál nem észleltek a kezeléssel összefüggő hatást az embrió magzati fejlődésére.
Patkányokon peri- és posztnatális fejlődési vizsgálatot végeztek. Naftifin-hidroklorid 30, 100 és 300 mg/kg/nap orális dózisát adták nőstény patkányoknak a 14. terhességi naptól a 21. laktációs napig. A nőstényeknél 300 mg/kg/nap (az MRHD 18-szorosa) esetén a vemhesség alatt és az utódoknál a laktáció alatt csökkent testtömeggyarapodást észleltek. Nem észleltek fejlődési toxicitást 100 mg/kg/nap (az MRHD 6-szorosa) mellett.
Laktáció
Kockázati összefoglaló
Nem áll rendelkezésre információ a naftifin-hidroklorid krém jelenlétéről az emberi tejben, a gyógyszer szoptatott csecsemőre gyakorolt hatásairól, vagy a gyógyszer tejtermelésre gyakorolt hatásairól. A szoptatás alatti klinikai adatok hiánya kizárja a naftifin-hidroklorid krém szoptatás alatti, csecsemőre gyakorolt kockázatának egyértelmű meghatározását; ezért a szoptatás fejlődését és egészségügyi előnyeit figyelembe kell venni az anya naftifin-hidroklorid krém iránti klinikai szükségletével és a szoptatott csecsemőre a naftifin-hidroklorid krém vagy az anyai alapbetegség esetleges káros hatásaival együtt.
GYermekgyógyászati alkalmazás
A naftifin-hidroklorid krém biztonságosságát és hatékonyságát a 12 éves és idősebb interdigitális tinea pedis és tinea cruris, valamint a 2 éves és idősebb tinea corporis gyermekbetegeknél megállapították .
A naftifin-hidroklorid krém alkalmazását ezekben a korcsoportokban a felnőtteken és gyermekeken végzett megfelelő és jól kontrollált vizsgálatok bizonyítékai támasztják alá, további biztonsági és PK-adatokat pedig a naftifin-hidroklorid krémnek kitett 49 gyermekgyógyászati alanyon végzett két nyílt vizsgálatból származó további biztonsági és PK-adatok .
A naftifin-hidroklorid krém biztonságosságát és hatékonyságát a tinea cruris és interdigitális tinea pedis kezelésében 12 évesnél fiatalabb gyermekgyógyászati betegeknél nem állapították meg. A naftifin-hidroklorid krém biztonságossága és hatékonysága a tinea corporis kezelésében 2 évesnél fiatalabb gyermekbetegeknél nem bizonyított.
Geriátriai alkalmazás
A naftifin-hidroklorid krémmel végzett klinikai vizsgálatok nem vontak be elegendő számú 65 éves és idősebb alanyokat annak megállapítására, hogy a fiatalabb alanyoktól eltérően reagálnak-e.
Naftifin krém leírása
A naftifin-hidroklorid krém, USP fehér vagy törtfehér színű krém, kizárólag helyi alkalmazásra. Minden gramm 20 mg naftifin-hidrokloridot, USP, (2%), egy szintetikus alilamin gombaellenes vegyületet tartalmaz.
Kémiailag a naftifin HCl (E)-N-Cinnamyl-N-methyl-1-napthalenemethylamine hydrochloride.
A molekuláris képlete C21H21N-HCl, molekulatömege 323,86.
A naftifin-hidroklorid, USP szerkezeti képlete:
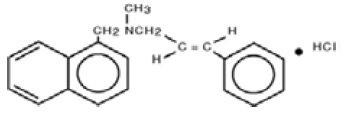
A naftifin-hidroklorid krém, USP a következő inaktív összetevőket tartalmazza: benzil-alkohol, cetil-alkohol, cetil-észterviasz, izopropil- mirisztát, poliszorbát 60, tisztított víz, nátrium-hidroxid, szorbitán-monosztearát és sztearil-alkohol. A pH beállításához sósav adható.
Naftifin krém – Klinikai farmakológia
Hatásmechanizmus
A naftifin-hidroklorid krém egy helyi gombaellenes gyógyszer.
Farmakodinamika
A naftifin-hidroklorid krém farmakodinamikáját nem állapították meg.
Farmakokinetika
In vitro és in vivo biológiai hozzáférhetőségi vizsgálatok kimutatták, hogy a naftifin elegendő koncentrációban hatol be a stratum corneumba ahhoz, hogy gátolja a dermatofiták növekedését.
A naftifin-hidroklorid krém farmakokinetikáját 21 felnőtt, férfi és nőnemű, tinea pedisben és tinea crurisban egyaránt szenvedő személyen végzett napi egyszeri helyi alkalmazást követően értékelték 2 héten keresztül. Az alkalmazott krém teljes mennyiségének mediánja 6,4 g (5,3 g és 7,5 g közötti tartomány) volt naponta. Az eredmények azt mutatták, hogy a naftifinnel szembeni szisztémás expozíció (azaz a maximális koncentráció (Cmax) és a 0-24 óra közötti görbe alatti terület (AUC0-24) mind a 21 alanynál nőtt a 2 hetes kezelési időszak alatt. Az AUC0-24 geometriai átlaga (variációs együttható vagy CV%) 117 (41,2) ng*hr/ml volt az 1. napon, és 204 (28,5) ng*hr/ml a 14. napon. A Cmax geometriai átlag (CV%) 7 ng/ml (55,6) volt az 1. napon és 11 ng/ml (29,3) a 14. napon. A Cmax érték eléréséig eltelt idő (Tmax) mediánja 8 óra (tartomány 4-24 óra) volt az 1. napon és 6 óra (tartomány 0-16 óra) a 14. napon. A felhalmozódás 14 napos helyi alkalmazás után kevesebb mint kétszeres volt. Az átlagkoncentrációk általában emelkedtek a 14 napos vizsgálati időszak alatt. A naftifin a 28. napon 13/21 (62%) alanynál továbbra is kimutatható volt a plazmában, az átlagos (szórás vagy SD) plazmakoncentráció 1,6 ± 0,5 ng/ml volt (a mennyiségi határ alatti (BLQ) és 3 ng/ml közötti tartomány). Ugyanebben a tinea pedisben és tinea crurisban szenvedő betegeken végzett farmakokinetikai vizsgálatban a kezelési időszak alatt a vizelettel ürülő dózis medián frakciója 0,0016% volt az 1. napon, míg a 14. napon 0,0020%.
Egy második, 22 alany bevonásával végzett vizsgálatban a naftifin-hidroklorid krém farmakokinetikáját 20, 13-18 évesnél fiatalabb, tinea pedisben és tinea crurisban egyaránt szenvedő gyermekgyógyászati alanyon értékelték. Az alanyokat átlagosan 8,1 g (6,6 g és 10,1 g közötti tartomány) adaggal kezelték, amelyet naponta egyszer, 2 héten keresztül alkalmaztak az érintett területekre. Az eredmények azt mutatták, hogy a szisztémás expozíció nőtt a kezelési időszak alatt. A geometriai átlag (CV%) AUC0-24 138 (50,2) ng*hr/ml volt az 1. napon, és 192 (74,9) ng*hr/ml a 14. napon. A Cmax geometriai átlag (CV %) 9,21 ng/ml (48,4) volt az 1. napon és 12,7 ng/ml (67,2) a 14. napon. A kezelési időszak alatt a vizelettel ürülő adag medián hányada 0,0030% volt az 1. napon és 0,0033% a 14. napon.
Egy harmadik vizsgálatban a naftifin-hidroklorid krém farmakokinetikáját vizsgálták 27, legalább közepesen súlyos tinea corporisban szenvedő, 2-12 évesnél fiatalabb gyermekkorú személyen. A vizsgálati alanyokat fiatalabb (2-6 éves korig, 17 alany) és idősebb (6-12 éves korig, 10 alany) csoportokra osztották. Az 1,3 g (1 g és 3,1 g közötti tartomány) és 2,3 g (2,2 g és 4,2 g közötti tartomány) medián adagot naponta egyszer alkalmazták 2 héten keresztül a fiatalabb és az idősebb csoportban az érintett területre és egy ½ hüvelykes margóra. A plazma és vizelet farmakokinetikai értékelését csak az idősebb csoportban az 1. napon, mindkét csoportban pedig a 14. napon végezték el. A naftifin-hidroklorid krém helyi alkalmazását követően valamennyi alany plazmájában mérhető naftifinszintet mutattak ki. Az 1. napon egyszeri adagot követően a 6-12 évesnél fiatalabb alanyoknál a Cmax és az AUC0-24 geometriai átlaga (CV%) 3,60 (76,6) ng/ml és 49,8 (64,4) ng*h/ml volt. A 14. napon ebben a csoportban a Cmax és az AUC0-24 3,31 (51,2) ng/ml és 52,4 (49,2) ng*h/ml volt. A 2-6 évesnél fiatalabb alanyoknál a 14. napon a Cmax és az AUC0-24 3,98 (186) ng/ml, illetve 54,8 (150) ng*h/ml volt. A 6-12 éves alanyok idősebb csoportjában a szisztémás expozíciók (mind a Cmax, mind az AUC0-24) az 1. és a 14. napon hasonlóak voltak. Az 1. és 14. napi gyógyszeralkalmazást követő 24 óra alatt a vizeletbe ürített dózis medián frakciója 0,0029%, illetve 0,0014% volt.
Mikrobiológia
Noha a gombák elleni pontos hatásmechanizmusa nem ismert, úgy tűnik, hogy a naftifin-hidroklorid a szkvalén2,3-epoxidáz enzim gátlásával beavatkozik a szterin bioszintézisbe.Az enzimaktivitás gátlása a szterolok, különösen az ergoszterol mennyiségének csökkenését és ennek megfelelően a szkvalén felhalmozódását eredményezi a sejtekben.
A rezisztencia mechanizmusa
A mai napig nem azonosították a naftifinnel szembeni rezisztencia mechanizmusát.
A naftifin a következő gombák legtöbb izolátumával szemben bizonyult aktívnak, mind in vitro, mind klinikai fertőzésekben, az INDIKÁCIÓK ÉS HASZNÁLATOK részben leírtak szerint:
Trichophyton rubrum
Nonklinikai toxikológia
Karcinogenezis, mutagenezis, termékenység károsodása
Egy 2 éves dermális karcinogenitási vizsgálatban a naftifin-hidroklorid krémet 1%, 2% és 3%-os helyi adagokban (10, 20 és 30 mg/kg/nap naftifin-hidroklorid) adták Sprague-Dawley patkányoknak. Ebben a vizsgálatban nem észleltek gyógyszerrel összefüggő daganatokat az ebben a vizsgálatban vizsgált legmagasabb, 30 mg/kg/nap dózisig (az AUC összehasonlítás alapján az MRHD 12-szerese).
A naftifin-hidroklorid nem mutatott mutagén vagy klasztogén potenciálra utaló jeleket két in vitro genotoxicitási vizsgálat (Ames-teszt és kínai hörcsög petefészeksejt kromoszóma-aberrációs vizsgálat) és egy in vivo genotoxicitási vizsgálat (egér csontvelő mikronukleusz vizsgálat) eredményei alapján.
A naftifin-hidroklorid orális adagolása patkányoknak a párzás, a vemhesség, az ellés és a laktáció során 100 mg/kg/nap dózisig (az MRHD hatszorosa) nem mutatott hatást a növekedésre, a termékenységre vagy a szaporodásra.
Klinikai vizsgálatok
Tinea Cruris
A naftifin-hidroklorid krém biztonságosságát és hatásosságát vizsgálták egy randomizált, kettős vak, járművekkel kontrollált, többközpontú vizsgálatban 146 tüneteket mutató és dermatofita kultúra pozitív tinea crurisban szenvedő személyen. Az alanyokat randomizálták, hogy naftifin-hidroklorid krémet vagy hordozót kapjanak. Az alanyok a naftifin-hidroklorid krémet vagy a vivőanyagot az érintett területre és az érintett területet körülvevő egészséges bőr ½ hüvelykes peremére kenték fel naponta egyszer 2 héten keresztül. A tinea cruris jeleit és tüneteit (erythema, viszketés és hámlás jelenléte vagy hiánya) értékelték, valamint KOH-vizsgálatot és dermatophyta tenyésztést végeztek a 4. héten, az elsődleges hatékonysági végponton.
A vizsgálati populáció átlagéletkora 47 év volt, 87%-a férfi és 43%-a fehér bőrű. A kiinduláskor a vizsgálati alanyoknál megerősítették a tinea cruris jeleit és tüneteit, pozitív KOH-vizsgálatot és a központi mikológiai laboratóriumból származó tenyésztési eredmények alapján megerősített dermatofita jelenlétet. A kezelési szándékkal rendelkező populáció elemzése a 4. heti látogatáskor teljes gyógyulással rendelkező alanyok arányának összehasonlítása volt (lásd az 1. táblázatot). A teljes gyógyulást klinikai gyógyulásként (erythema, viszketés és hámlás hiánya) és mikológiai gyógyulásként (negatív KOH és dermatofita tenyésztés) egyaránt definiálták.
A 4. héten klinikai gyógyulást és mikológiai gyógyulást tapasztaló alanyok százalékos arányát az alábbi 1. táblázat külön-külön mutatja be.
|
végpont |
Naftifin-hidroklorid krém, 2% |
Hordozó |
|
N=75 |
N=71 |
|
|
Teljes kurea |
19 (25%) |
2 (3%) |
|
Effektív kezelésb |
45 (60%) |
7 (10%) |
|
Mikológiai kúra |
54 (72%) |
11 (16%) |
|
a. A teljes gyógyulás a mikológiai gyógyulás és a klinikai gyógyulás összetett végpontja. A klinikai gyógyulás az erythema, a pruritus és a hámlás hiánya (0 fokozat). |
||
|
b. A hatékony kezelés negatív KOH preparátum és negatív dermatophyta tenyésztés, 0 vagy 1 fokozatú erythema, hámlás és pruritus (nincs vagy csaknem nincs). |
||
|
c. A mikológiai gyógyulást negatív KOH és dermatofita tenyésztésként határozzák meg. |
||
Interdigitális Tinea pedis
A naftifin-hidroklorid krém hatékonyságát vizsgálták egy randomizált, kettős vak, hatóanyag-kontrollált, többközpontú vizsgálatban 217 tüneteket mutató és dermatofita tenyésztés pozitív interdigitális tinea pedisben szenvedő személyen. Az alanyokat randomizálták, hogy naftifin-hidroklorid krémet vagy hordozót kapjanak. A vizsgálati alanyok a naftifin-hidroklorid krémet vagy a hordozót a lábfej érintett területére és az érintett területet körülvevő egészséges bőr ½ hüvelyknyi szélére kenték fel naponta egyszer 2 héten keresztül. Az interdigitális tinea pedis jeleit és tüneteit (erythema, viszketés és hámlás jelenléte vagy hiánya) értékelték, valamint KOH-vizsgálatot és dermatofita tenyésztést végeztek a 6. héten, az elsődleges hatékonysági végponton.
A vizsgálati populáció átlagéletkora 42 év volt, 71%-a férfi és 57%-a fehér bőrű. A vizsgálat kezdetén a vizsgálati alanyoknál megerősítették, hogy az interdigitális tinea pedis jelei és tünetei, pozitív KOH-vizsgálat és megerősített dermatofita tenyésztés volt. Az elsődleges hatékonysági végpont a 6. heti vizsgálat során teljes gyógyulást mutató alanyok aránya volt (lásd a 2. táblázatot). A teljes gyógyulást klinikai gyógyulásként (erythema, viszketés és hámlás hiánya) és mikológiai gyógyulásként (negatív KOH és dermatofita tenyésztés) egyaránt definiálták.
A 6. héten, négy héttel a kezelés befejezése után elért hatékonysági eredményeket az alábbi 2. táblázat mutatja be. A naftifin-hidroklorid krém teljes gyógyulást mutatott az interdigitális tinea pedisben szenvedő alanyoknál, de a csak mokaszin típusú tinea pedisben szenvedő alanyoknál teljes gyógyulás nem volt kimutatható.
|
végpont |
Naftifin-hidroklorid krém, 2% |
Hordozó |
|
N=147 |
N=70 |
|
|
Teljes kurea |
26 (18%) |
5 (7%) |
|
Effektív kezelésb |
83 (57%) |
14 (20%) |
|
Mikológiai kúra |
99 (67%) |
15 (21%) |
|
a. A teljes gyógyulás a mikológiai gyógyulás és a klinikai gyógyulás összetett végpontja. |
||
|
b. A hatékony kezelés negatív KOH-preparátum és negatív dermatophyta tenyésztés, 0 vagy 1 fokozatú erythema, hámlás és pruritus (hiányzik vagy majdnem hiányzik). |
||
|
c. A mikológiai gyógyulást negatív KOH és dermatofita tenyésztésként határozzák meg. |
||
Tinea corporis
A naftifin-hidroklorid krém biztonságosságát és hatékonyságát egy randomizált, kettős vak, járművekkel kontrollált, többközpontú vizsgálatban vizsgálták 184 tüneteket mutató és dermatofita tenyésztés pozitív tinea corporisban szenvedő személyen. Az alanyokat randomizálták, hogy naftifin-hidroklorid krémet vagy hordozót kapjanak. A vizsgálati alanyok a vizsgált hatóanyagot a tinea corporisban szenvedő összes érintett testfelületi területre, valamint az érintett elváltozásokat körülvevő egészséges bőr ½ hüvelykes peremére vitték fel két héten keresztül. A tinea corporis jeleit és tüneteit (erythema, induratio és viszketés jelenléte vagy hiánya) értékelték, valamint KOH-vizsgálatot és dermatophyta tenyésztést végeztek az elsődleges hatékonysági végpont értékeléséhez a 21. napon.
A vizsgálati populáció gyermekkorú volt (2 éves vagy annál idősebb és 18 évesnél fiatalabb), az átlagéletkor 9 év (naftifine hydrochloride cream) vagy 8 év (vehicle); a vizsgálati személyek 61%-a volt férfi és 45%-a fehér. A kiinduláskor a vizsgálati alanyoknál megerősítették a tinea corporis jeleit és tüneteit, pozitív KOH-vizsgálatot és megerősített dermatofita tenyésztést végeztek. Az elsődleges hatékonysági végpont a 21. napon teljes gyógyulást mutató alanyok aránya volt. A teljes gyógyulást úgy határozták meg, mint klinikai gyógyulást (erythema, induratio és viszketés hiánya a kiinduláskor jelenlévő összes elváltozáson) és mikológiai gyógyulást (negatív KOH és dermatophyta tenyésztés).
A 21. napon, egy héttel a kezelés befejezését követően a hatékonysági eredményeket az alábbi 3. táblázat mutatja be.
|
Naftifin-hidroklorid krém, 2% |
Hordozó |
|
|
Végpont |
N=91 |
N=93 |
|
Teljes kúra |
42 (46%) |
26 (28%) |
|
Effektív kezelésb |
53 (58%) |
32 (34%) |
|
Mikológiai kúra |
57 (63%) |
36 (39%) |
|
a. A teljes gyógyulás a mikológiai gyógyulás és a klinikai gyógyulás összetett végpontja. |
||
|
b. Hatékony kezelésnek minősül a negatív KOH-preparátum és a negatív dermatofita tenyésztés, az erythema, a bőrkeményedés és a viszketés 0 vagy 1 fokozatú (hiányzik vagy enyhe). |
||
|
c. A mikológiai gyógyulást negatív KOH és dermatofita tenyészetként határozzuk meg. |
||
HOW SUPPLIED/STORAGE AND HANDLING
Naftifine hydrochloride cream, USP 2%, fehér vagy törtfehér krém, amelyet az alábbi kiszerelésben szállítanak:
45 grammos tubusok – NDC 70700-161-18
60 grammos tubusok – NDC 70700-161-17
A naftifin-hidroklorid krémet 25°C-on (77°F) kell tárolni; 15° és 30°C (59° és 86°F) közötti eltérések megengedettek.
Betegtájékoztatás
- Tájékoztassa a betegeket, hogy a naftifin-hidroklorid krém kizárólag helyi alkalmazásra szolgál. A naftifin-hidroklorid krém nem szájon át történő, intravaginális vagy szemészeti alkalmazásra szolgál.
- Ha a naftifin-hidroklorid krém alkalmazása során irritáció vagy érzékenység alakul ki, a kezelést abba kell hagyni és megfelelő terápiát kell bevezetni. A betegeket arra kell utasítani, hogy forduljanak orvosukhoz, ha ezek az állapotok a naftifin-hidroklorid krém alkalmazását követően alakulnak ki.
Distributed by:
Xiromed, LLC,
Florham Park, NJ 07932
Rev. 09/2020
PI-161-00
PAKOLÁSI TABELLÁN MEGJELENŐ FELIRAT – 45g-os tubus

NDC 70700-161-18
Naftifine Cream, 2%
Xiromed, LLC
Csak helyi alkalmazásra
Nem szemészeti alkalmazásra, Orális vagy intravaginális használatra
45 g
Kizárólag orvosi rendelvényre
PAKOLÁSI TÁBLA ELLENŐRZÉSI TÁBLA – 60g tubus

NDC 70700-161-17
Naftifine Cream, 2%
Xiromed, LLC
Kizárólag helyi használatra
Nem szemészeti használatra, Orális vagy intravaginális használatra
60 g
Kizárólag orvosi rendelvényre
| NAFTIFINE HYDROCHLORIDE naftifine hydrochloride cream |
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
|
||||||||||||||||||||||||
| Marketing információk | |||
| Marketing kategória | Pályázati szám vagy monográfia hivatkozási száma | Marketing kezdete | Marketing vége |
| ANDA | ANDA210038 | 01/15/2021 | |
Címkéző – Xiromed, LLC (080228637)
Regisztráló – Xiromed Pharma España, S.L. (468835741)
Tovább a naftifine topikális
- Mellékhatások
- Terhesség vagy szoptatás alatt
- Adagolással kapcsolatos információk
- Árról & Kuponok
- En Español
- 7 Vélemények
- A gyógyszerosztály:
Fogyasztói források
- Betegtájékoztató
- Naftifine topikális (Korszerű olvasmány)
Szakmai források
- Receptköteles információk
- Naftifine (Szakmai betegtanácsadás)
- Naftifin gél (FDA)
Egyéb márkák Naftin
Kapcsolódó kezelési útmutatók
- Tinea pedis
- Tinea corporis
- Tinea cruris
Egészségügyi nyilatkozat