US Pharm. 2009;34(11):26-39.
A major depressziós zavarral (MDD) diagnosztizált betegek számára a megfelelő antidepresszáns kiválasztásakor nagy a bizonytalanság, nemcsak azért, mert a tanulmányok szerint nincs különbség a szerek hatékonysága között, hanem azért is, mert a betegeknek csak 11-30%-a ér el remissziót a kezdeti kezeléssel, még egy év elteltével is.1,2 Ez következésképpen arra késztette a klinikusokat, hogy próba és tévedés módszerével gyakorolják a depresszió kezelését3. Ráadásul a Mentális zavarok diagnosztikai és statisztikai kézikönyvének (DSM-IV-TR) legutóbbi nagy felülvizsgálata 2000-ben készült el.4 2005-ben iránymutatás-órát tettek közzé, amelyben áttekintették az egyes szerekkel, például a nefazodonnal kapcsolatban felmerült fontos biztonsági aggályokat, valamint az abban az évben engedélyezett két új antidepresszánst, az eszcitalopramot és a duloxetint.5 A DSM-IV-TR felülvizsgálata és frissítése (DSM-V kézirat) csak 2012 májusában esedékes. Ezért szükség van egy naprakész áttekintésre, amely segíti a klinikusokat az egyes betegek kezeléséhez szükséges megfelelő szerek kiválasztásában.
A 2007-es Sequenced Treatment Alternatives to Relieve Depression (STAR*D) vizsgálat arra tett kísérletet, hogy megvalósítható kezelési stratégiákat dolgozzon ki és értékeljen a klinikai eredmények javítására a kezelésre rezisztens depresszióban szenvedő, aktuális major depressziós epizóddal azonosított betegek esetében.6 A STAR*D célja konkrétan annak meghatározása volt, hogy a számos kezelés közül melyik a leghatékonyabb “következő lépés” azon betegek esetében, akik nem érnek el remissziót egy kezdeti vagy egy későbbi kezeléssel, vagy akik nem tolerálják a kezelést. A vizsgálat általános eredményei azt mutatták, hogy a pszichotróp gyógyszerek közötti farmakológiai különbségek nem jelentenek lényeges klinikai különbségeket, bár a tolerálhatóság különbözött.6
A cikk célja a szakirodalomban rendelkezésre álló kezelési bizonyítékok áttekintése, hogy egy gyors referenciát nyújtson, amely segít a klinikusoknak a megfelelő szer kiválasztásában, figyelembe véve a mellékhatásokat, a gyógyszerkölcsönhatásokat és a gyógyszerbiztonságot, valamint a betegek jellemzőit.
Mi a depresszió?
A depresszió krónikus vagy visszatérő mentális zavar lehet, amely számos tünettel jelentkezik, mint például levert hangulat, érdeklődés vagy örömvesztés, bűntudat, alvászavar vagy étvágytalanság, alacsony energia és gondolkodási nehézségek.7 A depresszió az egyénnek a mindennapi feladatok ellátására való képességében jelentős károsodáshoz vezethet. A depresszió öngyilkossághoz is vezethet, ami világszerte évente mintegy 850 000 ember életét követelő tragédia.7
Elterjedés és veszélyeztetett populációk
A becslések szerint világszerte 121 millió ember szenved depresszióban.7 2000-ben a depresszió az összes betegség közül a negyedik helyen állt a globális betegségterhelésben, és 2020-ra várhatóan a második helyre emelkedik a globális betegségterhelésben, a szívbetegségek után a második helyre.7
A depresszió kialakulásának nagyobb kockázatának kitett népességcsoportok közé tartoznak a nők, a 24 és 45 év közöttiek és azok, akiknek elsőfokú rokona depresszióban szenved. A nők 50 éves korukig fokozottan ki vannak téve a depresszió kockázatának, és az élethosszig tartó kockázatuk kétszer nagyobb, mint a férfiaké. A 24 és 45 év közötti embereknél a legmagasabb a depresszió előfordulási aránya. Végül a depressziós betegek elsőfokú rokonai 1,5-3-szor nagyobb valószínűséggel szenvednek depressziót, mint mások.4,8
Patofiziológia és farmakoterápia indoklása
A depresszió patofiziológiájának leírására tett kísérlet során biológiai és pszichoszociális okokat feltételeztek. A farmakológiai szerek a neurotranszmitterek diszregulációjához kapcsolódó biológiai okokat célozzák meg. Ezt a diszregulációt gyakran az agyi neurotranszmitterszintek hiányaként írják le. A noradrenalin, a szerotonin és a dopamin szintje csökkent lehet a depressziós betegeknél, így a neurotranszmitterek csökkent mennyiségét hozzák összefüggésbe a rendellenességgel.8 A farmakoterápia logikája az volt, hogy a neurotranszmitterek visszavételének blokkolásával vagy enzimatikus metabolizmusának megakadályozásával antidepresszánsok segítségével fokozzák ezeket a hiányosságokat. Összességében ezek a mechanizmusok a neurotranszmitterek szintjének növelését célozzák, vagy úgy, hogy a neuront arra kényszerítik, hogy gyakrabban tüzeljen és több neurotranszmittert termeljen, vagy úgy, hogy megakadályozzák magának a neurotranszmitternek a lebomlását.
Farmakológiai szerek
A depresszió kezelésére jelenleg többféle szercsoport áll rendelkezésre. Ezek közé tartoznak többek között a szelektív szerotonin visszavétel gátlók (SSRI-k), triciklikus antidepresszánsok (TCA-k), monoamino-oxidáz gátlók (MAOI-k) és szerotonin-noradrenalin visszavétel gátlók (SNRI-k).
Az antidepresszánsokat az MDD-vel kapcsolatos rövid távú placebokontrollos vizsgálatokban gyermekeknél, serdülőknél és fiatal felnőtteknél az öngyilkossági gondolkodás és az öngyilkossági hajlam fokozott kockázatával hozták összefüggésbe. Bárkinek, aki bármilyen antidepresszáns alkalmazását fontolgatja gyermek, serdülő vagy fiatal felnőtt esetében, mérlegelnie kell ezt a kockázatot és a klinikai szükségletet. A rövid távú vizsgálatok nem mutatták ki az antidepresszánsok szuiciditás kockázatának növekedését a placebóhoz képest 24 évesnél idősebb felnőtteknél, és a 65 éves és idősebb felnőtteknél a placebóhoz képest csökkent az antidepresszánsok kockázata. A depresszió és más pszichiátriai rendellenességek önmagukban is fokozott öngyilkossági kockázattal járnak. Az antidepresszáns terápiát megkezdett minden korú beteget megfelelően nyomon kell követni, és szorosan figyelni kell a klinikai állapotromlás, az öngyilkosság vagy a viselkedés szokatlan változásai szempontjából.9
Szelektív szerotonin visszavétel gátlók4,10: Az SSRI-ket első vonalbeli szereknek tekintik, amikor a depressziós betegek kezeléséről van szó. Ezek a gyógyszerek közé tartozik a citalopram, az eszcitalopram, a fluoxetin, a fluvoxamin, a paroxetin és a szertralin (1. TÁBLÁZAT). Ennek az osztálynak a fő mellékhatásai közé tartozik a hányinger, a hányás és a hasmenés, amelyek dózisfüggő hatások, és a kezelés első hetei után általában megszűnnek. Egyes betegeknél az SSRI-k nyugtalanságot és alvászavarokat okozhatnak, amelyek idővel szintén megszűnnek. A szexuális diszfunkció mellékhatás, amely minden antidepresszáns esetében jelen van, de úgy tűnik, hogy az SSRI-k esetében a leggyakoribb.
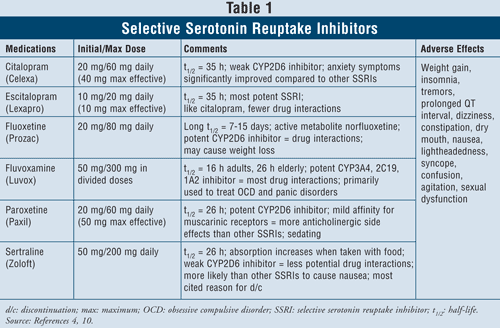
A szerotonin-szindróma (azaz hasi fájdalom, hasmenés, verejtékezés, mentális állapotváltozás, veseelégtelenség, kardiovaszkuláris sokk és esetleg halál) az SSRI-k ritka mellékhatása. A szerotonin-szindróma az SSRI-dózis növelésével vagy az SSRI-k gyógynövényekkel, például orbáncfűvel vagy tiltott kábítószerekkel együtt történő szedése esetén léphet fel. Végül az SSRI-k MAOI-kkal való kombinálása szintén halálos gyógyszerkölcsönhatásokhoz vezethet szerotonin-szindróma kialakulásával. Ha a klinikusok szükségét érzik, hogy az egyik szercsoportról a másikra váltsanak, azt javasolják, hogy legalább öt félév teljen el az SSRI abbahagyása és a MAOI elkezdése között.4 Az osztályba tartozó szerek közül a fluvoxa mine esetében a legmagasabb a gyógyszerinterakciók aránya, mivel számos májenzimet gátol, például a CYP450 1A2, 2C19, 2C9, 2D6 és 3A4 enzimeket. A fluvoxetin szorosan követi a fluvoxamin gyógyszerkölcsönhatási arányát a CYP 2C9, 2D6 és 3A4 gátlásával. Végül a citalopram és az eszcitalopram rendelkezik a legkevesebb gyógyszerkölcsönhatással, mivel kisebb mértékben gátolják a 2D6 enzimeket.
A betegjellemzőket és a biztonságosságot figyelembe véve az SSRI-k a legtöbb betegcsoportban biztonságosan alkalmazhatók, beleértve a már meglévő szívbetegségben, asztmában, demenciában és magas vérnyomásban szenvedőket is. Az idősek, akik különösen hajlamosak az ortosztatikus hipotenzióra, valamint a fogyásra, profitálhatnak leginkább az SSRI-k használatából, mivel ezek a szerek súlygyarapodást okoznak és nincs antikolinerg hatásuk.
Triciklikus antidepresszánsok4,10: A TCA-k blokkolják a noradrenalin és szerotonin visszavételét, de affinitással rendelkeznek az alfa1, H1 és muszkarin receptorokhoz is, így antikolinerg mellékhatásokat okoznak. Ezen az osztályon belül a szereknek két alosztálya áll rendelkezésre, a tercier és a szekunder amin TCA-k (2. TÁBLÁZAT). A másodlagos amin TCA-k (desipramin, maprotilin, nortriptilin) kisebb affinitással rendelkeznek az alfa1, H1 és muszkarin receptorokhoz, ezért kevesebb antikolinerg mellékhatást okoznak, mint a harmadlagos amin TCA-k (pl. amitriptilin, amoxapin, klomipramin, doxepin, imipramin).
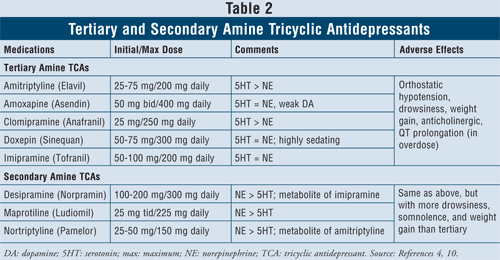
A szercsoport fő mellékhatásai az ortosztatikus hipotenzió, QT-meghosszabbodás, álmosság, szájszárazság, homályos látás, székrekedés és súlygyarapodás. Általában a tercier amin TCA-knak nagyobb a szerotoninaktivitásuk, szemben a szekunder amin TCA-kkal, amelyeknek nagyobb a noradrenalinaktivitásuk, így kevesebb álmosságot, somnolenciát és súlygyarapodást okoznak.
Tudott, hogy a TCA-k gátolják mind a CYP 2C19, mind a 2D6 enzimeket.11 Kisebb mértékben a CYP 1A2 és 3A4 enzimek is metabolizálják őket.12 Emiatt, bár a gyógyszer-gyógyszer kölcsönhatások e szerekkel nem feltétlenül jelentenek elsődleges problémát, a TCA-k SSRI-kkel való kombinálásakor óvatosság javasolt, mivel a TCA-k gyógyszerplazmaszintje akár négyszeresére is emelkedhet, ami esetleg toxikus hatásokhoz vezethet.13,14.
A betegjellemzőket és a biztonságosságot figyelembe véve a TCA-k ellenjavalltnak tekinthetők bizonyos speciális kardiológiai állapotokban, például olyan betegeknél, akiknek a kórtörténetében ritmuszavar, sinuscsomó-működési zavar vagy ingerületvezetési rendellenesség szerepel. Az idősek esetében óvatosság javasolt, mivel ők érzékenyebbek a kolinerg blokkolásra, valamint az ortosztatikus hipotenzióra. Továbbá a demenciában is szenvedő egyének különösen érzékenyek a muskarin-blokád memóriára és figyelemfelkeltésre gyakorolt toxikus hatásaira, és általában akkor járnak a legjobban, ha a legalacsonyabb antikolinerg hatású antidepresszánsokat kapják. Végezetül óvatosan kell eljárni, ha öngyilkossági gondolatokkal küzdő betegeknél a TCA-kezelés megkezdését fontolgatják a túladagolás magas halálozási kockázata miatt. A halálos dózis csak nyolcszorosa a terápiás dózisnak, így ha a TCA-k túladagolásban kerülnek bevitelre, blokkolhatják a szív sinoatrialis csomópontját.
Monoamin-oxidáz-gátlók4,10: A rendelkezésre álló MAOI-k közé tartozik az izokarboxazid, a fenelzin, a szelegilin és a tranyilcipromin (3. TÁBLÁZAT). A szelegilin kivételével, amely szelektív MAO B gátló, az összes többi szer mind a MAO A, mind a B enzimeket gátolja, amelyek az agyban a szerotonin, noradrenalin és dopamin metabolizmusáért felelősek. A súlyos mellékhatások és a szükséges étrendi korlátozások miatt a MAOI-kat általában olyan betegek számára tartják fenn, akiknél más antidepresszánsok nem használtak.
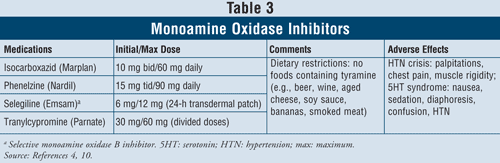
Hypertoniás krízis léphet fel, ha a MAOI-t szedő betegek tiramint tartalmazó élelmiszereket, például sört, bort, érlelt sajtot és füstölt húst fogyasztanak. Ez a reakció akut kezdődő súlyos fejfájás, hányinger, nyakmerevség, szívdobogás, mellkasi fájdalom és zavartság formájában jelentkezik. A MAOI-k szerotonin-szindrómát is okozhatnak. Mint korábban említettük, ez a szindróma leggyakrabban akkor fordul elő, ha a MAOI-kat más szerotonerg szerekkel, például SSRI-kkel egyidejűleg szedik, vagy ha a venlafaxint, egy SNRI-t, röviddel a MAOI után adják. Ha a betegeket rövid felezési idejű SSRI-ről MAOI-ra váltják, fontos, hogy az SSRI abbahagyása és a MAOI elkezdése között 2 hetes kimosási időszakot tartsanak be. Ha fluoxetin az SSRI, amelynek hosszú a felezési ideje, a kimosási időszaknak 5 hétnek kell lennie.4 A MAOI-k esetében egyéb mellékhatások is előfordulhatnak, mint például ortosztatikus hipotenzió, súlygyarapodás, szexuális diszfunkció és álmatlanság.
Az e szerekkel való gyógyszer-kölcsönhatások magas aránya miatt óvatosságra int, ha szimpatomimetikus hörgőtágítókat alkalmazó asztmás betegeknek írják fel. Magas vérnyomásban szenvedő betegeknél a MAOI-k ortosztatikus hipotenziót idézhetnek elő, különösen egyidejűleg alkalmazott diuretikus kezelések esetén.
Serotonin-Norepinefrin visszavétel gátlók4,10: Az SNRI-k, mint a desvenlafaxin, duloxetin és venlafaxin szintén alkalmazhatók első vonalbeli szerekként (4. TÁBLÁZAT). Ezek a gyógyszerek biztonságosabbak, mint a TCA-k, és mellékhatásaik hasonlóak az SSRI-kéhoz, beleértve a hányingert, hányást és szexuális diszfunkciót, valamint az emelkedett vérnyomást.
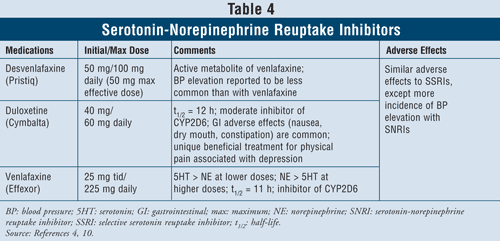
A venlafaxin az esetek 3-13%-ában okoz vérnyomás-emelkedést, míg a desvenlafaxin az esetek mindössze 1-2%-ában okozott vérnyomás-emelkedést.10 Ezért ajánlott elkerülni a venlafaxin alkalmazását kontrollálatlan magas vérnyomásban szenvedő betegeknél, mivel a szer súlyosbíthatja az állapotot. A duloxetin nagyobb noradrenalin-aktivitással rendelkezik, mint mindkét fent említett szer, így hasznos lehet az olyan fizikai tünetek, mint az izomfájdalmak, fejfájás, gyomorproblémák és általános fájdalom esetén, amelyek gyakran előfordulnak súlyosan depressziós betegeknél. A fájdalom tüneteinek hatékonysága miatt a duloxetint más javallatokra is engedélyezték, például fibromyalgiára és diabéteszes perifériás neuropátiás fájdalomra.15 Végül mindhárom szer alacsonyabb dózisban több szerotonin-, mint noradrenalin-aktivitást mutat, magasabb dózisban pedig több noradrenalin-, mint szerotonin-aktivitást, így dózisfüggő káros hatásai vannak.
Más antidepresszánsok4,10: Számos egyéb antidepresszáns áll rendelkezésre, amelyek hatásmechanizmusukban különböznek a korábban ismertetett gyógyszercsoportoktól.
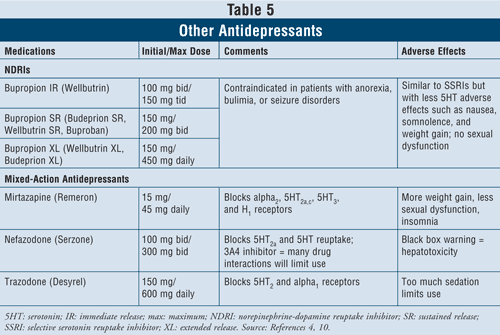
A noradrenalin-dopamin visszavétel gátlók (NDRI), mint például a Wellbutrin márkájú, azonnali felszabadulású (IR) bupropion (hosszú hatású gyógyszerformákban is kapható, mint például Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL és Buproban), első vonalbeli szerek lehetnek a depresszió kezelésére (5. TÁBLÁZAT). Mellékhatásaik hasonlóak az SSRI-okéhoz, minimális szerotoninhatással, például hányingerrel és súlygyarapodással, és kevés vagy semmilyen szexuális diszfunkcióval. A bupropionról kimutatták, hogy egyes betegeknél jótékony hatást gyakorol a Parkinson-kór tüneteire, de bizonyos pszichotikus tüneteket is kiválthat, talán a dopaminerg rendszerre gyakorolt agonista hatása miatt.16
Végül még három vegyes hatású antidepresszáns áll rendelkezésre: a mirtazapin, a nefazodon és a trazodon (5. TÁBLÁZAT). Mindhárom szer különböző szerotoninreceptorokat blokkol, így eltérő hatásúak. A mirtazapin az étvágy növelésével nagyobb súlygyarapodást okoz. A nefazodon korlátozottan alkalmazható a hepatotoxicitás és a CYP3A4 enzim gátlása miatt, ami gyógyszerkölcsönhatásokhoz vezet. A trazodon nagymértékben blokkolja a szerotoninreceptorokat, a muszkarinreceptorokhoz rosszul kötődik. Olyan mellékhatások léphetnek fel, mint a szedáció, fejfájás, memóriazavar, szájszárazság és székrekedés. A trazodon alkalmazása férfiaknál is óvatosságra int a priapizmus veszélye miatt.
Következtetés
Az antidepresszáns gyógyszerek általában egyformán hatásosnak bizonyultak; ezért a gyógyszerválasztásnak a mellékhatásokon, a gyógyszerkölcsönhatásokon, a biztonságosságon és a beteg preferenciáin kell alapulnia. Számos algoritmus áll rendelkezésre, amelyek a klinikusok számára iránymutatást adnak a beteg kezelése során, különösen a Texas Állami Egészségügyi Szolgálatok Minisztériumának nemrégiben frissített algoritmusa az MDD kezelésére (frissítve 2008 júliusában).17 Ha a betegek részleges választ mutatnak, a klinikusok dönthetnek úgy, hogy növelik a dózist, alternatív szerre váltanak, vagy antidepresszánsok kombinációját adják. Ezzel szemben, ha a betegek nem reagálnak, vagy nem tolerálják a gyógyszert, szintén indokolt alternatív szerre váltani, figyelembe véve, hogy a terápiás hatás általában 4-6 hét alatt jelentkezik, még akkor is, ha a mellékhatások már a kezelés 1 hete után jelentkezhetnek.4,17 Emellett, bár a mellékhatások a kezelés elején jelentkeznek, általában 2-3 hét után megszűnnek.4,17 Mindazonáltal, hogy melyik antidepresszáns biztosítja leginkább a beteg javulását és biztonságát, azt – legalábbis részben – próbálgatással lehet meghatározni. Tekintettel arra, hogy nehéz megjósolni, hogy egy adott beteg számára melyik gyógyszer lesz hatékony és tolerálható, az antidepresszánsok széles spektrumának ismerete óvatos és hasznos.
1. Song F, Freemantle N, Sheldon TA, et al. Selective serotonin reuptake inhibitors: meta-analysis of efficacy and acceptability. BMJ. 1993;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRI-k versus más antidepresszánsok depressziós zavar esetén. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selecting among second-step antidepressant medication monotherapies: predictive value of clinical, demographic, or first-step treatment features. Arch Gen Psychiatry. 2008;65:870-881.
4. American Psychiatric Association. A mentális zavarok diagnosztikai és statisztikai kézikönyve, negyedik kiadás, szöveges revízió (DSM-IV-TR). Washington, DC: Amerikai Pszichiátriai Társaság; 2000.
5. Major depressziós zavarral foglalkozó munkacsoport. Guideline Watch: Gyakorlati irányelvek a súlyos depressziós zavarban szenvedő betegek kezelésére. 2nd ed. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigálás a szekvenált kezelési alternatívák a depresszió enyhítésére (STAR*D) vizsgálatban: gyakorlati eredmények és következmények a depresszió kezelésére az alapellátásban. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Egészségügyi Világszervezet. www.who.int/mental_health/management/depression/definition/en. Hozzáférés 2009. október 5.
8. Dipiro JT, Talbert RL, Yee GC, et al. Pharmacotherapy: A Pathophysiologic Approach. 6th ed. New York, NY: McGraw-Hill; 2005.
9. A termékek címkézésének felülvizsgálata. Öngyilkosság és antidepresszáns gyógyszerek. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Hozzáférés 2009. október 5.
10. Gyógyszerekkel kapcsolatos információk. Micromedex Healthcare Series. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Hozzáférés 2009. október 5.
11. Shin J-G, Park J-Y, Kim M-J, et al. Triciklikus antidepresszánsok gátló hatása humán citokróm P450 enzimekre in vitro: a TCA-k és a fenitoin közötti gyógyszerkölcsönhatás mechanizmusa. Drug Metab Dispos. 2002;30:1102-1107.
12. Brown CH. Az SSRI-k gyógyszer-kölcsönhatásainak áttekintése. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Metabolikus gyógyszerkölcsönhatások új pszichotróp szerekkel. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. A fluoxetin és a triciklikus antidepresszánsok kölcsönhatásának számszerűsítése és mechanizmusa. Clin Pharmacol Ther. 1992;51:239-248.
15. Cymbalta (duloxetin-hidroklorid) betegtájékoztató. Indianapolis, IN: Eli Lilly and Company; 2009. február. http://pi.lilly.com/us/cymbalta-pi.pdf. Hozzáférés 2009. október 5.
16. Goetz CG, Tanner CM, Klawans HL. Bupropion a Parkinson-kórban. Neurológia. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Major depressziós zavar algoritmusai. Texas Állami Egészségügyi Minisztérium; 2008. július. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Hozzáférés 2009. október 5.
A cikkel kapcsolatos észrevételekért forduljon a [email protected] címre.
.