US Pharm. 2009;34(11):26-39.
L’incertezza è alta quando si tratta di selezionare l’antidepressivo appropriato per i pazienti con diagnosi di disturbo depressivo maggiore (MDD), non solo perché gli studi non hanno riportato differenze di efficacia tra gli agenti, ma anche perché solo l’11% al 30% dei pazienti raggiungerà la remissione con il trattamento iniziale, anche dopo un anno.1,2 Questo di conseguenza ha portato i medici a praticare in modo trial-and-error per trattare la depressione.3 Inoltre, l’ultima importante revisione del Manuale diagnostico e statistico dei disturbi mentali (DSM-IV-TR) è stata prodotta nel 2000.4 Nel 2005, è stata pubblicata una linea guida per rivedere importanti problemi di sicurezza che erano emersi su alcuni agenti, come il nefazodone, così come per rivedere due nuovi antidepressivi approvati quell’anno, escitalopram e duloxetina.5 La revisione e l’aggiornamento del DSM-IV-TR (manoscritto DSM-V) non è previsto fino a maggio 2012. Pertanto, c’è bisogno di una revisione aggiornata per aiutare i medici a decidere sugli agenti appropriati per trattare i singoli pazienti.
Lo studio Sequenced Treatment Alternatives to Relieve Depression (STAR*D) del 2007 ha cercato di sviluppare e valutare strategie di trattamento fattibili per migliorare gli esiti clinici per i pazienti con depressione resistente al trattamento che sono stati identificati con un episodio depressivo maggiore in corso.6 In particolare, STAR*D mirava a determinare quale dei diversi trattamenti è il “passo successivo” più efficace per i pazienti che non raggiungono la remissione con un trattamento iniziale o successivo o che non possono tollerare il trattamento. I risultati generali di questo studio hanno dimostrato che le differenze farmacologiche tra i farmaci psicotropi non si sono tradotte in differenze cliniche sostanziali, anche se la tollerabilità differiva.6
Lo scopo di questo articolo è quello di rivedere le prove di trattamento disponibili in letteratura al fine di fornire un rapido riferimento che aiuterà i medici a decidere l’agente appropriato, prendendo in considerazione gli effetti avversi, le interazioni farmacologiche e la sicurezza dei farmaci, nonché le caratteristiche del paziente.
Che cos’è la depressione?
La depressione può essere un disturbo mentale cronico o ricorrente che si presenta con diversi sintomi come umore depresso, perdita di interesse o di piacere, sentimenti di colpa, sonno disturbato o appetito, bassa energia e difficoltà di pensiero.7 La depressione può portare ad una sostanziale compromissione della capacità di un individuo di occuparsi delle responsabilità quotidiane. La depressione può anche portare al suicidio, una tragedia che causa la perdita di circa 850.000 vite in tutto il mondo ogni anno.7
Prevalenza e popolazioni a rischio
Si stima che nel mondo ci siano 121 milioni di persone affette da depressione.7 Nel 2000, la depressione era la quarta causa principale del carico globale di malattia tra tutte le malattie, ed entro il 2020 si prevede che salirà al secondo posto tra le cause principali del carico globale di malattia, seconda solo alle malattie cardiache.7
Le popolazioni a più alto rischio di sviluppare la depressione includono le donne, le persone tra i 24 e i 45 anni, e quelle con parenti di primo grado con depressione. Le donne sono a maggior rischio di depressione fino ai 50 anni, e il loro rischio nel corso della vita è due volte maggiore di quello degli uomini. Le persone tra i 24 e i 45 anni sperimentano il più alto tasso di depressione. Infine, i parenti di primo grado dei pazienti depressi hanno da 1,5 a 3 volte più probabilità di sperimentare la depressione rispetto agli altri.4,8
Patofisiologia e razionale della farmacoterapia
Cause biologiche e psicosociali sono state ipotizzate nel tentativo di descrivere la fisiopatologia della depressione. Gli agenti farmacologici mirano alle cause biologiche legate alla disregolazione dei neurotrasmettitori. Questa disregolazione è spesso descritta come una carenza nei livelli di neurotrasmettitori cerebrali. I livelli di noradrenalina, serotonina e dopamina possono essere diminuiti nei pazienti con depressione, associando così una quantità ridotta di neurotrasmettitori al disturbo.8 Il razionale della farmacoterapia è stato quello di aumentare queste carenze bloccando la ricaptazione o impedendo il metabolismo enzimatico dei neurotrasmettitori tramite gli antidepressivi. Nel complesso, questi meccanismi mirano ad aumentare il livello di neurotrasmettitori o costringendo il neurone a sparare più spesso e produrre più neurotrasmettitori o impedendo la degradazione del neurotrasmettitore stesso.
Agenti farmacologici
Diverse classi di agenti sono attualmente disponibili per trattare la depressione. Essi comprendono gli inibitori selettivi della ricaptazione della serotonina (SSRI), gli antidepressivi triciclici (TCA), gli inibitori delle monoamino ossidasi (MAOI) e gli inibitori della ricaptazione della serotonina-norepinefrina (SNRI), tra gli altri.
Gli antidepressivi sono stati associati a un aumento del rischio di pensieri suicidi e di suicidalità nei bambini, negli adolescenti e nei giovani adulti in studi a breve termine controllati con placebo sul MDD. Chiunque consideri l’uso di qualsiasi antidepressivo in un bambino, adolescente o giovane adulto deve bilanciare questo rischio con la necessità clinica. Gli studi a breve termine non hanno mostrato un aumento del rischio di suicidalità con gli antidepressivi rispetto al placebo negli adulti oltre i 24 anni, e c’era una riduzione del rischio con gli antidepressivi rispetto al placebo negli adulti di 65 anni e più. La depressione e altri disturbi psichiatrici sono a loro volta associati a un aumento del rischio di suicidio. I pazienti di tutte le età che sono iniziati alla terapia antidepressiva dovrebbero essere monitorati adeguatamente e osservati da vicino per il peggioramento clinico, suicidalità, o cambiamenti insoliti nel comportamento.9
Inibitori selettivi della ricaptazione della serotonina4,10: gli SSRI sono considerati agenti di prima linea quando si tratta di trattare i pazienti con depressione. Questi farmaci includono citalopram, escitalopram, fluoxetina, fluvoxamina, paroxetina e sertralina (TABELLA 1). I principali effetti avversi di questa classe includono nausea, vomito e diarrea, che sono effetti dose-dipendenti e tendono a dissiparsi dopo le prime settimane di trattamento. In alcuni pazienti, gli SSRI possono causare agitazione e disturbi del sonno, che si dissipano anch’essi con il tempo. La disfunzione sessuale è un effetto collaterale presente con tutti gli antidepressivi, ma sembra essere più comune con gli SSRI.
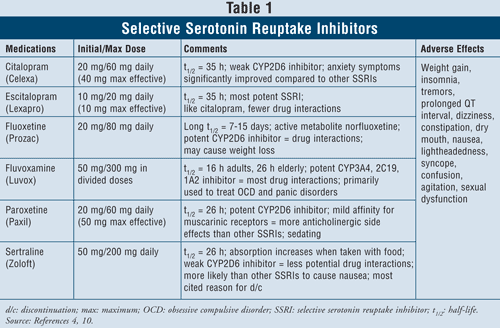
La sindrome da serotonina (cioè, dolore addominale, diarrea, sudorazione, cambiamento dello stato mentale, insufficienza renale, shock cardiovascolare e possibilmente morte) è un raro effetto avverso degli SSRI. La sindrome da serotonina può verificarsi con un aumento della dose di SSRI o con l’assunzione di SSRI con erbe come l’erba di San Giovanni o con droghe illecite. Infine, la combinazione di SSRI con MAOI può anche portare a interazioni farmacologiche letali con lo sviluppo della sindrome da serotonina. Quando i medici sentono la necessità di passare da una classe di agenti all’altra, si suggerisce che trascorrano almeno cinque emivite tra il momento in cui si interrompe l’SSRI e si inizia l’IMAO.4 Di tutti gli agenti della classe, il fluvoxa mine ha il più alto tasso di interazioni farmacologiche, poiché inibisce diversi enzimi epatici come il CYP450 1A2, 2C19, 2C9, 2D6, e 3A4. La fluoxetina segue da vicino il tasso di interazione farmacologica della fluvoxamina con l’inibizione del CYP 2C9, 2D6 e 3A4. Infine, il citalopram e l’escitalopram hanno le minori interazioni farmacologiche, poiché inibiscono gli enzimi 2D6 in misura minore.
Se si considerano le caratteristiche dei pazienti e la sicurezza, gli SSRI sono sicuri da usare nella maggior parte dei gruppi di pazienti, compresi quelli con malattia cardiaca preesistente, asma, demenza e ipertensione. Gli anziani, che sono particolarmente inclini all’ipotensione ortostatica e alla perdita di peso, possono beneficiare maggiormente dell’uso degli SSRI, poiché questi agenti producono un aumento di peso e non hanno attività anticolinergica.
Antidepressivi triciclici4,10: i TCA bloccano la ricaptazione di noradrenalina e serotonina, ma hanno anche affinità per i recettori alfa1, H1 e muscarinici, causando così effetti avversi anticolinergici. Ci sono due sottoclassi di agenti disponibili all’interno di questa classe, i TCA amminici terziari e secondari (TABELLA 2). I TCA amminici secondari (desipramina, maprotilina, nortriptilina) hanno meno affinità per i recettori alfa1, H1 e muscarinici, causando quindi meno effetti avversi anticolinergici rispetto ai TCA amminici terziari (per esempio, amitriptilina, amoxapina, clomipramina, doxepina, imipramina).
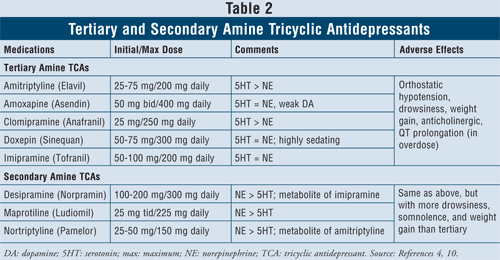
I principali effetti avversi di questa classe di agenti sono ipotensione ortostatica, prolungamento del QT, sonnolenza, bocca secca, visione offuscata, costipazione e aumento di peso. In generale, i TCA delle amine terziarie hanno più attività della serotonina rispetto ai TCA delle amine secondarie, che hanno più attività della norepinefrina, causando così meno sonnolenza, sonnolenza e aumento di peso.
È noto che i TCA inibiscono entrambi gli enzimi CYP 2C19 e 2D6.11 Sono anche metabolizzati in misura minore dagli enzimi CYP 1A2 e 3A4.12 Per questo motivo, anche se le interazioni farmaco-farmaco con questi agenti potrebbero non essere la preoccupazione principale, si consiglia di usare cautela quando si combinano i TCA con gli SSRI, dal momento che il livello plasmatico dei TCA può aumentare fino a quattro volte, portando eventualmente a effetti tossici.13,14
Quando si considerano le caratteristiche del paziente e la sicurezza, i TCA sono controindicati in alcune condizioni cardiache specifiche come i pazienti con una storia di aritmie, disfunzione del nodo del seno o difetti di conduzione. Si consiglia cautela con gli anziani, poiché sono più sensibili al blocco colinergico e all’ipotensione ortostatica. Inoltre, gli individui che soffrono anche di demenza saranno particolarmente suscettibili agli effetti tossici del blocco muscarinico sulla memoria e sulla capacità di attenzione e in genere farebbero meglio a somministrare antidepressivi con il più basso grado di effetti anticolinergici. Infine, la cautela dovrebbe essere esercitata quando si considera di iniziare i TCA in pazienti con pensieri suicidi a causa degli alti rischi di letalità con il sovradosaggio. La dose letale è solo otto volte la dose terapeutica, quindi se i TCA sono ingeriti in una dose eccessiva, possono bloccare il nodo senoatriale nel cuore.
Inibitori della monoammina ossidasi4,10: Gli IMAO che sono disponibili includono isocarboxazid, fenelzina, selegilina e tranilcipromina (TABELLA 3). A parte la selegilina, che è un inibitore selettivo delle MAO B, tutti gli altri agenti inibiscono entrambi gli enzimi MAO A e B responsabili del metabolismo di serotonina, norepinefrina e dopamina nel cervello. A causa dei gravi effetti avversi e delle restrizioni dietetiche richieste, gli IMAO sono generalmente riservati ai pazienti che hanno fallito altri antidepressivi.
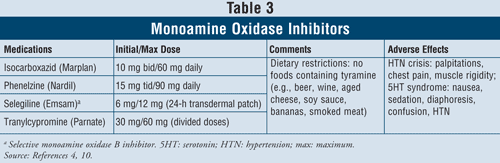
La crisi ipertensiva può verificarsi quando i pazienti che prendono gli IMAO ingeriscono alimenti contenenti tiramina, come la birra, il vino, il formaggio stagionato e la carne affumicata. Questa reazione si presenta come un inizio acuto di grave mal di testa, nausea, rigidità del collo, palpitazioni, dolore al petto e confusione. Gli IMAO possono anche causare la sindrome da serotonina. Come menzionato in precedenza, questa sindrome si verifica più comunemente quando gli IMAO vengono assunti in concomitanza con altri agenti serotoninergici come gli SSRI o se la venlafaxina, un SNRI, viene somministrata subito dopo un IMAO. Quando i pazienti passano da un SSRI con una breve emivita a un IMAO, è importante rispettare un periodo di washout di 2 settimane tra la sospensione dell’SSRI e l’inizio dell’IMAO. Se la fluoxetina è l’SSRI, che ha una lunga emivita, il periodo di washout dovrebbe essere di 5 settimane.4 Altri effetti avversi possono verificarsi con gli IMAO come ipotensione ortostatica, aumento di peso, disfunzione sessuale e insonnia.
A causa dell’alto tasso di interazioni farmacologiche con questi agenti, si deve usare cautela quando vengono prescritti a pazienti con asma che usano broncodilatatori simpaticomimetici. Nei pazienti con ipertensione, gli IMAO possono indurre ipotensione ortostatica, specialmente con trattamenti diuretici concomitanti.
Inibitori della ricaptazione della serotonina-norepinefrina4,10: Gli SNRI come desvenlafaxina, duloxetina e venlafaxina possono anche essere usati come agenti di prima linea (TABELLA 4). Questi farmaci sono più sicuri dei TCA, e i loro effetti avversi sono simili a quelli degli SSRI, tra cui nausea, vomito e disfunzioni sessuali, così come la pressione sanguigna elevata.
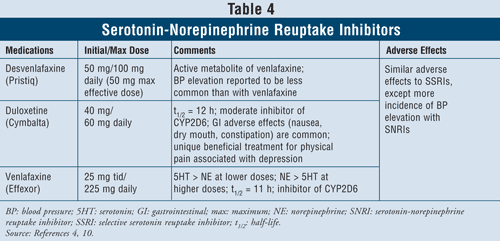
La venlafaxina ha dimostrato di causare un aumento della pressione sanguigna nel 3% al 13% dei casi, mentre la desvenlafaxina è stata segnalata per causare un aumento della pressione sanguigna solo nel 1% al 2% dei casi.10 Pertanto, si raccomanda di evitare l’uso di venlafaxina in pazienti con ipertensione non controllata poiché l’agente può aggravare la condizione. La duloxetina ha una maggiore attività della norepinefrina rispetto a entrambi gli agenti sopra citati, risultando così utile con sintomi fisici come dolori muscolari, mal di testa, problemi di stomaco e dolore generalizzato, che spesso si verificano nei pazienti gravemente depressi. Grazie alla sua efficacia nei sintomi del dolore, la duloxetina è stata approvata anche per altre indicazioni come la fibromialgia e il dolore neuropatico periferico diabetico.15 Infine, tutti e tre gli agenti hanno più serotonina che attività norepinefrina a basse dosi e più norepinefrina che attività serotonina a dosi più alte, avendo così effetti avversi dose-dipendenti.
Altri antidepressivi4,10: sono disponibili diversi altri antidepressivi che differiscono nel loro meccanismo d’azione dalle classi di farmaci descritti in precedenza.
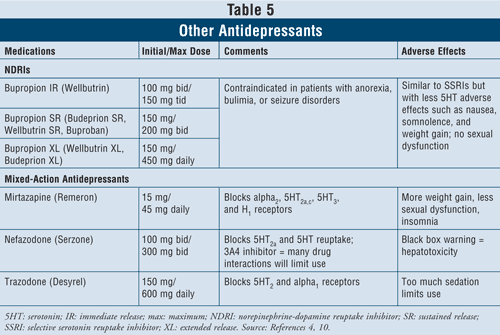
Gli inibitori della ricaptazione della norepinefrina-dopamina (NDRIs) come il bupropione a rilascio immediato (IR) di marca Wellbutrin (disponibile anche in forme di dosaggio a lunga durata d’azione come Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL, e Buproban) possono essere utilizzati come agenti di prima linea per trattare la depressione (TABELLA 5). I loro effetti avversi sono simili a quelli degli SSRI, con effetti minimi sulla serotonina come nausea e aumento di peso e poca o nessuna disfunzione sessuale. Il bupropione ha dimostrato di esercitare effetti benefici sui sintomi del morbo di Parkinson in alcuni pazienti, ma può anche indurre alcuni sintomi psicotici, forse a causa della sua azione agonistica sul sistema dopaminergico.16
Infine, sono disponibili altri tre antidepressivi ad azione mista: mirtazapina, nefazodone e trazodone (TABELLA 5). Tutti e tre gli agenti bloccano diversi recettori della serotonina, avendo così effetti distinti. La mirtazapina causa un maggiore aumento di peso aumentando l’appetito. Il nefazodone ha usi limitati a causa dell’epatotossicità e dell’inibizione dell’enzima CYP3A4, che porta a interazioni farmacologiche. Il trazodone blocca i recettori della serotonina in larga misura, con scarso legame ai recettori muscarinici. Possono verificarsi effetti avversi come sedazione, mal di testa, perdita di memoria, bocca secca e costipazione. Si consiglia inoltre cautela con l’uso di trazodone negli uomini a causa del rischio di priapismo.
Conclusione
In generale, i farmaci antidepressivi hanno dimostrato di essere ugualmente efficaci; Pertanto, la scelta dei farmaci dovrebbe essere basata sugli effetti avversi, le interazioni farmacologiche, la sicurezza e le preferenze del paziente. Sono disponibili diversi algoritmi per guidare il medico durante il trattamento del paziente, in particolare l’algoritmo recentemente aggiornato del Texas Department of State Health Services per il trattamento del MDD (aggiornato a luglio 2008).17 Se i pazienti mostrano una risposta parziale, i medici possono scegliere di aumentare la dose, passare a un agente alternativo o dare una combinazione di antidepressivi. Al contrario, se i pazienti non rispondono o non possono tollerare il farmaco, il passaggio a un agente alternativo è anche appropriato, tenendo in considerazione che gli effetti terapeutici di solito si verificano tra le 4 e le 6 settimane, anche se gli effetti avversi potrebbero apparire dopo 1 settimana di trattamento.4,17 Inoltre, mentre gli effetti avversi appaiono all’inizio del trattamento, generalmente si dissipano dopo 2 o 3 settimane.4,17 Tuttavia, l’antidepressivo che più probabilmente garantirà il miglioramento e la sicurezza di un paziente può essere determinato, almeno parzialmente, da prove ed errori. Data la difficoltà di prevedere quale farmaco sarà efficace e tollerato da un singolo paziente, la familiarità con un ampio spettro di antidepressivi è prudente e utile.
1. Song F, Freemantle N, Sheldon TA, et al. Inibitori selettivi della ricaptazione della serotonina: meta-analisi di efficacia e accettabilità. BMJ. 1993;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRIs versus altri antidepressivi per il disturbo depressivo. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selezione tra le monoterapie farmacologiche antidepressive di secondo passo: valore predittivo delle caratteristiche cliniche, demografiche o di trattamento di primo passo. Arch Gen Psychiatry. 2008;65:870-881.
4. American Psychiatric Association. Manuale diagnostico e statistico dei disturbi mentali, quarta edizione, revisione del testo (DSM-IV-TR). Washington, DC: American Psychiatric Association; 2000.
5. Gruppo di lavoro sul disturbo depressivo maggiore. Guarda la linea guida: Practice Guidelines for the Treatment of Patients with Major Depressive Disorder. 2a ed. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigazione nello studio Sequenced Treatment Alternatives to Relieve Depression (STAR*D): risultati pratici e implicazioni per il trattamento della depressione nell’assistenza primaria. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Organizzazione Mondiale della Sanità. www.who.int/mental_health/management/depression/definition/en. Accesso al 5 ottobre 2009.
8. Dipiro JT, Talbert RL, Yee GC, et al. Pharmacotherapy: A Pathophysiologic Approach. 6a ed. New York, NY: McGraw-Hill; 2005.
9. Revisioni dell’etichettatura del prodotto. Suicidalità e farmaci antidepressivi. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Accesso 5 ottobre 2009.
10. Informazioni sulla droga. Micromedex Healthcare Series. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Accessed October 5, 2009.
11. Shin J-G, Park J-Y, Kim M-J, et al. Effetti inibitori di antidepressivi triciclici su enzimi del citocromo P450 umano in vitro: meccanismo di interazione tra TCA e fenitoina. Drug Metab Dispos. 2002;30:1102-1107.
12. Marrone CH. Panoramica delle interazioni farmaco-farmaco con SSRIs. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Interazioni farmacologiche metaboliche con nuovi agenti psicotropi. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. Quantificazione e meccanismo dell’interazione tra fluoxetina e antidepressivi triciclici. Clin Pharmacol Ther. 1992;51:239-248.
15. Cymbalta (duloxetina cloridrato) foglietto illustrativo. Indianapolis, IN: Eli Lilly and Company; febbraio 2009. http://pi.lilly.com/us/cymbalta-pi.pdf. Accesso 5 ottobre 2009.
16. Goetz CG, Tanner CM, Klawans HL. Bupropione nella malattia di Parkinson. Neurologia. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Algoritmi per il disturbo depressivo maggiore. Texas Department of State Health Services; luglio 2008. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Accessed October 5, 2009.
Per commentare questo articolo, contattare [email protected].
.