30 anni maschio con visione centrale offuscata
Alex W. Cohen, MD, PhD e Jordan M. Graff, MD
Marzo 9, 2008
Aggiornato da Lindsay K. McConnell, MD
Maggio 8, 2017
Lavorazione principale: Visione centrale offuscata nell’occhio sinistro.
Storia della malattia attuale: Un uomo bianco di 30 anni ha notato una distorsione visiva centrale e la perdita della vista nell’occhio sinistro (OS) nelle ultime settimane. Il suo optometrista locale lo ha indirizzato all’Università dello Iowa Dipartimento di Oftalmologia e Scienze Visive per un’ulteriore valutazione.
Anamnesi oculare passata: Nessuno.
Anamnesi medica: Il paziente non ha riportato alcuna malattia sistemica o malattia precedente.
Medicazioni: Nessuna.
Anamnesi familiare: Nessuna malattia oculare familiare e per il resto non ha contribuito.
Anamnesi sociale: Sposato, vive con la moglie. Lavora come programmatore di computer. Il paziente ha vissuto nella valle del fiume Mississippi per tutta la sua vita.
Esame oculare:
- Acutezza visiva, senza correzione: Occhio destro (OD)–20/20; OS–20/40
- Motilità: Piena, entrambi gli occhi (OU)
- Pressione intraoculare: OD — 15 mmHg; OS — 16 mmHg
- Pupille: Ugualmente reattive alla luce. Nessun difetto pupillare afferente relativo (RAPD)
- Campi visivi di confronto (CVF): Completo, OU
- Esame del segmento esterno e anteriore: Normale, OU
- Esame del fondo dilatato (DFE):
- OD: vitreo chiaro e nervo ottico sano senza pallore o edema. C’è atrofia peripapillare e pigmentazione scura. Macula e vasi normali. In periferia ci sono alcune cicatrici corioretiniche “bucate”.
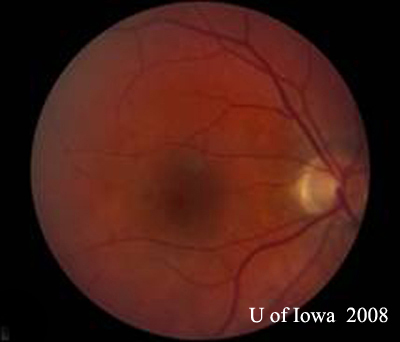
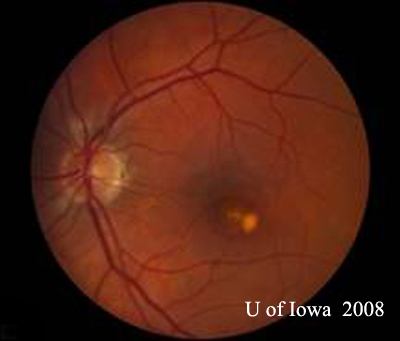
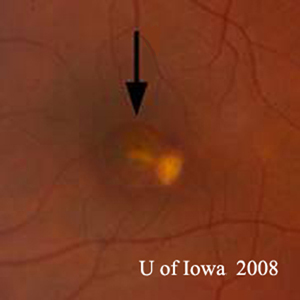
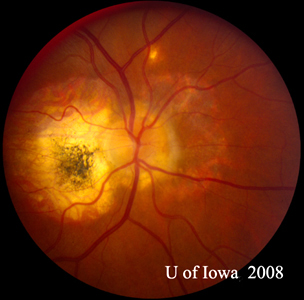
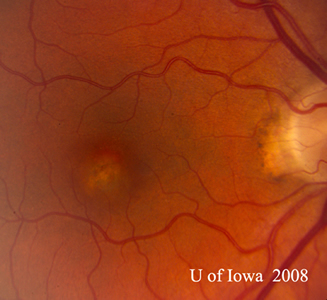
- OS: Vitreo chiaro con assolutamente nessuna cellula o segno di infiammazione. La testa del nervo ottico è sana senza pallore o edema. C’è atrofia peripapillare e aumento della pigmentazione. All’interno della macula, c’è una lesione subretinica giallastra in rilievo (vedi figure 1 e 2).
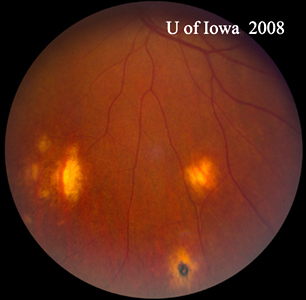
| A: foto del fundus a 30 gradi, OD. Notare i cambiamenti atrofici peripapillari. | B: foto del fundus a 30 gradi, OS. Sono evidenti modifiche atrofiche e pigmentarie peripapillari simili. Si noti l'”istospot” corioretinico all’interno della macula e l’assenza di qualsiasi infiammazione vitreale. |
 |
 |
|
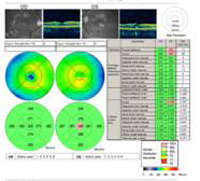
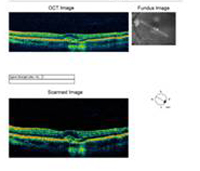
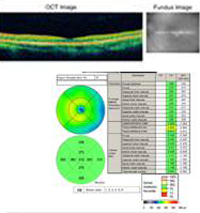
A: La tomografia a coerenza ottica (OCT) di entrambi gli occhi mostra un aumento dello spessore maculare centrale (CMT) OS (295µm) rispetto a OD (205µm). A). |
B: Si noti la presenza di liquido sottoretinico e la distorsione della depressione foveale, OS. |
 |
 |
Corso: Questo paziente ha una storia e un aspetto clinico fortemente suggestivi della presunta sindrome da istoplasmosi oculare (POHS). Mentre la sua lesione maculare spessa e gialla non è perfettamente classica (vedere la figura 5 e la discussione qui sotto), tutte le indicazioni suggeriscono che una membrana coroideale neovascolare (CNVM) si è sviluppata in questa macula sinistra nel sito di una cicatrice corioretinica. Abbiamo discusso a lungo con i pazienti le opzioni di trattamento, compresi gli studi clinici stabiliti per il laser maculare o la terapia fotodinamica (PDT) alla lesione. Inoltre, il paziente è stato informato dei primi risultati in letteratura e dell’esperienza personale che suggeriscono buoni risultati con l’uso off-label del bevacizumab intravitreale (Avastin). Il paziente scelse l’iniezione intravitreale, che fu eseguita senza complicazioni. È stato rivisto quattro settimane dopo l’iniezione, quando la sua visione era migliorata a 20/20 e la lesione retinica era asciutta sia clinicamente che tramite OCT (Figura 4).
Discorso: La presunta sindrome da istoplasmosi oculare (POHS) è una diagnosi clinica fatta sulla base di una costellazione di risultati oculari che sono stati originariamente descritti nel 1960. La sindrome è un disordine infiammatorio che è stato postulato come risultato di un’infezione sistemica con il fungo dimorfico Histoplasma capsulatum. Tuttavia, non ci sono stati studi di conferma che implicano direttamente questo fungo nella patogenesi della malattia. Piuttosto, i dati epidemiologici suggeriscono che la prevalenza della POHS è notevolmente aumentata nelle aree che sono endemiche per gli organismi Histoplasma. Classicamente, le persone che vivono nelle valli dei fiumi Ohio e Mississippi sono note per avere un tasso del 70% di test cutanei positivi per l’esposizione a H.capsulatum. Infatti, la grande maggioranza dei pazienti con POHS reagisce positivamente a questo test cutaneo. Tuttavia, solo circa il 4,4% dei pazienti con un test cutaneo positivo hanno prove di POHS. Pertanto, la relazione tra H. capsulatum e POHS rimane presunta.
Da notare che i pazienti con POHS sono spesso giovani e altrimenti sani e le lesioni retiniche possono produrre una significativa perdita visiva funzionale in questa popolazione in età lavorativa.
La diagnosi di POHS si basa sull’identificazione dei classici reperti del fundus. Questi sono la presenza di atrofia o pigmentazione peripapillare, la presenza di caratteristiche lesioni corioretiniche atrofiche “punched-out” e l’assenza di coinvolgimento del vitreo sovrastante. Si pensa che i cambiamenti peripapillari rappresentino una membrana neovascolare coroideale (CNVM) regredita, e che le lesioni “perforate” rappresentino aree di semina ematogena di H. capsulatum nella retina. Va notato che molte delle cicatrici corioretiniche periferiche “punched-out” possono anche essere associate a piccole CNVM che non vengono portate all’attenzione clinica e regrediscono spontaneamente. Esempi classici di queste lesioni possono essere visti nella Figura 5. Spesso, come nel caso qui presentato, la POHS si presenta all’attenzione dell’oculista con una CNVM sintomatica che coinvolge la macula o la fovea. In questo caso, la lesione maculare era un po’ insolita con una spessa sostanza gialla, mentre la CNVM nella POHS è spesso una rete di pizzo grigio-verde derivante da una cicatrice corioretinica (vedi Figura 6) che viene definita presto nell’angiogramma e perde tardi.
| A: POHS in un paziente con significativa atrofia peripapillare e cambiamento di pigmento, dimostrando l’aspetto di una CNVM peripapillare regredita che è stata postulata come fonte di queste lesioni. | B: Cicatrici corioretiniche periferiche in un paziente con POHS. |
 |
 |
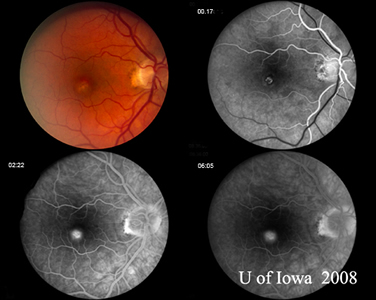
| A: CNVM maculare grigio-verde in un paziente con POHS | B: L’angiogramma in fluoresceina del paziente nella Figura 6A dimostra il classico modello di perdita associato alla CNVM nel paziente con POHS. |
 |
 |
La patogenesi della CNVM è sconosciuta; tuttavia, diversi autori hanno suggerito che in seguito alla diffusione ematogena degli organismi alla retina, si verificano aree di infiammazione focale, portando a una rottura della membrana di Bruch, e quindi predisponendo alla formazione della CNVM. La POHS è stata anche postulata come risultato di un innesco autoimmune, che viene stimolato dalla presenza dell’organismo infettivo. In ogni caso, i pazienti sono di solito o identificati mentre sono asintomatici (minoranza) o vengono all’attenzione di un oculista con lamentele di diminuzione della vista.
Il trattamento della POHS si è evoluto negli ultimi anni, e mentre non esiste una terapia diretta per colpire l’organismo, diverse modalità sono state identificate come utili nel trattamento della CNVM che l’accompagna. Storicamente, la fotocoagulazione laser ha portato all’inibizione di ben definite, classiche lesioni extrafoveali, juxtafoveali e peripapillari nella POHS. Tuttavia, lo scotoma centrale risultante era a volte inaccettabile al posto delle nuove opzioni terapeutiche. La terapia fotodinamica (PDT) con verteporfina è stata approvata dalla FDA per il trattamento della CNVM relativa alla POHS alla fine del 2001 e si è dimostrata sicura ed efficace per il trattamento della malattia. Una volta che gli agenti anti-VEGF si sono dimostrati efficaci nel trattamento della CNVM correlata alla AMD, a metà degli anni 2000 sono stati pubblicati dei case report che dimostravano il loro successo nel trattamento delle membrane neovascolari nei pazienti con POHS. Dopo la pubblicazione di numerosi case report e revisioni retrospettive che mostrano l’efficacia del trattamento con agenti anti-VEGF, questi sono diventati lo standard di cura utilizzando gli stessi principi di quelli per il trattamento della CNVM correlata alla AMD.
Diagnosi: Presunta sindrome da istoplasmosi oculare (POHS) con CNVM
EPIDEMIOLOGIA
|
SIGNI
|
SINTOMI
|
TREAZIONE
|
Diagnosi differenziale per cicatrice corioretinica maculare con liquido associato:
- Tossoplasmosi (avrebbe infiammazione del vitreo)
- Degenerazione miopica
- Strisce angioidi
- Età-Related Macular Degeneration (AMD)
- Corioretinopatia sierosa centrale (CSCR)
- Coroidopatia interna perforata (PIC)
- Coroidite multifocale (MFC)
- CNVM idiopatica
- Prasad AG, Van Gelder RN. Presunta sindrome da istoplasmosi oculare. Curr Opin Ophthalmol 2005;16(6):364-368. https://www.ncbi.nlm.nih.gov/pubmed/16264347
- Oliver A, Ciulla TA, Comer GM. Approfondimenti nuovi e classici sulla presunta sindrome da istoplasmosi oculare e sul suo trattamento. Curr Opin Ophthalmol 2005;16(3):160-165. https://www.ncbi.nlm.nih.gov/pubmed/15870572
- Rosenfeld PJ, Saperstein DA, Bressler NM, Reaves TA, Sickenberg M, Rosa RH, Jr., Sternberg P, Jr., Aaberg TM, Sr., Aaberg TM, Jr., Verteporfin in Ocular Histoplasmosis Study G. Photodynamic therapy with verteporfin in ocular histoplasmosis: uncontrolled, open-label 2-year study. Ophthalmology 2004;111(9):1725-1733. https://www.ncbi.nlm.nih.gov/pubmed/15350329
- Adan A, Navarro M, Casaroli-Marano RP, Ortiz S, Molina JJ. Intravitreal bevacizumab come trattamento iniziale per la neovascolarizzazione coroideale associata a presunta sindrome da istoplasmosi oculare. Graefes Arch Clin Exp Ophthalmol 2007;245(12):1873-1875. https://www.ncbi.nlm.nih.gov/pubmed/17786466
- Schadlu R, Blinder KJ, Shah GK, Holekamp NM, Thomas MA, Grand MG, Engelbrecht NE, Apte RS, Joseph DP, Prasad AG, Smith BT, Sheybani A. Intravitreal bevacizumab per neovascolarizzazione coroideale in istoplasmosi oculare. Am J Ophthalmol 2008;145(5):875-878. https://www.ncbi.nlm.nih.gov/pubmed/18321466
- Weingeist TA, Watzke RC. Coinvolgimento oculare da histoplasma capsulatum. Int Ophthalmol Clin 1983;23(2):33-47. https://www.ncbi.nlm.nih.gov/pubmed/6189798
- Cionni DA, Lewis SA, Petersen MR, Foster RE, Riemann CD, Sisk RA, Hutchins RK, Miller DM. Analisi dei risultati per bevacizumab intravitreale nel trattamento della neovascolarizzazione coroideale secondaria a istoplasmosi oculare. Ophthalmology 2012;119(2):327-332. https://www.ncbi.nlm.nih.gov/pubmed/22133795
- Degenerazione maculare legata all’età e altre cause di neovascolarizzazione coroideale. Corso di scienze di base e cliniche (BCSC) Sezione 12: Retina e vitreo. San Francisco: American Academy of Ophthalmology; 2014-2015.
Formato di citazione suggerito
McConnell LK. Revisione di ; EyeRounds.org. 5 luglio 2017; Disponibile da: http://www.EyeRounds.org/cases/83-Presumed-Ocular-Histoplasmosis-POHS.htm.
.