30-jarige man met wazig centraal zicht
Alex W. Cohen, MD, PhD and Jordan M. Graff, MD
March 9, 2008
Updated by Lindsay K. McConnell, MD
May 8, 2017
Chief Complaint: Wazig centraal zicht in het linkeroog.
Geschiedenis van de huidige ziekte: Een 30-jarige blanke man merkte de afgelopen weken centrale visuele vervorming en verlies van het gezichtsvermogen in het linkeroog (OS) op. Zijn plaatselijke optometrist verwees hem naar de Universiteit van Iowa Afdeling Oogheelkunde en Visuele Wetenschappen voor verdere evaluatie.
Vorige ooggeschiedenis: Geen.
Medische voorgeschiedenis: De patiënt meldde geen eerdere systemische ziekten of aandoeningen.
Medicijnen: Geen.
Familiegeschiedenis: Geen familiaire oogziekten en voor het overige niet-betrokken.
Sociale voorgeschiedenis: Getrouwd, woont samen met zijn vrouw. Hij werkt als computerprogrammeur. De patiënt heeft zijn hele leven in de Mississippi River Valley gewoond.
Oculair onderzoek:
- Visual Acuity, zonder correctie: Rechteroog (OD)-20/20; OS–20/40
- Motiliteit: Volledig, beide ogen (OU)
- Intraoculaire druk: OD — 15 mmHg; OS — 16 mmHg
- Pupillen: Gelijk reageren op licht. Geen relatieve afferente pupilafwijking (RAPD)
- Confrontatie gezichtsvelden (CVF): Volledig, OU
- Extern en voorste segment onderzoek: Normaal, OU
- Gedilateerd fundus onderzoek (DFE):
- OD: Helder glasvocht en gezonde oogzenuw zonder bleekheid of oedeem. Er is peripapillaire atrofie en donkere pigmentatie. Normale macula en vaten. In de periferie zijn er enkele “uitgestanste” chorioretinale littekens.
- OS: Helder glasvocht met absoluut geen cellen of tekenen van ontsteking. De kop van de oogzenuw is gezond zonder bleekheid of oedeem. Er is peripapillaire atrofie en verhoogde pigmentatie. Binnen de macula is er een verheven gelige subretinale laesie (zie figuren 1 en 2).
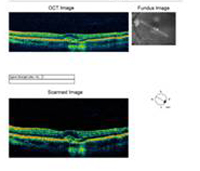
| A: 30-graden fundusfoto, OD. Let op de peripapillaire atrofische veranderingen. | B: 30-graden fundusfoto, OS. Vergelijkbare peripapillaire atrofische en pigment veranderingen zijn duidelijk. Let op de chorioretinale “histospot” binnen de macula en de afwezigheid van enige glasvochtontsteking. |
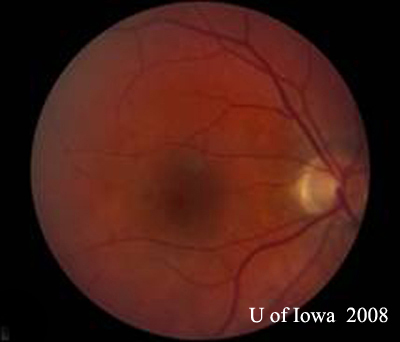 |
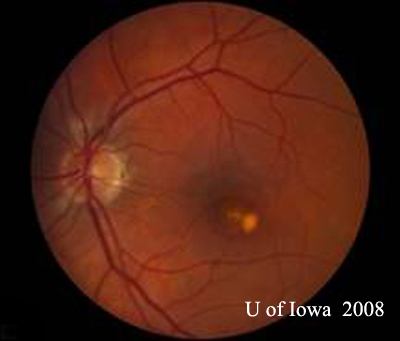 |
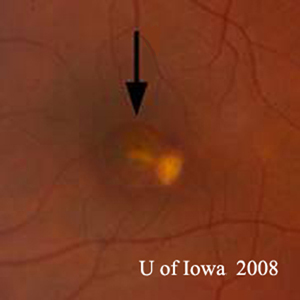
|
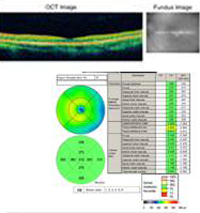
A: Optische Coherentie Tomografie (OCT) scans van beide ogen tonen een toename van de centrale maculaire dikte (CMT) OS (295µm) in vergelijking met OD (205µm). A). |
B: Let op de aanwezigheid van subretinale vloeistof en vervorming van de foveale depressie, OS. |
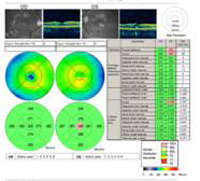 |
 |
Voorgeschiedenis: Deze patiënt heeft een voorgeschiedenis en klinisch beeld die sterk wijzen op het vermoedelijke oculaire histoplasmose syndroom (POHS). Hoewel zijn dikke, gele maculaire laesie niet perfect klassiek is (zie Figuur 5 en Discussie hieronder), wijzen alle aanwijzingen erop dat zich een choroïdaal neovasculair membraan (CNVM) heeft ontwikkeld in deze linker macula op de plaats van een chorioretinaal litteken. We bespraken uitvoerig met de patiënt de mogelijkheden voor behandeling, waaronder klinische studies voor maculaire laser- of fotodynamische therapie (PDT) van de laesie. Bovendien werd de patiënt geïnformeerd over de eerste resultaten in de literatuur en persoonlijke ervaringen die wijzen op goede resultaten met het off-label gebruik van intravitreale bevacizumab (Avastin). De patiënt koos voor een intravitreale injectie, die zonder complicaties werd uitgevoerd. Hij werd vier weken na de injectie opnieuw gezien. Zijn gezichtsvermogen was toen verbeterd tot 20/20 en de retinale laesie was zowel klinisch als met OCT droog (afbeelding 4).
Discussie: Het Presumed Ocular Histoplasmosis Syndrome (POHS) is een klinische diagnose die wordt gesteld op basis van een constellatie van oculaire bevindingen die oorspronkelijk in 1960 werden beschreven. Het syndroom is een ontstekingsaandoening waarvan wordt aangenomen dat ze het gevolg is van een systemische infectie met de dimorfe schimmel Histoplasma capsulatum. Er zijn echter geen bevestigende studies die deze schimmel rechtstreeks bij de pathogenese van de ziekte betrekken. Epidemiologische gegevens wijzen er eerder op dat de prevalentie van POHS sterk toeneemt in gebieden waar de Histoplasma-organismen endemisch zijn. Van mensen die in de valleien van de Ohio- en Mississippi-rivier wonen, is bekend dat zij een positieve huidtest voor blootstelling aan H.capsulatum hebben van maar liefst 70%. Inderdaad reageert de overgrote meerderheid van de patiënten met POHS positief op deze huidtest. Echter, slechts ongeveer 4,4% van de patiënten met een positieve huidtest heeft bewijs van POHS. Daarom blijft het verband tussen H. capsulatum en POHS verondersteld.
Opgemerkt moet worden dat patiënten met POHS vaak jong en verder gezond zijn en dat de retinale laesies een aanzienlijk functioneel verlies van het gezichtsvermogen kunnen veroorzaken in deze populatie van werkende leeftijd.
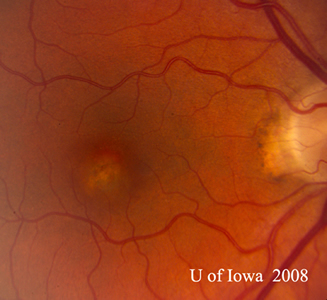
De diagnose van POHS wordt gesteld op basis van de identificatie van klassieke fundusbevindingen. Deze zijn de aanwezigheid van peripapillaire atrofie of pigmentatie, de aanwezigheid van karakteristieke “punched-out” chorioretinale atrofische laesies, en de afwezigheid van bovenliggende glasvocht betrokkenheid. De peripapillaire veranderingen worden verondersteld een gereconstrueerd choroïdaal neovasculair membraan (CNVM) te vertegenwoordigen, en de “punched-out” laesies worden verondersteld gebieden te vertegenwoordigen van hematogene uitzaaiing van H. capsulatum naar het netvlies. Opgemerkt moet worden dat veel van de perifere “doorprikte” chorioretinale littekens ook geassocieerd kunnen zijn met kleine CNVM’s die klinisch niet onder de aandacht worden gebracht en spontaan verdwijnen. Klassieke voorbeelden van deze laesies zijn te zien in figuur 5. Vaak, zoals in het hier gepresenteerde geval, zal POHS zich onder de aandacht van de oogarts brengen met een symptomatische CNVM die de macula of fovea betreft. In dit geval was de macula laesie enigszins ongewoon met een dikke gele substantie, terwijl het CNVM bij POHS vaak een grijs-groen net is dat ontstaat uit een chorioretinaal litteken (zie figuur 6) dat vroeg in het angiogram wordt gedefinieerd en laat uitlekt.
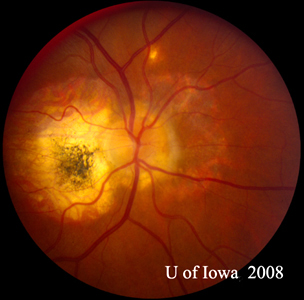
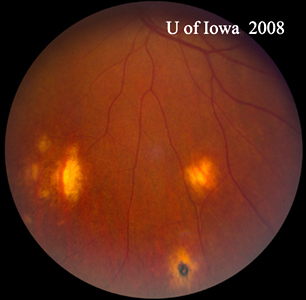
| A: POHS bij een patiënt met significante peripapillaire atrofie en pigmentverandering, die de verschijning toont van een geregenereerd peripapillair CNVM dat is gepostuleerd als de bron van deze laesies. | B: Perifere chorioretinale littekens bij een patiënt met POHS. |
 |
 |
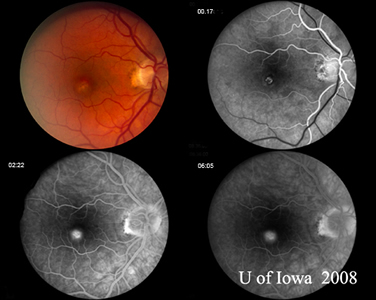
| A: Grijs-groen maculair CNVM bij een patiënt met POHS | B: Fluoresceïne-angiogram van de patiënt in figuur 6A toont klassiek lekkagepatroon geassocieerd met CNVM bij een patiënt met POHS. |
 |
 |
De pathogenese van de CNVM is onbekend; verschillende auteurs hebben echter gesuggereerd dat na hematogene verspreiding van de organismen naar het netvlies, gebieden van focale ontsteking ontstaan, die leiden tot een verstoring van het membraan van Bruch, en zo predisponeren voor de vorming van CNVM. Er wordt ook verondersteld dat POHS het gevolg is van een auto-immuun reactie, die wordt uitgelokt door de aanwezigheid van het infectieuze organisme. In elk geval worden de patiënten gewoonlijk asymptomatisch geïdentificeerd (minderheid) of komen zij onder de aandacht van een oogarts met klachten van verminderd gezichtsvermogen.
De behandeling van POHS is de laatste jaren geëvolueerd, en hoewel er geen directe therapie bestaat om het organisme aan te pakken, zijn verschillende modaliteiten geïdentificeerd als gunstig bij de behandeling van de begeleidende CNVM. In het verleden kon met laserfotocoagulatie een remming van goed gedefinieerde, klassieke extrafoveale, juxtafoveale en peripapillaire laesies bij POHS worden bereikt. Het resulterende centrale scotoma was echter soms onaanvaardbaar in plaats van nieuwere therapeutische opties. Fotodynamische therapie (PDT) met verteporfin werd eind 2001 door de FDA goedgekeurd voor de behandeling van CNVM die verband houden met POHS en er werd aangetoond dat deze therapie veilig en effectief was voor de behandeling van de ziekte. Toen eenmaal was aangetoond dat anti-VEGF-middelen doeltreffend waren voor de behandeling van CNVM die verband houden met AMD, werden in het midden van de jaren 2000 casusverslagen gepubliceerd waaruit bleek dat zij succesvol waren voor de behandeling van neovasculaire membranen bij patiënten met POHS. Na de publicatie van talrijke gevalsbeschrijvingen en retrospectieve beoordelingen die de doeltreffendheid van de behandeling met anti-VEGF middelen aantoonden, zijn zij de standaardbehandeling geworden, gebruikmakend van dezelfde principes als die voor de behandeling van AMD-gerelateerde CNVM.
Diagnose: Vermoedelijk Oculair Histoplasmose Syndroom (POHS) met CNVM
EPIDEMIOLOGIE
|
SIGNAAMS
|
SYMPTOMEN
|
TREATMENT
|
Differentiële diagnoses voor maculair chorioretinaal litteken met geassocieerd vocht:
- Toxoplasmose (zou glasvochtontsteking hebben)
- Myopic degeneratie
- Angiod streaks
- Age-Related Macular Degeneration (AMD)
- Central Serous Chorioretinopathy (CSCR)
- Punctate Inner Choroidopathy (PIC)
- Multifocal Choroiditis (MFC)
- Idiopathic CNVM
- Prasad AG, Van Gelder RN. Vermoedelijk oculair histoplasmose syndroom. Curr Opin Ophthalmol 2005;16(6):364-368. https://www.ncbi.nlm.nih.gov/pubmed/16264347
- Oliver A, Ciulla TA, Comer GM. New and classic insights into presumed ocular histoplasmosis syndrome and its treatment. Curr Opin Ophthalmol 2005;16(3):160-165. https://www.ncbi.nlm.nih.gov/pubmed/15870572
- Rosenfeld PJ, Saperstein DA, Bressler NM, Reaves TA, Sickenberg M, Rosa RH, Jr., Sternberg P, Jr., Aaberg TM, Sr., Verteporfin in Ocular Histoplasmosis Study G. Photodynamic therapy with verteporfin in ocular histoplasmosis: uncontrolled, open-label 2-year study. Ophthalmology 2004;111(9):1725-1733. https://www.ncbi.nlm.nih.gov/pubmed/15350329
- Adan A, Navarro M, Casaroli-Marano RP, Ortiz S, Molina JJ. Intravitreal bevacizumab as initial treatment for choroidal neovascularization associated with presumed ocular histoplasmosis syndrome. Graefes Arch Clin Exp Ophthalmol 2007;245(12):1873-1875. https://www.ncbi.nlm.nih.gov/pubmed/17786466
- Schadlu R, Blinder KJ, Shah GK, Holekamp NM, Thomas MA, Grand MG, Engelbrecht NE, Apte RS, Joseph DP, Prasad AG, Smith BT, Sheybani A. Intravitreale bevacizumab voor choroïdale neovascularisatie bij oculaire histoplasmose. Am J Ophthalmol 2008;145(5):875-878. https://www.ncbi.nlm.nih.gov/pubmed/18321466
- Weingeist TA, Watzke RC. Oculaire betrokkenheid door histoplasma capsulatum. Int Ophthalmol Clin 1983;23(2):33-47. https://www.ncbi.nlm.nih.gov/pubmed/6189798
- Cionni DA, Lewis SA, Petersen MR, Foster RE, Riemann CD, Sisk RA, Hutchins RK, Miller DM. Analyse van uitkomsten voor intravitreale bevacizumab bij de behandeling van choroïdale neovascularisatie secundair aan oculaire histoplasmose. Ophthalmology 2012;119(2):327-332. https://www.ncbi.nlm.nih.gov/pubmed/22133795
- Age-Related Macular Degeneration and Other Causes of Choroidal Neovascularization. Basis en klinische wetenschapscursus (BCSC) Sectie 12: Retina en glasvocht. San Francisco: American Academy of Ophthalmology; 2014-2015.
Suggested citation format
McConnell LK. Herziening van ; EyeRounds.org. July 5, 2017; Available from: http://www.EyeRounds.org/cases/83-Presumed-Ocular-Histoplasmosis-POHS.htm.