Histoplasmose Ocular Presumida (POHS):
Histoplasmose Ocular Presumida (POHS):
Histoplasmose Ocular Presumida (POHS):
Histoplasmose Ocular Presumida (POHS) EyeRounds.org – Ophthalmology – The University of Iowa Cohen, MD, PhD e Jordan M. Graff, MD
Histoplasmose Ocular Presumida (POHS):
Histoplasmose Ocular Presumida (POHS) EyeRounds.org – Ophthalmology – The University of Iowa Cohen, MD, PhD e Jordan M. Graff, MD
Março 9, 2008
Updated by Lindsay K. McConnell, MD
Maio 8, 2017
>
Queixa do Chefe: Visão central desfocada no olho esquerdo.
História da Doença Presente: Um homem branco de 30 anos de idade notou distorção visual central e perda de visão no olho esquerdo (OS) nas últimas semanas. Seu optometrista local encaminhou-o ao Departamento de Oftalmologia e Ciências Visuais da Universidade de Iowa para uma avaliação mais aprofundada.
História Ocular passada: Nenhum.
História Médica: O paciente não relatou doenças sistémicas ou doenças anteriores.
Medicamentos: Nenhum.
História Familiar: Nenhuma doença oftalmológica familiar e não-contributiva.
História Social: Casado, vive com a sua esposa. Ele trabalha como programador de computadores. O paciente viveu no Vale do Rio Mississippi durante toda a sua vida.
Exame circular:
- Acuidade Visual, sem correcção: Olho direito (OD)–20/20; OS–20/40
- Motilidade: Completo, ambos os olhos (OU)
- Pressão intra-ocular: OD — 15 mmHg; OS — 16 mmHg
- Pupilas: Igualmente reactivo à luz. Sem defeito pupilar relativo aferente (RAPD)
- Campos visuais de confronto (CVF): Completo, OU
- Externo e exame do segmento anterior: Normal, OU
- Exame do fundo dilatado (DFE):
- OD: Vítreo claro e nervo óptico saudável, sem palidez ou edema. Há atrofia peripapilar e pigmentação escura. Mácula e vasos normais. Na periferia há algumas cicatrizes de corioretina “perfuradas”.
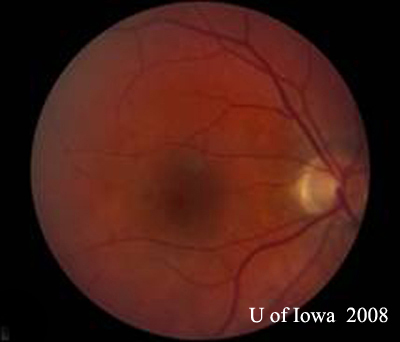
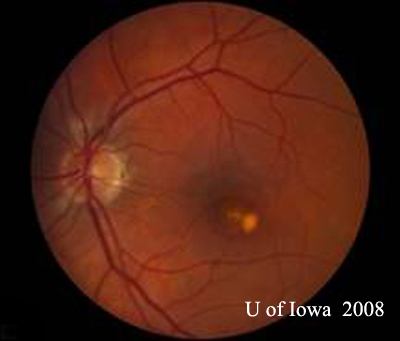
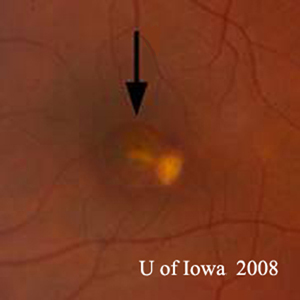
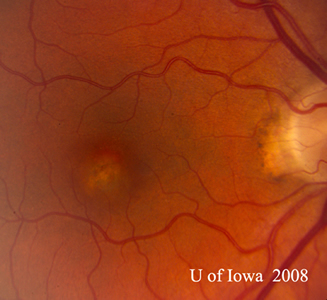
- OS: Vítreo claro sem absolutamente nenhuma célula ou sinais de inflamação. A cabeça do nervo óptico é saudável, sem palidez ou edema. Há atrofia peripapilar e aumento da pigmentação. Dentro da mácula, há uma lesão subretiniana elevada e amarelada (ver Figuras 1 e 2).
| A: Foto de fundo de 30 graus, DO. Observe as alterações atróficas peripapilares. | B: foto de fundo de 30 graus, SO. Similary peripapillary atrophic and pigment changes are evident. Notar o “histospot” corioretinário dentro da mácula e a ausência de qualquer inflamação vítrea. |
 |
 |
|
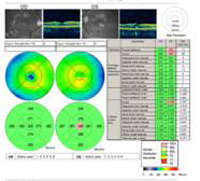
A: Tomografia de Coerência Óptica (TCO) de ambos os olhos mostra um aumento na espessura macular central (CMT) OS (295µm) comparado com OD (205µm). A). |
B: Note a presença de fluido subretinal e distorção da depressão foveal, OS. |
 |
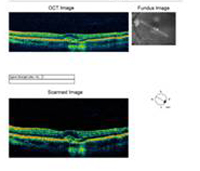 |
Curso: Este paciente tem uma história e uma aparência clínica fortemente sugestiva da presumível síndrome de histoplasmose ocular (POHS). Embora sua lesão macular espessa e amarela não seja perfeitamente clássica (ver Figura 5 e Discussão abaixo), todas as indicações sugerem que uma membrana neovascular coróide (MVCN) se desenvolveu nesta mácula esquerda no local de uma cicatriz corioretal. Discutimos longamente com os pacientes as opções de tratamento, incluindo estudos clínicos estabelecidos para laser macular ou terapia fotodinâmica (TDP) para a lesão. Além disso, o paciente foi informado sobre resultados iniciais na literatura e experiência pessoal sugerindo bons resultados com o uso off-label de bevacizumab intravitreal (Avastin). O paciente escolheu a injeção intravitreal, que foi realizada sem complicação. Ele foi visto novamente às quatro semanas após a injeção, quando sua visão havia melhorado para 20/20 e a lesão da retina estava seca tanto clinicamente como por TOC (Figura 4).
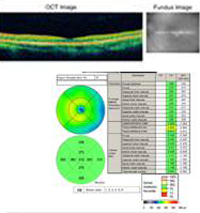
Discussão: A Síndrome de Histoplasmose Ocular Presumida (POHS) é um diagnóstico clínico feito com base em uma constelação de achados oculares que foram originalmente descritos em 1960. A síndrome é um distúrbio inflamatório que tem sido postulado como resultado de infecção sistêmica com os fungos dimórficos Histoplasma capsulatum. Não houve, no entanto, estudos confirmatórios que implicassem diretamente este fungo na patogênese da doença. Pelo contrário, os dados epidemiológicos sugerem que a prevalência de POHS está muito aumentada em áreas endêmicas para os organismos Histoplasma. Classicamente, as pessoas que vivem nos vales dos rios Ohio e Mississippi são conhecidas por terem uma taxa de 70% de teste cutâneo positivo para exposição ao H.capsulatum. De facto, a grande maioria dos pacientes com POHS reagem positivamente a este teste cutâneo. Contudo, apenas cerca de 4,4% dos pacientes com um teste cutâneo positivo têm evidência de POHS. Portanto, a relação entre o H. capsulatum e o POHS permanece presumida.
De notar que os pacientes com POHS são frequentemente jovens e saudáveis e as lesões da retina podem produzir perda visual funcional significativa nesta população em idade de trabalho.
O diagnóstico de POHS é feito com base na identificação dos achados fundus clássicos. Estes são a presença de atrofia ou pigmentação peripapilar, a presença de lesões atróficas corioretíficas “puncionadas” características e a ausência de envolvimento vítreo sobrejacente. Pensa-se que as alterações peripapilares representam uma membrana neovascular coróide regressiva (CNVM) e que as lesões “punchd-out” representam áreas de semeadura hematogénica de H. capsulatum para a retina. Deve-se notar que muitas das cicatrizes periféricas “punchd-out” corioretinosas podem muito bem estar associadas a pequenas CNVMs também que não são chamadas à atenção clinicamente e regridem espontaneamente. Exemplos clássicos destas lesões podem ser vistos na Figura 5. Muitas vezes, como no caso aqui apresentado, o POHS irá apresentar à atenção do oftalmologista uma MCNV sintomática envolvendo a mácula ou fóvea. Neste caso, a lesão macular foi algo incomum com uma substância amarela espessa para ela, enquanto a CNVM no POHS é frequentemente uma rede de rendilhado cinza-esverdeado decorrente de uma cicatriz corioretina (ver Figura 6) que é definida precocemente no angiograma e vaza tardiamente.
| A: POHS em um paciente com atrofia peripapilar significativa e mudança de pigmento, demonstrando o aparecimento de uma CNVM peripapilar regressiva que tem sido postulada como a fonte dessas lesões. | B: Cicatrizes periféricas de corioretina em um paciente com POHS. |
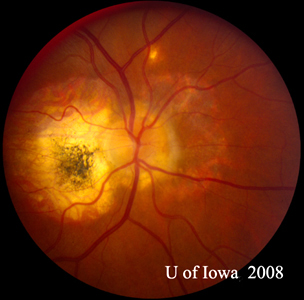 |
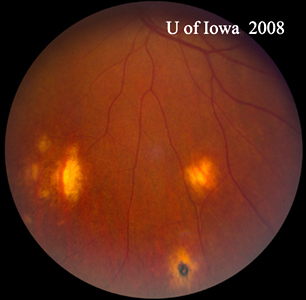 |
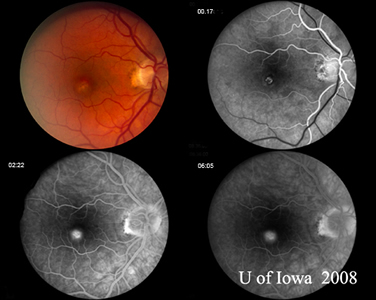
| A: CNVM macular cinza-verde em paciente com POHS | B: Angiograma de fluoresceína do paciente na Figura 6A demonstra o padrão clássico de fuga associado à CNVM em paciente com POHS. |
 |
 |
A patogênese da CMVMN é desconhecida; entretanto, vários autores sugeriram que após a disseminação hematogênica dos organismos na retina, áreas de inflamação focal ocorrem, levando a uma ruptura na membrana de Bruch, predispondo assim à formação da CMVMN. A POHS também foi postulada como resultado do gatilho auto-imune, que é desvirtuado pela presença do organismo infeccioso. Em qualquer caso, os pacientes são normalmente identificados enquanto assintomáticos (minoritários) ou chegam ao conhecimento de um oftalmologista com queixas de diminuição da visão.
O tratamento do POHS tem evoluído ao longo dos últimos anos, e embora não exista uma terapia directa para o organismo, várias modalidades têm sido identificadas como benéficas no tratamento da CNVM de acompanhamento. Historicamente, a fotocoagulação a laser resultou na inibição de lesões bem definidas, clássicas extrafoveais, justafoveais e peripapilares em POHS. No entanto, o escotoma central resultante era, por vezes, inaceitável em vez de novas opções terapêuticas. A terapia fotodinâmica (TDP) com verteporfina foi aprovada pelo FDA para o tratamento da CNVM relacionada ao POHS no final de 2001 e demonstrou ser segura e eficaz para o tratamento da doença. Uma vez provada a eficácia dos agentes anti-VEGF no tratamento da CNVM relacionada à DMRI, foram publicados relatos de casos em meados dos anos 2000 mostrando seu sucesso no tratamento das membranas neovasculares em pacientes com POHS. Após a publicação de inúmeros relatos de casos e revisões retrospectivas mostrando a eficácia do tratamento com agentes anti-VEGF, eles se tornaram o padrão de tratamento utilizando os mesmos princípios para o tratamento da DCVM relacionada à DMRI.
Diagnóstico: Síndrome de Histoplasmose Ocular Presumida (POHS) com CNVM
EPIDEMIOLOGIA
|
SIGNS
|
SYMPTOMS
|
Tratamento
|
Diagnóstico diferencial para cicatriz corioretal macular com líquido associado:
- Toxoplasmose (teria inflamação vítrea)
- Degeneração miópica
- Estrias angiodas
- Idade…Degeneração Macular Relacionada (DMA)
- Cioretinopatia Serosa Central (CSCR)
- Coroidopatia Interna Punctal (PIC)
- Coroidite Multifocal (MFC)
- Coroidopatia Diopática CNVM
- Prasad AG, Van Gelder RN. Síndrome de histoplasmose ocular presumida. Curr Opinião Ophthalmol 2005;16(6):364-368. https://www.ncbi.nlm.nih.gov/pubmed/16264347
- Oliver A, Ciulla TA, Comer GM. Novos e clássicos insights sobre a síndrome da histoplasmose ocular presumida e seu tratamento. Curr Opinião Ophthalmol 2005;16(3):160-165. https://www.ncbi.nlm.nih.gov/pubmed/15870572
- Rosenfeld PJ, Saperstein DA, Bressler NM, Reaves TA, Sickenberg M, Rosa RH, Jr., Sternberg P, Jr., Aaberg TM, Sr., Aaberg TM, Jr., Verteporfin in Ocular Histoplasmose Estudo G. Terapia fotodinâmica com verteporfina em histoplasmose ocular: estudo de 2 anos sem controle, aberto. Ophthalmology 2004;111(9):1725-1733. https://www.ncbi.nlm.nih.gov/pubmed/15350329
- Adan A, Navarro M, Casaroli-Marano RP, Ortiz S, Molina JJ. Intravitreal bevacizumab como tratamento inicial para a neovascularização coróide associada à síndrome de histoplasmose ocular presumida. Graefes Arch Clin Exp Ophthalmol 2007;245(12):1873-1875. https://www.ncbi.nlm.nih.gov/pubmed/17786466
- Schadlu R, Blinder KJ, Shah GK, Holekamp NM, Thomas MA, Grand MG, Engelbrecht NE, Apte RS, Joseph DP, Prasad AG, Smith BT, Sheybani A. Intravitreal bevacizumab para neovascularização coróide em histoplasmose ocular. Am J Ophthalmol 2008;145(5):875-878. https://www.ncbi.nlm.nih.gov/pubmed/18321466
- Weingeist TA, Watzke RC. Envolvimento ocular por histoplasma capsulatum. Int Ophthalmol Clin 1983;23(2):33-47. https://www.ncbi.nlm.nih.gov/pubmed/6189798
- Cionni DA, Lewis SA, Petersen MR, Foster RE, Riemann CD, Sisk RA, Hutchins RK, Miller DM. Análise dos resultados para bevacizumab intravitreal no tratamento da neovascularização coróide secundária à histoplasmose ocular. Ophthalmology 2012;119(2):327-332. https://www.ncbi.nlm.nih.gov/pubmed/22133795
- Degeneração Macular Relacionada à Idade e Outras Causas da Neovascularização Coroidal. Curso de ciências básicas e clínicas (BCSC) Secção 12: Retina e Vítreo. São Francisco: Academia Americana de Oftalmologia; 2014-2015.
Formato de citação falsificada
McConnell LK. Revisão de ; EyeRounds.org. 5 de julho de 2017; Disponível em: http://www.EyeRounds.org/cases/83-Presumed-Ocular-Histoplasmosis-POHS.htm.