30-jähriger Mann mit verschwommenem zentralen Sehen
Alex W. Cohen, MD, PhD und Jordan M. Graff, MD
März 9, 2008
Aktualisiert von Lindsay K. McConnell, MD
Mai 8, 2017
Hauptbeschwerde: Verschwommenes zentrales Sehen auf dem linken Auge.
Geschichte der aktuellen Erkrankung: Ein 30-jähriger weißer Mann bemerkte in den letzten Wochen eine zentrale Sehstörung und einen Sehverlust auf dem linken Auge (OS). Sein örtlicher Augenarzt überwies ihn zur weiteren Abklärung an das Department of Ophthalmology and Visual Sciences der University of Iowa.
Augenärztliche Vorgeschichte: Keine.
Medizinische Vorgeschichte: Der Patient gab keine früheren systemischen Krankheiten oder Erkrankungen an.
Medikamente: Keine.
Familiäre Vorgeschichte: Keine familiären Augenkrankheiten und ansonsten unauffällig.
Soziale Vorgeschichte: Verheiratet, lebt mit seiner Frau zusammen. Er arbeitet als Computerprogrammierer. Der Patient hat sein ganzes Leben lang im Mississippi River Valley gelebt.
Augenuntersuchung:
- Sehschärfe, ohne Korrektur: Rechtes Auge (OD)–20/20; OS–20/40
- Motilität: Voll, beide Augen (OU)
- Intraokularer Druck: OD — 15 mmHg; OS — 16 mmHg
- Pupillen: Gleiche Lichtreaktivität. Kein relativer afferenter Pupillendefekt (RAPD)
- Konfrontationsgesichtsfelder (CVF): Vollständig, OU
- Untersuchung des äußeren und vorderen Augenabschnitts: Normal, OU
- Dilatierte Fundusuntersuchung (DFE):
- OD: Klarer Glaskörper und gesunder Sehnerv ohne Blässe oder Ödeme. Es besteht eine peripapilläre Atrophie und dunkle Pigmentierung. Normale Makula und Gefäße. In der Peripherie befinden sich einige „ausgestanzte“ chorioretinale Narben.
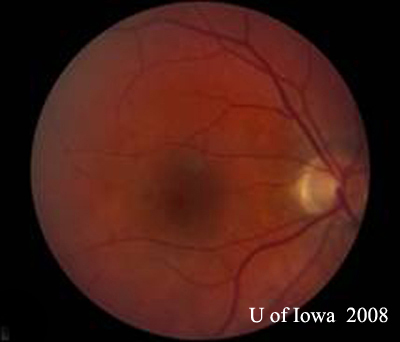
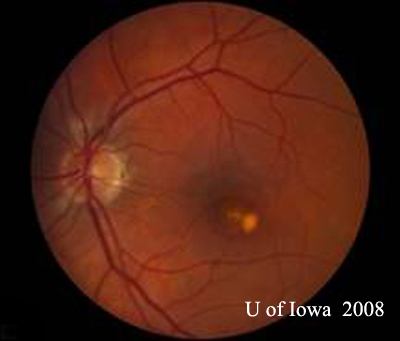
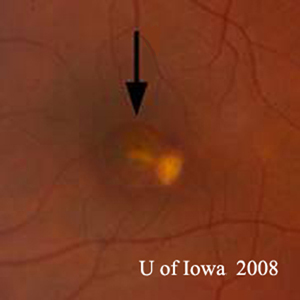
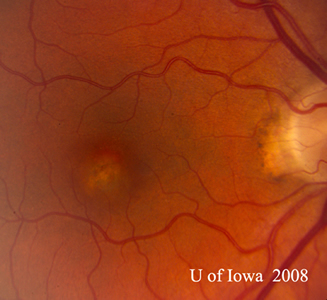
- OS: Klarer Glaskörper ohne Zellen oder Anzeichen einer Entzündung. Der Sehnervenkopf ist gesund, ohne Blässe oder Ödeme. Es besteht eine peripapilläre Atrophie und eine erhöhte Pigmentierung. In der Makula befindet sich eine erhabene gelbliche subretinale Läsion (siehe Abbildungen 1 und 2).
| A: 30-Grad-Fundusaufnahme, OD. Man beachte die peripapillären atrophischen Veränderungen. | B: 30-Grad-Fundusfoto, OS. Auch hier sind peripapilläre atrophische und Pigmentveränderungen erkennbar. Man beachte den chorioretinalen „Histospot“ innerhalb der Makula und das Fehlen jeglicher Glaskörperentzündung. |
 |
 |
|
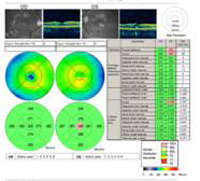
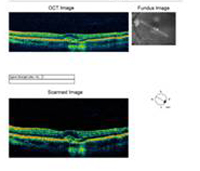
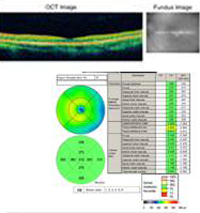
A: Optische Kohärenztomographie (OCT) Scans beider Augen zeigen eine Zunahme der zentralen Makuladicke (CMT) OS (295µm) im Vergleich zu OD (205µm). A). |
B: Man beachte das Vorhandensein von subretinaler Flüssigkeit und die Verzerrung der fovealen Depression, OS. |
 |
 |
Verlauf: Die Anamnese und das klinische Erscheinungsbild dieses Patienten deuten stark auf das mutmaßliche okuläre Histoplasmose-Syndrom (POHS) hin. Seine dicke, gelbe Makulaläsion ist zwar nicht ganz klassisch (siehe Abbildung 5 und Diskussion unten), aber alles deutet darauf hin, dass sich in dieser linken Makula an der Stelle einer chorioretinalen Narbe eine choroidale neovaskuläre Membran (CNVM) entwickelt hat. Wir besprachen mit der Patientin ausführlich die Behandlungsmöglichkeiten, einschließlich etablierter klinischer Studien zur Makulalaser- oder photodynamischen Therapie (PDT) der Läsion. Darüber hinaus wurde die Patientin über erste Ergebnisse in der Literatur und persönliche Erfahrungen informiert, die auf gute Ergebnisse mit dem Off-Label-Einsatz von intravitrealem Bevacizumab (Avastin) hinweisen. Der Patient entschied sich für die intravitreale Injektion, die ohne Komplikationen durchgeführt wurde. Vier Wochen nach der Injektion wurde er erneut untersucht. Zu diesem Zeitpunkt hatte sich sein Sehvermögen auf 20/20 verbessert, und die Netzhautläsion war sowohl klinisch als auch mittels OCT trocken (Abbildung 4).
Diskussion: Das Presumed Ocular Histoplasmosis Syndrome (POHS) ist eine klinische Diagnose, die auf einer Konstellation von Augenbefunden beruht, die ursprünglich 1960 beschrieben wurden. Bei dem Syndrom handelt es sich um eine entzündliche Erkrankung, die auf eine systemische Infektion mit dem dimorphen Pilz Histoplasma capsulatum zurückzuführen ist. Es gibt jedoch keine bestätigenden Studien, die diesen Pilz direkt mit der Pathogenese der Krankheit in Verbindung bringen. Vielmehr deuten epidemiologische Daten darauf hin, dass die Prävalenz von POHS in Gebieten, in denen der Histoplasma-Organismus endemisch ist, stark erhöht ist. Es ist bekannt, dass bei Menschen, die in den Tälern des Ohio und des Mississippi leben, bis zu 70 % der Hauttests positiv auf H. capsulatum reagieren. In der Tat reagiert die große Mehrheit der Patienten mit POHS positiv auf diesen Hauttest. Allerdings weisen nur etwa 4,4 % der Patienten mit positivem Hauttest eine POHS auf. Daher wird der Zusammenhang zwischen H. capsulatum und POHS weiterhin vermutet.
Anzumerken ist, dass Patienten mit POHS oft jung und ansonsten gesund sind und dass die Netzhautläsionen in dieser Bevölkerungsgruppe im erwerbsfähigen Alter zu einem erheblichen funktionellen Sehverlust führen können.
Die Diagnose von POHS wird auf der Grundlage klassischer Fundusbefunde gestellt. Diese sind das Vorhandensein einer peripapillären Atrophie oder Pigmentierung, das Vorhandensein charakteristischer „ausgestanzter“ chorioretinaler atrophischer Läsionen und das Fehlen einer darüber liegenden Glaskörperbeteiligung. Bei den peripapillären Veränderungen geht man davon aus, dass es sich um eine regressierte choroidale neovaskuläre Membran (CNVM) handelt, und bei den „ausgestanzten“ Läsionen denkt man, dass es sich um Bereiche handelt, in denen H. capsulatum hämatogen in die Netzhaut eingedrungen ist. Es ist zu beachten, dass viele der peripheren „ausgestanzten“ chorioretinalen Narben auch mit kleinen CNVMs verbunden sein können, die klinisch nicht auffallen und sich spontan zurückbilden. Klassische Beispiele für diese Läsionen sind in Abbildung 5 zu sehen. Oftmals, wie in dem hier vorgestellten Fall, wird der Augenarzt auf POHS mit einer symptomatischen CNVM aufmerksam, die die Makula oder Fovea betrifft. In diesem Fall war die Makulaläsion etwas ungewöhnlich mit einer dicken gelben Substanz, wohingegen die CNVM bei POHS oft ein grau-grünes, spitzenartiges Netz ist, das aus einer chorioretinalen Narbe entsteht (siehe Abbildung 6), die früh im Angiogramm definiert wird und erst spät austritt.
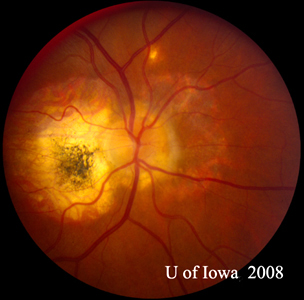
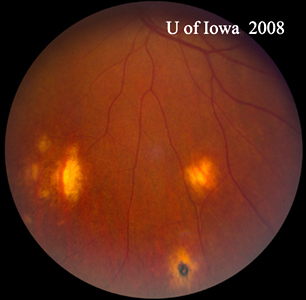
| A: POHS bei einem Patienten mit signifikanter peripapillärer Atrophie und Pigmentveränderung, der das Erscheinungsbild einer regressierten peripapillären CNVM zeigt, die als Ursache dieser Läsionen postuliert wurde. | B: Periphere chorioretinale Narben bei einem Patienten mit POHS. |
 |
 |
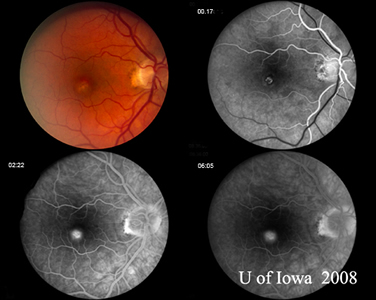
| A: Graugrüne makuläre CNVM bei einem Patienten mit POHS | B: Das Fluorescein-Angiogramm des Patienten in Abbildung 6A zeigt das klassische Leckagemuster, das mit CNVM bei Patienten mit POHS assoziiert ist. |
 |
 |
Die Pathogenese der CNVM ist nicht bekannt; mehrere Autoren haben jedoch vorgeschlagen, dass nach der hämatogenen Ausbreitung der Organismen auf die Netzhaut Bereiche fokaler Entzündungen auftreten, die zu einer Störung der Bruch’schen Membran führen und somit die Bildung einer CNVM begünstigen. Es wurde auch postuliert, dass die POHS durch eine Autoimmunreaktion ausgelöst wird, die durch das Vorhandensein des infektiösen Organismus ausgelöst wird. In jedem Fall werden die Patienten in der Regel entweder in einem asymptomatischen Zustand identifiziert (Minderheit) oder sie wenden sich an einen Augenarzt mit Beschwerden über eine Sehverschlechterung.
Die Behandlung von POHS hat sich in den letzten Jahren weiterentwickelt, und obwohl es keine direkte Therapie zur Bekämpfung des Organismus gibt, haben sich mehrere Modalitäten als nützlich für die Behandlung der begleitenden CNVM erwiesen. In der Vergangenheit konnte mit der Laserphotokoagulation eine Hemmung gut definierter, klassischer extrafovealer, juxtafovealer und peripapillärer Läsionen bei POHS erreicht werden. Das daraus resultierende zentrale Skotom war jedoch manchmal inakzeptabel und wurde durch neuere therapeutische Optionen ersetzt. Die photodynamische Therapie (PDT) mit Verteporfin wurde Ende 2001 von der FDA für die Behandlung von CNVM im Zusammenhang mit POHS zugelassen und erwies sich als sicher und wirksam bei der Behandlung der Krankheit. Nachdem sich Anti-VEGF-Mittel bei der Behandlung von CNVM im Zusammenhang mit AMD als wirksam erwiesen hatten, wurden Mitte der 2000er Jahre Fallberichte veröffentlicht, die ihren Erfolg bei der Behandlung von neovaskulären Membranen bei Patienten mit POHS belegen. Nach der Veröffentlichung zahlreicher Fallberichte und retrospektiver Übersichten, die die Wirksamkeit der Behandlung mit Anti-VEGF-Mitteln zeigten, wurden diese zum Standard der Behandlung, wobei die gleichen Prinzipien wie bei der Behandlung der AMD-bedingten CNVM angewandt wurden.
Diagnose: Vermutetes okuläres Histoplasmosesyndrom (POHS) mit CNVM
EPIDEMIOLOGIE
|
SIGNALE
|
SYMPTOME
|
TREATMENT
|
Differenzialdiagnosen für makuläre chorioretinale Narbe mit assoziierter Flüssigkeit:
- Toxoplasmose (hätte Glaskörperentzündung)
- Myopische Degeneration
- Angiod-Streifen
- Age-Altersbedingte Makuladegeneration (AMD)
- Zentrale seröse Chorioretinopathie (CSCR)
- Punktierte innere Choroidopathie (PIC)
- Multifokale Choroiditis (MFC)
- Idiopathische CNVM
- Prasad AG, Van Gelder RN. Vermutetes okuläres Histoplasmose-Syndrom. Curr Opin Ophthalmol 2005;16(6):364-368. https://www.ncbi.nlm.nih.gov/pubmed/16264347
- Oliver A, Ciulla TA, Comer GM. Neue und klassische Erkenntnisse über das mutmaßliche okuläre Histoplasmose-Syndrom und seine Behandlung. Curr Opin Ophthalmol 2005;16(3):160-165. https://www.ncbi.nlm.nih.gov/pubmed/15870572
- Rosenfeld PJ, Saperstein DA, Bressler NM, Reaves TA, Sickenberg M, Rosa RH, Jr., Sternberg P, Jr., Aaberg TM, Sr., Aaberg TM, Jr., Verteporfin in Ocular Histoplasmosis Study G. Photodynamic therapy with verteporfin in ocular histoplasmosis: uncontrolled, open-label 2-year study. Ophthalmology 2004;111(9):1725-1733. https://www.ncbi.nlm.nih.gov/pubmed/15350329
- Adan A, Navarro M, Casaroli-Marano RP, Ortiz S, Molina JJ. Intravitreales Bevacizumab als Erstbehandlung von choroidalen Neovaskularisationen in Verbindung mit einem vermuteten okulären Histoplasmose-Syndrom. Graefes Arch Clin Exp Ophthalmol 2007;245(12):1873-1875. https://www.ncbi.nlm.nih.gov/pubmed/17786466
- Schadlu R, Blinder KJ, Shah GK, Holekamp NM, Thomas MA, Grand MG, Engelbrecht NE, Apte RS, Joseph DP, Prasad AG, Smith BT, Sheybani A. Intravitreales Bevacizumab für choroidale Neovaskularisation bei okulärer Histoplasmose. Am J Ophthalmol 2008;145(5):875-878. https://www.ncbi.nlm.nih.gov/pubmed/18321466
- Weingeist TA, Watzke RC. Ocular involvement by histoplasma capsulatum. Int Ophthalmol Clin 1983;23(2):33-47. https://www.ncbi.nlm.nih.gov/pubmed/6189798
- Cionni DA, Lewis SA, Petersen MR, Foster RE, Riemann CD, Sisk RA, Hutchins RK, Miller DM. Analyse der Ergebnisse für intravitreale Bevacizumab in der Behandlung der choroidalen Neovaskularisation sekundär zu okulärer Histoplasmose. Ophthalmology 2012;119(2):327-332. https://www.ncbi.nlm.nih.gov/pubmed/22133795
- Age-Related Macular Degeneration and Other Causes of Choroidal Neovascularization. Basic and clinical science course (BCSC) Section 12: Retina and Vitreous. San Francisco: American Academy of Ophthalmology; 2014-2015.
Vorgeschlagenes Zitierformat
McConnell LK. Revision of ; EyeRounds.org. July 5, 2017; Available from: http://www.EyeRounds.org/cases/83-Presumed-Ocular-Histoplasmosis-POHS.htm.