Los piroxenos son el grupo más significativo y abundante de silicatos ferromagnesianos formadores de rocas. Se encuentran en casi todas las variedades de rocas ígneas y aparecen en rocas de composición muy diferente formadas en condiciones de metamorfismo regional y de contacto. El nombre de piroxeno deriva del griego pyro, que significa «fuego», y xenos, que significa «extraño», y fue dado por Haüy a los cristales verdosos que se encuentran en muchas lavas y que él consideraba que habían sido incluidos en ellas accidentalmente.
La composición química de los minerales del grupo del piroxeno puede expresarse mediante la fórmula general:
XYZ2O6
en la que X = Na+, Ca2+, Mn2+, Fe2+, Mg2+, Li+; Y = Mn2+, Fe2+, Mg2+, Fe3+, Al3+, Cr3+, Ti4+; y Z= Si4+, Al3+. La gama de posibles sustituciones químicas en el piroxeno está limitada por los tamaños de los sitios disponibles en la estructura y la carga de los cationes sustituyentes. Los sitios de los cationes X son en general más grandes que los de los cationes Y. Se produce una amplia sustitución atómica entre las composiciones ideales de los miembros finales. La mayoría de los piroxenos sólo tienen una sustitución limitada de aluminio por silicio en el sitio Z (tetraédrico). Cuando un ion sustituto difiere en carga, la neutralidad eléctrica se mantiene mediante sustituciones acopladas. Por ejemplo, el par formado por Na+ y Al3+ sustituye a 2Mg2+.
Los piroxenos más comunes pueden representarse como parte del sistema químico CaSiO3 (wollastonita, un piroxenoide), MgSiO3 (enstatita) y FeSiO3 (ferrosilita). (Fig.1). Dado que no existen piroxenos verdaderos con contenidos de calcio superiores a los de la unión diópsido-hedenbergita, la parte de este sistema por debajo de esta unión se conoce como el cuadrilátero de piroxeno.
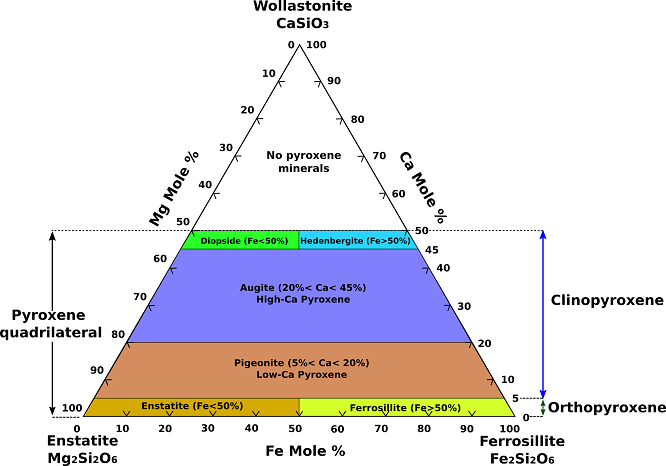
Fig.1Diagrama de composición ternaria de los piroxenos.
La sustitución completa existe entre la enstatita (Mg2Si2O6) y la ferrosilita (Fe2Si2O6), y la solución sólida completa de hierro por magnesio existe entre el diópsido (CaMgSi2O6) y la hedenbergita (CaFeSi2O6). La augita, la augita subcálcica y la pigeonita se encuentran en el interior del cuadrilátero de piroxeno. Compositivamente, la augita está relacionada con los miembros de la serie diópsido-hedenbergita con una sustitución limitada de Na+ por Ca2+, Al3+ por Mg2+ y Fe2+, y Al3+ por Si4+ en el sitio Z (tetraédrico). Las augitas con aluminio o sodio sustanciales no pueden representarse estrictamente en el plano cuadrilátero. La pigeonita monoclínica abarca un campo de solución sólida de magnesio-hierro con un contenido de calcio ligeramente superior al de la serie ortorrómbica de enstatita-ortoferrosilita.
Las sustituciones acopladas que implican Na+, Li+ o Al3+ por Mg2+ en la estructura de enstatita dan lugar a piroxenos que se sitúan fuera del campo composicional cuadrilátero. La sustitución acoplada de Na+ y Al3+ por 2Mg2+ en la enstatita produce el piroxeno jadeíta. La sustitución acoplada de Na+ y Fe3+ por 2Mg2+ produce el piroxeno aegirina (acmita). La sustitución de Li+ y Al3+ por 2Mg2+ produce el espodumeno. La sustitución de Al3+ por Mg2+ y Al3+ por Si4+ produce el componente ideal de la tschermakita MgAlSiAlO6. Otros piroxenos menos comunes con composiciones fuera del cuadrilátero del piroxeno son la johannsenita y la kosmochlor (ureyita). La johannsenita implica la sustitución del manganeso por el hierro en la hedenbergita. La kosmochlor tiene cromo (Cr) en lugar de hierro o aluminio en un piroxeno sódico.
A altas temperaturas, los piroxenos tienen campos de solución sólida más extensos que a bajas. En consecuencia, a medida que las temperaturas disminuyen, el piroxeno ajusta su composición en el estado sólido mediante la exsolución de una fase separada en forma de láminas dentro del grano de piroxeno anfitrión. Las láminas se exsuelen a lo largo de direcciones cristalográficas específicas, produciendo intercrecimientos orientados con textura paralela y en espiga. Hay cinco combinaciones principales de pares de exsolución: (1) augita con láminas de enstatita, (2) augita con láminas de pigeonita, (3) augita con láminas de pigeonita y enstatita, (4) pigeonita con láminas de augita, y (5) enstatita con láminas de augita.
Los piroxenos difieren compositivamente de los anfíboles en dos aspectos principales. Los piroxenos no contienen agua esencial en forma de hidroxilos en su estructura, mientras que los anfíboles se consideran silicatos hidrosos. La segunda diferencia química clave entre los dos es la presencia del sitio A en los anfíboles, que contiene los elementos alcalinos grandes, típicamente sodio y a veces potasio; los piroxenos no tienen un sitio equivalente que pueda acomodar el potasio.
Estructura
El grupo de los piroxenos incluye minerales que se forman en los sistemas cristalinos ortorrómbico y monoclínico. Los piroxenos ortorrómbicos se denominan ortopiroxenos y los monoclínicos, clinopiroxenos. La característica esencial de todas las estructuras de piroxeno es la unión de los tetraedros de silicio-oxígeno (SiO4) compartiendo dos de las cuatro esquinas para formar cadenas continuas. Las cadenas, que se extienden indefinidamente en paralelo al eje cristalográfico c, tienen la composición de (Si2O6) (Fig.2). Una distancia de repetición de aproximadamente 5,3 Å a lo largo de la cadena define el eje c de la celda unitaria. Las cadenas de Si2O6 están unidas a una capa de bandas de cationes coordinados octaédricamente que también se extienden paralelas al eje c.
.png)
Fig.2: diagrama esquemático de la estructura del piroxeno de cadena simple. Donde dos tetraedros se tocan, comparten un ion oxígeno. De Wikipedia
Las bandas octaédricas consisten en octaedros M1 y M2 intercalados entre dos cadenas tetraédricas de orientación opuesta. Los sitios M1 están ocupados por cationes más pequeños como el magnesio, el hierro, el aluminio y el manganeso, que se coordinan con seis átomos de oxígeno para formar un octaedro regular. En los piroxenos monoclínicos, el sitio M2 es un gran poliedro irregular ocupado por los cationes más grandes de calcio y sodio que están en coordinación óctuple. En los piroxenos ortorrómbicos de bajo calcio, M2 contiene magnesio y hierro, y el poliedro adopta una forma octaédrica más regular. La franja del catión M1 está unida a los átomos de oxígeno de dos cadenas tetraédricas de orientación opuesta (Fig.3). Juntos, forman una banda tetraédrica-octaédrica-tetraédrica (t-o-t). En la Fig. 3 se muestra una proyección esquemática de la estructura del piroxeno perpendicular al eje c y la relación de la escisión del piroxeno con las bandas t-o-t o haces I.
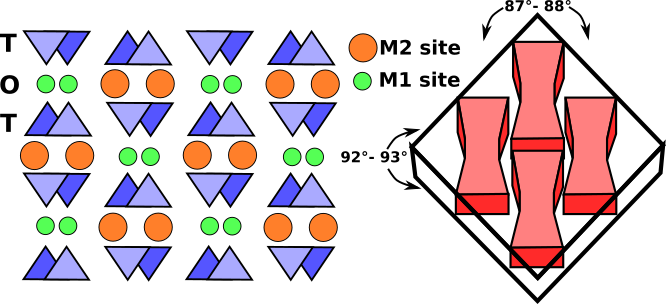
Fig.3: Proyección esquemática de la estructura monoclínica del piroxeno perpendicular al eje c. Las bandas T-O-T, denominadas vigas I, tienen enlaces muy fuertes que resisten la ruptura y producen la típica escisión de cerca de 90° de los piroxenos (líneas discontinuas).
En secciones delgadas, los piroxenos monoclínicos se distinguen por dos direcciones de escisión a aproximadamente 87° y 93°, secciones transversales basales de ocho lados y color marrón claro o verde. Los piroxenos ortorrómbicos difieren de los monoclínicos en que tienen una extinción paralela.
Bibliografía
– Cox et al. (1979): The Interpretation of Igneous Rocks, George Allen and Unwin, London.
– Howie, R. A., Zussman, J., & Deer, W. (1992). An introduction to the rock-forming minerals (p. 696). Longman.
– Le Maitre, R. W., Streckeisen, A., Zanettin, B., Le Bas, M. J., Bonin, B., Bateman, P., & Lameyre, J. (2002). Igneous rocks. A classification and glossary of terms, 2. Cambridge University Press.
– Middlemost, E. A. (1986). Magmas and magmatic rocks: an introduction to igneous petrology.
– Shelley, D. (1993). Igneous and metamorphic rocks under the microscope: classification, textures, microstructures and mineral preferred-orientations.
– Vernon, R. H. & Clarke, G. L. (2008): Principles of Metamorphic Petrology. Cambridge University Press.