A piroxének a kőzetalkotó ferromagnéziás szilikátok legjelentősebb és leggyakoribb csoportja. Megtalálhatók a vulkáni kőzetek szinte minden fajtájában, és a regionális és kontakt metamorfózis körülményei között kialakult, igen eltérő összetételű kőzetekben fordulnak elő. A piroxén elnevezés a görög pyro, azaz “tűz” és xenos, azaz “idegen” szóból származik, és Haüy adta a sok lávában található zöldes színű kristályoknak, amelyeket szerinte véletlenül kerültek bele.
A piroxéncsoportba tartozó ásványok kémiai összetétele az általános képlettel fejezhető ki:
XYZ2O6
melyben X = Na+, Ca2+, Mn2+, Fe2+, Mg2+, Li+; Y = Mn2+, Fe2+, Mg2+, Fe3+, Al3+, Cr3+, Ti4+; és Z= Si4+, Al3+. A piroxénben lehetséges kémiai helyettesítések tartományát a szerkezetben rendelkezésre álló helyek mérete és a helyettesítő kationok töltése korlátozza. Az X-kation helyek általában nagyobbak, mint az Y-kation helyek. Az ideális végtag-összetételek között kiterjedt atomi szubsztitúció fordul elő. A legtöbb piroxénben a Z (tetraéderes) helyen a szilíciumot csak korlátozott mértékben helyettesíti alumínium. Ha a helyettesítő ionok töltése különbözik, az elektromos semlegességet a kapcsolt helyettesítések tartják fenn. Például a Na+-ból és Al3+-ból álló pár 2Mg2+ helyettesít.
A leggyakoribb piroxének a CaSiO3 (wollastonit, egy piroxenoid), MgSiO3 (enstatit) és FeSiO3 (ferroszilik) kémiai rendszer részeként ábrázolhatók. (1. ábra). Mivel a diopszid-hedenbergit csatlakozásnál nagyobb kalciumtartalmú valódi piroxének nem léteznek, ezért a rendszer ezen csatlakozás alatti részét piroxénnégyszögnek nevezik.
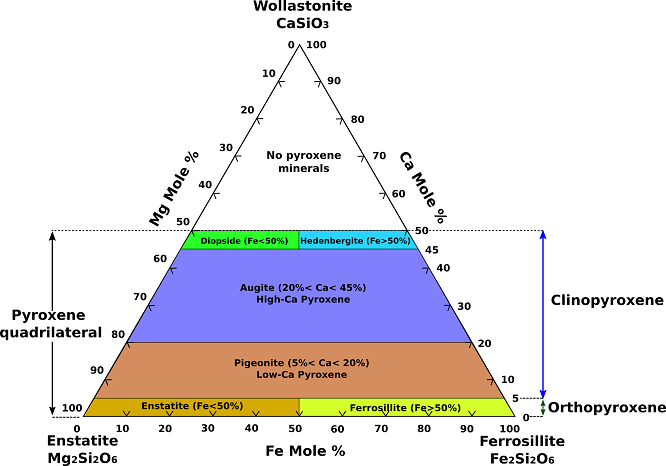
1. ábra.: A piroxének hármas összetételi diagramja.
Az ensztatit (Mg2Si2O6) és a ferroszilit (Fe2Si2O6) között teljes helyettesítés, a diopszid (CaMgSi2O6) és a hedenbergit (CaFeSi2O6) között pedig a vas teljes szilárd oldódása a magnéziumra. A piroxénnégyszög belsejében augit, szubkalcikus augit és galambit található. Összetételét tekintve az augit a diopszid-hedenbergit-sorozat tagjaival áll rokonságban, a Z (tetraéderes) helyen a Ca2+ korlátozott mértékben Na+-mal, az Mg2+ és Fe2+ Al3+-mal, valamint a Si4+ Al3+-mal helyettesítve. A jelentős alumíniumot vagy nátriumot tartalmazó augitok nem ábrázolhatók szigorúan a négyszögletes síkban. A monoklin pigeonit a magnézium-vas szilárd oldat mezőjét foglalja magába, valamivel magasabb kalciumtartalommal, mint az orthorhombikus enstatit-ortoferroszilit sorozat.
Az enstatit szerkezetben az Mg2+ helyett Na+, Li+ vagy Al3+ bevonásával történő helyettesítések olyan piroxéneket eredményeznek, amelyek kívül esnek a négyszögletes összetételi mezőn. Az enstatitban a Na+ és az Al3+ 2Mg2+ párosított helyettesítése a jadeit piroxént eredményezi. A Na+ és Fe3+ 2Mg2+ párosított helyettesítésével a piroxén aegirin (akmit) keletkezik. A 2Mg2+ Li+ és Al3+ helyettesítésével spodumén keletkezik. Mg2+ Al3+ és Si4+ Al3+ helyettesítésével MgAlSiAlO6 ideális tschermakit komponenst kapunk. A piroxénnégyszögön kívüli összetételű, kevésbé gyakori piroxének közé tartozik a johannsenit , és a kozmoklorit (ureyit) . A johannsenit a hedenbergitben a vasat mangánnal helyettesíti. A kozmoklórban a vas vagy az alumínium helyett króm (Cr) van egy nátriumos piroxénben.
Magas hőmérsékleten a piroxéneknek kiterjedtebb szilárd oldatmezői vannak, mint alacsonyabb hőmérsékleten. Következésképpen a hőmérséklet csökkenésével a piroxén szilárd halmazállapotban úgy módosítja összetételét, hogy egy külön fázist old ki lamellák formájában a gazdatest piroxénszemcsén belül. A lamellák meghatározott kristályográfiai irányok mentén oldódnak ki, párhuzamos és halszálkás textúrájú, orientált szemcsék keletkeznek. Az exsolúciós pároknak öt fő kombinációja létezik: (1) augit enstatitlamellákkal, (2) augit galambitlamellákkal, (3) augit galambit- és enstatitlamellákkal, (4) galambit augitlamellákkal és (5) enstatit augitlamellákkal.
A piroxének két fő tekintetben különböznek összetételileg az amfibóloktól. A piroxének nem tartalmaznak esszenciális vizet hidroxilok formájában a szerkezetükben, míg az amfibolokat vizes szilikátoknak tekintik. A második kulcsfontosságú kémiai különbség a kettő között az amfibolokban az A-site jelenléte, amely a nagy alkáli elemeket, jellemzően nátriumot és időnként káliumot tartalmaz; a piroxéneknek nincs megfelelő, káliumot befogadni képes helyük.
Szerkezet
A piroxéncsoportba olyan ásványok tartoznak, amelyek mind az orthorombiás, mind a monoklin kristályrendszerben képződnek. Az orthorombikus piroxéneket ortopiroxéneknek, a monoklin piroxéneket pedig klinopiroxéneknek nevezik. Valamennyi piroxén szerkezetének alapvető jellemzője a szilícium-oxigén (SiO4) tetraéderek összekapcsolódása azáltal, hogy a négy sarokból kettőt megosztva folytonos láncokat alkotnak. A c-krisztallográfiai tengellyel végtelenül párhuzamosan húzódó láncok (Si2O6) összetételűek (2. ábra). A lánc hossza mentén körülbelül 5,3 Å ismétlődési távolság határozza meg az egységcella c-tengelyét. A Si2O6 láncok egy oktaéderes koordinációjú kationsávok rétegéhez kapcsolódnak, amelyek szintén a c-tengellyel párhuzamosan húzódnak.
.png)
2. ábra: az egyláncú piroxén szerkezetének sematikus ábrája. Ahol két tetraéder összeér, ott egy oxigénionon osztoznak. A Wikipédiából
Az oktaéderes sávok két ellentétes irányú tetraéderes lánc közé szorított M1 és M2 oktaéderekből állnak. Az M1 helyeket kisebb kationok, például magnézium, vas, alumínium és mangán foglalják el, amelyek hat oxigénatomhoz koordinálva szabályos oktaédert alkotnak. A monoklin piroxénekben az M2 hely egy nagy szabálytalan poliéder, amelyet a nagyobb kalcium- és nátriumkationok foglalnak el, amelyek nyolcszoros koordinációban vannak. Az alacsony kalciumtartalmú orthorombos piroxénekben az M2 magnéziumot és vasat tartalmaz, és a poliéder szabályosabb oktaéder alakot vesz fel. Az M1 kationcsík két ellentétes irányú tetraéderes lánc oxigénatomjához kötődik (3. ábra). Ezek együtt egy tetraéder-oktaéder-tetraéder (t-o-t) szalagot alkotnak. A piroxén szerkezetének a c-tengelyre merőleges sematikus vetülete és a piroxén hasadásának a t-o-t csíkokhoz vagy I-gerendákhoz való viszonya a 3. ábrán látható.
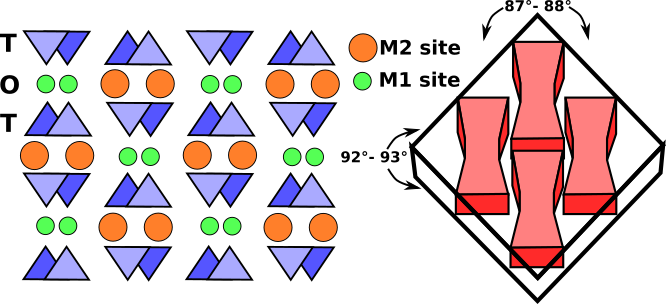
3. ábra: A monoklin piroxén szerkezetének a c-tengelyre merőleges sematikus vetülete. A T-O-T csíkok, az úgynevezett I-gerendák nagyon erős kötésekkel rendelkeznek, amelyek ellenállnak a törésnek, és a piroxénekre jellemző, közel 90°-os hasadási irányt eredményeznek (szaggatott vonalak).
A monoklin piroxéneket vékonymetszeteken a két, kb. 87°-os és 93°-os hasadási irány, a nyolcoldalú bazális keresztmetszet és a világosbarna vagy zöld szín különbözteti meg. Az orthorhombos piroxének abban különböznek a monoklin piroxénektől, hogy párhuzamos töréssel rendelkeznek.
Bibliográfia
– Cox et al. (1979): The Interpretation of Igneous Rocks, George Allen and Unwin, London.
– Howie, R. A., Zussman, J., & Deer, W. (1992). Bevezetés a kőzetalkotó ásványokba (696. o.). Longman.
– Le Maitre, R. W., Streckeisen, A., Zanettin, B., Le Bas, M. J., Bonin, B., Bateman, P., & Lameyre, J. (2002). Igneous rocks. A classification and glossary of terms, 2. Cambridge University Press.
– Middlemost, E. A. (1986). Magmák és magmás kőzetek: bevezetés az magmás petrológiába.
– Shelley, D. (1993). Igneous and metamorphic rocks under the microscope: classification, textures, microstructures and mineral preferred-orientations.
– Vernon, R. H. & Clarke, G. L. (2008): Principles of Metamorphic Petrology. Cambridge University Press.