US Pharm. 2009;34(11):26-39.
Incertitudinea este mare atunci când vine vorba de selectarea antidepresivului adecvat pentru pacienții diagnosticați cu tulburare depresivă majoră (MDD), nu numai pentru că studiile nu au raportat diferențe de eficacitate între agenți, ci și pentru că doar 11% până la 30% dintre pacienți vor ajunge la remisiune cu tratamentul inițial, chiar și după un an.1,2 În consecință, acest lucru i-a determinat pe clinicieni să practice într-un mod de tip încercare și eroare pentru a trata depresia.3 Mai mult, ultima revizuire majoră a Manualului de Diagnostic și Statistică a Tulburărilor Mentale (DSM-IV-TR) a fost elaborată în anul 2000.4 În 2005, a fost publicat un ghid de supraveghere pentru a trece în revistă preocupările importante privind siguranța care apăruseră în legătură cu unii agenți, cum ar fi nefazodona, precum și pentru a analiza două noi antidepresive aprobate în acel an, escitalopramul și duloxetina.5 Revizuirea și actualizarea DSM-IV-TR (manuscrisul DSM-V) nu este prevăzută până în mai 2012. Prin urmare, este nevoie de o revizuire actualizată pentru a ajuta clinicienii să decidă asupra agenților adecvați pentru tratarea pacienților individuali.
Studiul Sequenced Treatment Alternatives to Relief Depression (STAR*D) din 2007 a încercat să dezvolte și să evalueze strategii de tratament fezabile pentru a îmbunătăți rezultatele clinice pentru pacienții cu depresie rezistentă la tratament care au fost identificați cu un episod depresiv major curent.6 În mod specific, STAR*D a urmărit să determine care dintre mai multe tratamente este cel mai eficient „pas următor” pentru pacienții care nu ating remisiunea cu un tratament inițial sau ulterior sau care nu pot tolera tratamentul. Rezultatele generale ale acestui studiu au demonstrat că diferențele farmacologice dintre medicamentele psihotrope nu s-au tradus prin diferențe clinice substanțiale, deși tolerabilitatea a fost diferită.6
Scopul acestui articol este de a trece în revistă dovezile de tratament disponibile în literatura de specialitate pentru a oferi o referință rapidă care să ajute clinicienii să decidă asupra agentului adecvat, luând în considerare efectele adverse, interacțiunile medicamentoase și siguranța medicamentelor, precum și caracteristicile pacienților.
Ce este depresia?
Depresia poate fi o tulburare mentală cronică sau recurentă care se prezintă cu mai multe simptome, cum ar fi starea de spirit depresivă, pierderea interesului sau a plăcerii, sentimente de vinovăție, tulburări de somn sau de apetit, energie scăzută și dificultăți de gândire.7 Depresia poate duce la afectarea substanțială a capacității unui individ de a se ocupa de responsabilitățile zilnice. Depresia poate duce, de asemenea, la sinucidere, o tragedie care reprezintă pierderea a aproximativ 850.000 de vieți la nivel mondial în fiecare an.7
Prevalența și populațiile cu risc
Se estimează că există 121 de milioane de persoane la nivel mondial afectate de depresie.7 În 2000, depresia a fost al patrulea contributor principal la povara globală a bolilor dintre toate bolile, iar până în 2020 se anticipează că va crește până la al doilea contributor principal la povara globală a bolilor, după bolile de inimă.7
Populațiile cu risc mai mare de a dezvolta depresie includ femeile, persoanele cu vârste cuprinse între 24 și 45 de ani și cele cu rude de gradul întâi cu depresie. Femeile prezintă un risc crescut de depresie până la vârsta de 50 de ani, iar riscul lor pe parcursul vieții este de două ori mai mare decât al bărbaților. Persoanele cu vârste cuprinse între 24 și 45 de ani înregistrează cea mai mare rată de depresie. În cele din urmă, rudele de prim grad ale pacienților depresivi au o probabilitate de 1,5 până la 3 ori mai mare de a suferi de depresie decât ceilalți.4,8
Raționamente de fiziopatologie și farmacoterapie
Cauzele biologice și psihosociale au fost ipotezate în încercarea de a descrie fiziopatologia depresiei. Agenții farmacologici vor viza cauzele biologice legate de dereglarea neurotransmițătorilor. Această dereglare este adesea descrisă ca o deficiență a nivelurilor de neurotransmițători cerebrali. Nivelurile de noradrenalină, serotonină și dopamină pot fi diminuate la pacienții cu depresie, asociind astfel o cantitate scăzută de neurotransmițători cu tulburarea.8 Raționamentul farmacoterapiei a fost acela de a stimula aceste deficiențe prin blocarea recaptării sau prevenirea metabolismului enzimatic al neurotransmițătorilor prin intermediul antidepresivelor. În general, aceste mecanisme urmăresc creșterea nivelului de neurotransmițători fie prin forțarea neuronului să tragă mai des și să producă mai mulți neurotransmițători, fie prin prevenirea degradării neurotransmițătorului însuși.
Agenți farmacologici
În prezent sunt disponibile mai multe clase de agenți pentru tratarea depresiei. Acestea includ inhibitori selectivi ai recaptării serotoninei (SSRI), antidepresive triciclice (TCA), inhibitori ai monoaminoxidazei (IMAO) și inhibitori ai recaptării serotoninei-norepinefrinei (SNRI), printre altele.
Antidepresivele au fost asociate cu un risc crescut de gândire suicidară și suicidalitate la copii, adolescenți și adulți tineri în studii controlate cu placebo pe termen scurt privind MDD. Oricine are în vedere utilizarea oricărui antidepresiv la un copil, adolescent sau adult tânăr trebuie să pună în balanță acest risc cu nevoia clinică. Studiile pe termen scurt nu au evidențiat o creștere a riscului de suicidalitate cu antidepresive în comparație cu placebo la adulții de peste 24 de ani și a existat o reducere a riscului cu antidepresive în comparație cu placebo la adulții cu vârsta de 65 de ani și peste. Depresia și alte tulburări psihiatrice sunt la rândul lor asociate cu un risc crescut de suicid. Pacienții de toate vârstele care încep un tratament antidepresiv trebuie monitorizați în mod corespunzător și observați îndeaproape pentru înrăutățire clinică, suicidalitate sau modificări neobișnuite ale comportamentului. 9
Inhibitori selectivi ai recaptării serotoninei4,10: SSRI sunt considerați agenți de primă linie atunci când vine vorba de tratarea pacienților cu depresie. Aceste medicamente includ citalopramul, escitalopramul, fluoxetina, fluvoxamina, paroxetina și sertralina (TABELUL 1). Efectele adverse majore ale acestei clase includ greața, vărsăturile și diareea, care sunt efecte dependente de doză și tind să se disipeze după primele săptămâni de tratament. La unii pacienți, SSRI pot provoca agitație și tulburări de somn, care se vor disipa, de asemenea, cu timpul. Disfuncția sexuală este un efect secundar prezent la toate antidepresivele, dar pare să fie cel mai frecvent în cazul SSRI.
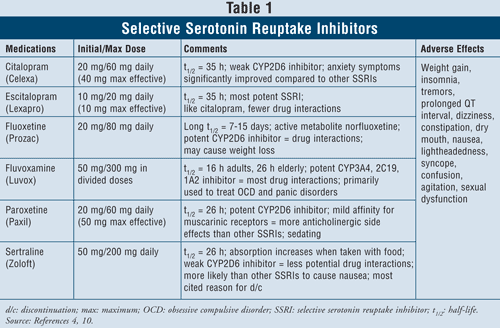
Sindromul serotoninei (adică durere abdominală, diaree, transpirație, modificări ale stării mentale, insuficiență renală, șoc cardiovascular și posibil deces) este un efect advers rar al SSRI. Sindromul serotoninic poate apărea la o creștere a dozei de ISRS sau prin administrarea de ISRS împreună cu plante medicinale precum sunătoarea sau cu droguri ilicite. În cele din urmă, combinarea SSRI cu IMAO poate duce, de asemenea, la interacțiuni medicamentoase letale cu dezvoltarea sindromului serotoninic. Atunci când clinicienii simt nevoia de a trece de la o clasă de agenți la alta, se sugerează să treacă cel puțin cinci jumătăți de viață între momentul în care se întrerupe SSRI și se începe administrarea IMAO.4 Dintre toți agenții din clasă, fluvoxa mine are cea mai mare rată de interacțiuni medicamentoase, deoarece inhibă mai multe enzime hepatice, cum ar fi CYP450 1A2, 2C19, 2C9, 2D6 și 3A4. Fluoxetina urmează îndeaproape rata de interacțiune medicamentoasă a fluvoxaminei, cu inhibarea CYP 2C9, 2D6 și 3A4. În cele din urmă, citalopramul și escitalopramul au cele mai puține interacțiuni medicamentoase, deoarece inhibă într-o măsură mai mică enzimele 2D6.
Când se iau în considerare caracteristicile și siguranța pacienților, SSRI sunt sigure pentru utilizare la majoritatea grupurilor de pacienți, inclusiv la cei cu afecțiuni cardiace preexistente, astm, demență și hipertensiune arterială. Vârstnicii, care sunt deosebit de predispuși la hipotensiune ortostatică, precum și la pierderea în greutate, pot beneficia cel mai mult de utilizarea SSRI, deoarece acești agenți produc creștere în greutate și nu au activitate anticolinergică.
Antidepresive triciclice4,10: TCA-urile blochează recaptarea noradrenalinei și serotoninei, dar au, de asemenea, afinitate pentru receptorii alfa1, H1 și muscarinici, provocând astfel efecte adverse anticolinergice. Există două subclase de agenți disponibili în cadrul acestei clase, TCA-urile cu amină terțiară și secundară (TABELUL 2). TCA cu amină secundară (desipramină, maprotilină, nortriptilină) au mai puțină afinitate pentru receptorii alfa1, H1 și muscarinici, provocând astfel mai puține efecte adverse anticolinergice decât TCA cu amină terțiară (de exemplu, amitriptilină, amoxapină, clomipramină, doxepină, imipramină).
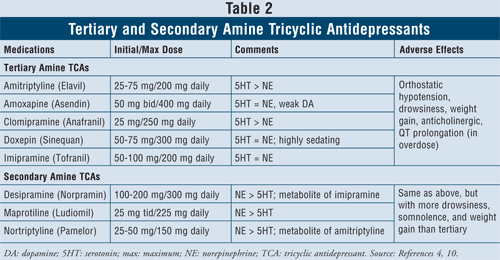
Principalele efecte adverse ale acestei clase de agenți sunt hipotensiunea ortostatică, prelungirea QT, somnolența, uscăciunea gurii, vedere încețoșată, constipația și creșterea în greutate. În general, TCA-urile cu amine terțiare au mai multă activitate serotoninică față de TCA-urile cu amine secundare, care au mai multă activitate noradrenalină, provocând astfel mai puțină somnolență, somnolență și creștere în greutate.
Se știe că TCA-urile inhibă atât enzimele CYP 2C19, cât și 2D6.11 Ele sunt, de asemenea, metabolizate într-o măsură mai mică de enzimele CYP 1A2 și 3A4.12 Din acest motiv, deși interacțiunile medicamentoase cu acești agenți ar putea să nu fie principala preocupare, se recomandă prudență atunci când se combină TCA-urile cu SSRI-urile, deoarece nivelul plasmatic al TCA-urilor are potențialul de a crește de până la patru ori, ceea ce poate duce la efecte toxice.13,14
Când se iau în considerare caracteristicile și siguranța pacienților, TCA-urile sunt contraindicate în unele afecțiuni cardiace specifice, cum ar fi pacienții cu antecedente de aritmii, disfuncție a nodului sinusal sau defecte de conducere. Se recomandă prudență în cazul persoanelor în vârstă, deoarece acestea sunt mai sensibile la blocarea colinergică, precum și la hipotensiunea ortostatică. În plus, persoanele care suferă și de demență vor fi deosebit de sensibile la efectele toxice ale blocadei muscarinice asupra memoriei și a capacității de atenție și, în general, ar fi mai bine să li se administreze antidepresive cu cel mai mic grad de efecte anticolinergice. În cele din urmă, trebuie manifestată prudență atunci când se ia în considerare începerea tratamentului cu TCA la pacienții cu gânduri suicidare, din cauza riscurilor ridicate de letalitate în cazul supradozajului. Doza letală este de numai opt ori mai mare decât doza terapeutică, astfel încât, dacă TCA-urile sunt ingerate în supradozaj, acestea pot bloca nodulul sinoatrial din inimă.
Inhibitori ai monoaminooxidazei4,10: IMAO-urile care sunt disponibile includ izocarboxazidul, fenelzina, selegilina și tranilcipromina (TABELUL 3). În afară de selegilină, care este un inhibitor selectiv al MAO B, toți ceilalți agenți inhibă atât enzimele MAO A, cât și B, responsabile de metabolismul serotoninei, noradrenalinei și dopaminei în creier. Din cauza efectelor adverse severe și a restricțiilor dietetice necesare, IMAO sunt, în general, rezervate pacienților la care au eșuat alte antidepresive.
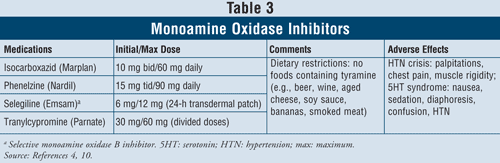
Criza hipertensivă poate apărea atunci când pacienții care iau IMAO ingerează alimente care conțin tiramină, cum ar fi berea, vinul, brânza maturată și carnea afumată. Această reacție se prezintă ca o apariție acută de cefalee severă, greață, rigiditate a gâtului, palpitații cardiace, dureri toracice și confuzie. IMAO pot provoca, de asemenea, sindromul serotoninei. După cum s-a menționat anterior, acest sindrom apare cel mai frecvent atunci când IMAO sunt administrate concomitent cu alți agenți serotoninergici, cum ar fi SSRI sau dacă venlafaxina, un SNRI, este administrată la scurt timp după un IMAO. Atunci când pacienții sunt trecuți de la un SSRI cu un timp de înjumătățire scurt la un IMAO, este important să se respecte o perioadă de spălare de 2 săptămâni între întreruperea SSRI și începerea tratamentului cu IMAO. Dacă SSRI este fluoxetina, care are un timp de înjumătățire lung, perioada de spălare trebuie să fie de 5 săptămâni.4 Alte efecte adverse pot apărea cu IMAO, cum ar fi hipotensiunea ortostatică, creșterea în greutate, disfuncția sexuală și insomnia.
Datorită ratei ridicate de interacțiuni medicamentoase cu acești agenți, trebuie să se manifeste prudență atunci când sunt prescrise la pacienții cu astm care utilizează bronhodilatatoare simpatomimetice. La pacienții cu hipertensiune arterială, IMAO-urile pot induce hipotensiune ortostatică, în special în cazul tratamentelor diuretice concomitente.
Inhibitori ai recaptării serotoninei și noradrenalinei4,10: Inhibitorii recaptării serotoninei și noradrenalinei (SNRI), cum ar fi desvenlafaxina, duloxetina și venlafaxina, pot fi, de asemenea, utilizați ca agenți de primă intenție (TABELUL 4). Aceste medicamente sunt mai sigure decât TCA-urile, iar efectele lor adverse sunt similare cu cele ale SSRI-urilor, inclusiv greață, vărsături și disfuncții sexuale, precum și tensiune arterială crescută.
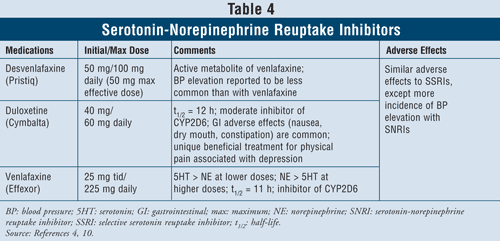
S-a demonstrat că venlafaxina determină o creștere a tensiunii arteriale în 3% până la 13% din cazuri, în timp ce desvenlafaxina a fost raportată ca determinând o creștere a tensiunii arteriale în doar 1% până la 2% din cazuri.10 Astfel, se recomandă evitarea utilizării venlafaxinei la pacienții cu hipertensiune arterială necontrolată, deoarece agentul poate exacerba această afecțiune. Duloxetina are mai multă activitate noradrenalină decât ambii agenți menționați mai sus, fiind astfel utilă în cazul simptomelor fizice, cum ar fi durerile musculare, durerile de cap, problemele stomacale și durerile generalizate, care apar adesea la pacienții cu depresie severă. Datorită eficacității sale în ceea ce privește simptomele durerii, duloxetina a fost aprobată și pentru alte indicații, cum ar fi fibromialgia și durerea neuropată periferică diabetică.15 În cele din urmă, toți cei trei agenți au o activitate mai mare a serotoninei decât a norepinefrinei la doze mai mici și o activitate mai mare a norepinefrinei decât a serotoninei la doze mai mari, având astfel efecte adverse dependente de doză.
Alte antidepresive4,10: Sunt disponibile mai multe alte antidepresive care diferă în mecanismul lor de acțiune de clasele de medicamente descrise anterior.
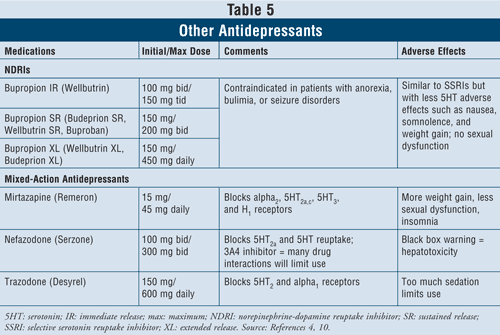
Inhibitorii recaptării noradrenalinei-dopaminei (NDRI), cum ar fi bupropionul de marcă Wellbutrin cu eliberare imediată (IR) (disponibil, de asemenea, în forme farmaceutice cu acțiune prelungită, cum ar fi Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL și Buproban) pot fi utilizați ca agenți de primă linie pentru tratarea depresiei (TABELUL 5). Efectele lor adverse sunt similare cu cele ale ISRS, cu efecte minime asupra serotoninei, cum ar fi greața și creșterea în greutate și cu disfuncții sexuale puține sau deloc. S-a demonstrat că bupropionul exercită efecte benefice asupra simptomelor bolii Parkinson la unii pacienți, dar poate induce, de asemenea, unele simptome psihotice, poate din cauza acțiunii sale agoniste asupra sistemului dopaminergic.16
În cele din urmă, mai sunt disponibile încă trei antidepresive cu acțiune mixtă: mirtazapina, nefazodona și trazodona (TABELUL 5). Toți cei trei agenți blochează diferiți receptori ai serotoninei, având astfel efecte distincte. Mirtazapina determină o mai mare creștere în greutate prin creșterea poftei de mâncare. Nefazodona are utilizări limitate din cauza hepatotoxicității și a inhibării enzimei CYP3A4, ceea ce duce la interacțiuni medicamentoase. Trazodona blochează în mare măsură receptorii de serotonină, cu o slabă legare la receptorii muscarinici. Pot apărea efecte adverse precum sedare, cefalee, tulburări de memorie, uscăciune a gurii și constipație. De asemenea, se recomandă prudență în cazul utilizării trazodonei la bărbați din cauza riscului de priapism.
Concluzie
În general, medicamentele antidepresive s-au dovedit a fi la fel de eficiente; prin urmare, alegerea medicamentelor trebuie să se bazeze pe efectele adverse, interacțiunile medicamentoase, siguranța și preferințele pacientului. Mai mulți algoritmi sunt disponibili pentru a ghida clinicianul în timpul tratamentului pacientului, în special algoritmul recent actualizat al Departamentului de Stat al Serviciilor de Sănătate din Texas pentru tratamentul MDD (actualizat în iulie 2008).17 În cazul în care pacienții prezintă un răspuns parțial, clinicienii pot alege să mărească doza, să treacă la un agent alternativ sau să administreze o combinație de antidepresive. Dimpotrivă, dacă pacienții nu răspund sau nu pot tolera medicamentul, schimbarea cu un agent alternativ este, de asemenea, adecvată, luând în considerare faptul că efectele terapeutice vor apărea, de obicei, între 4 și 6 săptămâni, chiar dacă efectele adverse ar putea apărea după 1 săptămână de tratament.4,17 În plus, deși efectele adverse apar la începutul tratamentului, acestea se disipă, în general, după 2 până la 3 săptămâni.4,17 Cu toate acestea, antidepresivul care va asigura cel mai probabil ameliorarea și siguranța unui pacient poate fi determinat, cel puțin parțial, prin încercări și erori. Având în vedere dificultatea de a prezice ce medicament va fi atât eficient pentru un pacient individual, cât și tolerat de acesta, familiarizarea cu un spectru larg de antidepresive este prudentă și utilă.
1. Song F, Freemantle N, Sheldon TA, et al. Inhibitori selectivi ai recaptării serotoninei: meta-analiză a eficacității și acceptabilității. BMJ. 1993;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRIs versus alte antidepresive pentru tulburarea depresivă. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selecting among second-step antidepressant medication monotherapies: predictive value of clinical, demographic, or first-step treatment features. Arch Gen Psychiatry. 2008;65:870-881.
4. American Psychiatric Association. Manualul diagnostic și statistic al tulburărilor mintale, ediția a patra, Revizuirea textului (DSM-IV-TR). Washington, DC: American Psychiatric Association; 2000.
5. Grupul de lucru pentru tulburarea depresivă majoră. Guideline Watch: Ghid de practică pentru tratamentul pacienților cu tulburare depresivă majoră. Ediția a 2-a. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigarea în studiul Sequenced Treatment Alternatives to Relief Depression (STAR*D): rezultate practice și implicații pentru tratamentul depresiei în asistența medicală primară. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Organizația Mondială a Sănătății. www.who.int/mental_health/management/depression/definition/en. Accesat la 5 octombrie 2009.
8. Dipiro JT, Talbert RL, Yee GC, et al. Pharmacotherapy: A Pathophysiologic Approach. Ediția a 6-a. New York, NY: McGraw-Hill; 2005.
9. Revizuiri la etichetarea produselor. Suiciditatea și medicamentele antidepresive. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Accesat la 5 octombrie 2009.
10. Informații despre medicamente. Seria Micromedex Healthcare. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Accesat la 5 octombrie 2009.
11. Shin J-G, Park J-Y, Park J-Y, Kim M-J, et al. Efectele inhibitorii ale antidepresivelor triciclice asupra enzimelor citocromului P450 uman in vitro: mecanism de interacțiune medicamentoasă între TCA și fenitoină. Drug Metab Dispos. 2002;30:1102-1107.
12. Brown CH. Prezentare generală a interacțiunilor medicamentoase cu SSRI. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Interacțiuni medicamentoase metabolice cu noii agenți psihotropi. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. Cuantificarea și mecanismul interacțiunii dintre fluoxetină și antidepresivele triciclice. Clin Pharmacol Ther. 1992;51:239-248.
15. Prospectul Cymbalta (clorhidrat de duloxetină). Indianapolis, IN: Eli Lilly and Company; februarie 2009. http://pi.lilly.com/us/cymbalta-pi.pdf. Accesat la 5 octombrie 2009.
16. Goetz CG, Tanner CM, Klawans HL. Bupropion în boala Parkinson. Neurologie. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Algoritmi de tulburare depresivă majoră. Texas Department of State Health Services; iulie 2008. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Accesat la 5 octombrie 2009.
Pentru a comenta acest articol, contactați [email protected].
.