30-letni mężczyzna z niewyraźnym widzeniem centralnym
Alex W. Cohen, MD, PhD and Jordan M. Graff, MD
March 9, 2008
Updated by Lindsay K. McConnell, MD
May 8, 2017
Chief Complaint: Zamazane centralne widzenie w lewym oku.
Historia obecnej choroby: 30-letni biały mężczyzna zauważył centralne zniekształcenie widzenia i utratę widzenia w lewym oku (OS) w ciągu ostatnich kilku tygodni. Jego miejscowy optometrysta skierował go do Wydziału Okulistyki i Nauk o Wzroku Uniwersytetu Iowa w celu dalszej oceny.
Przeszła historia oczna: Brak.
Historia medyczna: Pacjent nie zgłaszał wcześniejszych chorób ogólnoustrojowych ani schorzeń.
Leki: Brak.
Historia rodzinna: Brak rodzinnych chorób oczu i poza tym bez współudziału.
Historia społeczna: Żonaty, mieszka z żoną. Pracuje jako programista komputerowy. Pacjent przez całe życie mieszkał w Dolinie Rzeki Missisipi.
Badanie okulistyczne:
- Ostrość wzroku, bez korekcji: Prawe oko (OD)–20/20; OS–20/40
- Motility: Pełna, oboje oczu (OU)
- Ciśnienie wewnątrzgałkowe: OD — 15 mmHg; OS — 16 mmHg
- Pupils: Jednakowo reaktywne na światło. Brak względnego aferentnego defektu źrenic (RAPD)
- Konfrontacyjne pola widzenia (CVF): Pełne, OU
- Badanie odcinka zewnętrznego i przedniego: Normalne, OU
- Badanie dna oka (Dilated fundus examination, DFE):
- OD: Przejrzysta szklistka i zdrowy nerw wzrokowy bez bladości i obrzęku. Występuje atrofia okołopapilarna i ciemna pigmentacja. Plamka i naczynia prawidłowe. Na obwodzie znajduje się kilka „wybijających się” blizn chorioretinalnych.
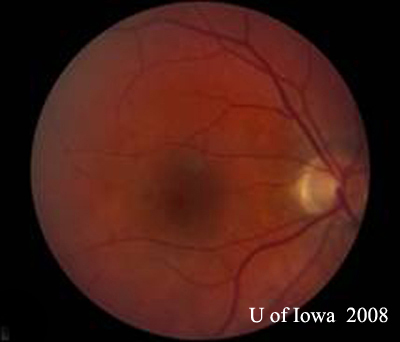
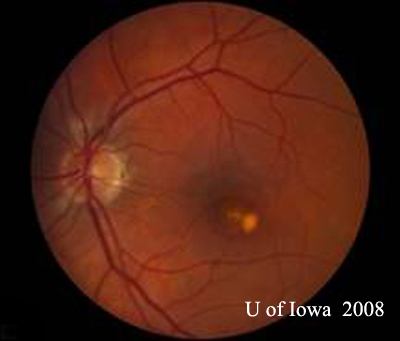
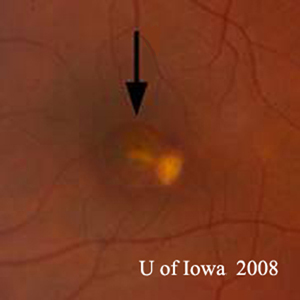
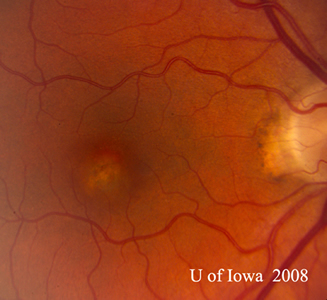
- OS: Przejrzysta szklistka bez komórek i oznak zapalenia. Głowa nerwu wzrokowego jest zdrowa, bez bladości i obrzęku. Występuje atrofia okołopapilarna i zwiększona pigmentacja. W obrębie plamki żółtawe zmiany podsiatkówkowe (patrz ryc. 1 i 2).
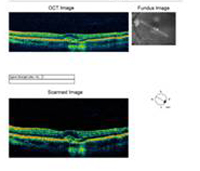
| A: Zdjęcie dna oka pod kątem 30 stopni, OD. Zwracają uwagę zmiany zanikowe okołogałkowe. | B: Zdjęcie dna oka pod kątem 30 stopni, OS. Widoczne są podobne okołogałkowe zmiany zanikowe i zmiany pigmentowe. Należy zwrócić uwagę na chorioretinalny „histospot” w obrębie plamki i brak jakiegokolwiek zapalenia ciała szklistego. |
 |
 |
|
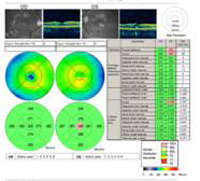
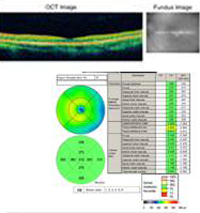
A: Skany optycznej koherentnej tomografii (OCT) obu oczu wykazują wzrost centralnej grubości plamki (CMT) OS (295µm) w porównaniu z OD (205µm). A). |
B: Zwróć uwagę na obecność płynu podsiatkówkowego i zniekształcenie wgłębienia foveal, OS. |
 |
 |
Przebieg: Ten pacjent ma historię i wygląd kliniczny silnie sugerujący przypuszczalny zespół histoplazmozy ocznej (POHS). Chociaż jego gruba, żółta zmiana plamkowa nie jest idealnie klasyczna (patrz Rycina 5 i Dyskusja poniżej), wszystko wskazuje na to, że naczyniówkowa błona neowaskularna (CNVM) rozwinęła się w tej lewej plamce w miejscu blizny chorioretinalnej. Omówiliśmy z pacjentem szczegółowo opcje leczenia, w tym uznane badania kliniczne dotyczące laseroterapii plamki żółtej lub terapii fotodynamicznej (PDT) zmiany. Dodatkowo, pacjent został poinformowany o wczesnych wynikach w literaturze i osobistych doświadczeniach sugerujących dobre wyniki z pozarejestracyjnym stosowaniem bevacizumabu (Avastin). Pacjent wybrał iniekcję dożylną, którą wykonano bez komplikacji. Widziano go ponownie cztery tygodnie po wstrzyknięciu, w tym czasie jego wzrok poprawił się do 20/20, a zmiana siatkówki była sucha zarówno klinicznie, jak i w badaniu OCT (ryc. 4).
Discussion: Przypuszczalny oczny zespół histoplazmozy (POHS) jest rozpoznaniem klinicznym postawionym na podstawie konstelacji wyników badań ocznych, które zostały pierwotnie opisane w 1960 roku. Zespół ten jest zaburzeniem zapalnym, które postuluje się jako wynik ogólnoustrojowego zakażenia dimorficznymi grzybami Histoplasma capsulatum. Nie przeprowadzono jednak badań potwierdzających, które bezpośrednio wiązałyby udział tego grzyba w patogenezie choroby. Dane epidemiologiczne sugerują raczej, że częstość występowania POHS jest znacznie zwiększona na obszarach endemicznego występowania Histoplasma. Wiadomo, że u mieszkańców dolin rzek Ohio i Mississippi odsetek dodatnich testów skórnych w kierunku ekspozycji na H.capsulatum sięga 70%. Rzeczywiście, zdecydowana większość pacjentów z POHS reaguje pozytywnie na ten test skórny. Jednakże, tylko około 4,4% pacjentów z pozytywnym wynikiem testu skórnego ma dowody na występowanie POHS. Dlatego związek pomiędzy H. capsulatum i POHS pozostaje domniemany.
Uwaga, pacjenci z POHS są często młodzi i zdrowi, a zmiany w siatkówce mogą powodować znaczną funkcjonalną utratę wzroku w tej populacji w wieku produkcyjnym.
Diagnoza POHS jest stawiana na podstawie identyfikacji klasycznych wyników badań dna oka. Są to: obecność peryapilarnego zaniku lub pigmentacji, obecność charakterystycznych „wykrawanych” chorioretinalnych zmian zanikowych i brak leżącego nad nimi zajęcia ciała szklistego. Uważa się, że zmiany okołonaczyniowe reprezentują zregenerowaną neowaskularną błonę naczyniową naczyniówki (CNVM), a „wyłupiaste” zmiany reprezentują obszary hematogennego wysiewu H. capsulatum do siatkówki. Należy zauważyć, że wiele z obwodowych „wykrawanych” blizn naczyniówkowych może być również związanych z małymi CNVM, które nie zwracają uwagi klinicznej i ulegają samoistnej regresji. Klasyczne przykłady takich zmian można zobaczyć na rycinie 5. Często, tak jak w przedstawionym przypadku, POHS zgłasza się do okulisty z objawowym CNVM obejmującym plamkę lub fovea. W tym przypadku zmiana plamkowa była nieco nietypowa, z grubą żółtą substancją, podczas gdy CNVM w POHS jest często szaro-zieloną koronkową siatką powstającą z blizny chorioretinalnej (patrz Rycina 6), która jest zdefiniowana wcześnie na angiogramie i przecieka późno.
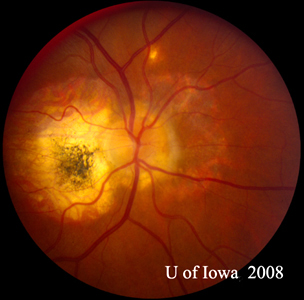
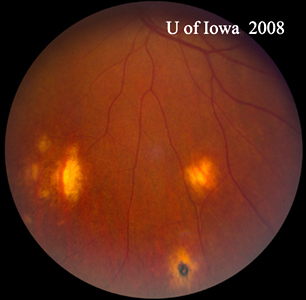
| A: POHS u pacjenta ze znacznym zanikiem okołotarczowym i zmianami barwnikowymi, demonstrujący wygląd cofniętego okołotarczowego CNVM, który był postulowany jako źródło tych zmian. | B: Obwodowe blizny chorioretinalne u pacjenta z POHS. |
 |
 |
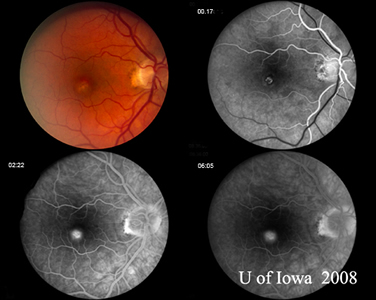
| A: Szaro-zielona plamka CNVM u pacjenta z POHS | B: Angiogram fluoresceinowy pacjenta z ryciny 6A demonstruje klasyczny wzór przecieku związany z CNVM u pacjenta z POHS. |
 |
 |
Patogeneza CNVM jest nieznana; jednakże, kilku autorów zasugerowało, że po hematogennym rozprzestrzenieniu się organizmów do siatkówki, pojawiają się obszary ogniskowego zapalenia, prowadzące do przerwania ciągłości błony Brucha, a tym samym predysponujące do tworzenia CNVM. Postuluje się również, że POHS może być wynikiem wyzwalania autoimmunologicznego, które jest stymulowane przez obecność drobnoustroju zakaźnego. W każdym razie, pacjenci są zwykle albo identyfikowani w czasie bezobjawowym (mniejszość), albo zgłaszają się do okulisty ze skargami na pogorszenie widzenia.
Leczenie POHS rozwinęło się w ciągu ostatnich kilku lat, i podczas gdy nie ma bezpośredniej terapii skierowanej na organizm, kilka metod zostało zidentyfikowanych jako korzystne w leczeniu towarzyszących CNVM. Dawniej fotokoagulacja laserowa prowadziła do zahamowania dobrze zdefiniowanych, klasycznych zmian pozagałkowych, podspojówkowych i okołogałkowych w POHS. Wynikająca z tego skotoma centralna była jednak niekiedy nie do zaakceptowania w porównaniu z nowszymi opcjami terapeutycznymi. Terapia fotodynamiczna (PDT) z werteporfiną została zatwierdzona przez FDA do leczenia CNVM związanych z POHS pod koniec 2001 roku i okazała się bezpieczna i skuteczna w leczeniu tej choroby. Po udowodnieniu skuteczności leków anty-VEGF w leczeniu CNVM związanych z AMD, w połowie XXI wieku opublikowano opisy przypadków wskazujące na ich skuteczność w leczeniu błon neowaskularnych u pacjentów z POHS. Po opublikowaniu licznych opisów przypadków i retrospektywnych przeglądów wykazujących skuteczność leczenia środkami anty-VEGF, stały się one standardem postępowania wykorzystującym te same zasady, co w leczeniu CNVM związanego z AMD.
Diagnoza: Przypuszczalny zespół histoplazmozy ocznej (POHS) z CNVM
EPIDEMIOLOGIA
|
ZNACZENIA
|
SYMPTOMY
|
TREATMENT
|
Diagnozy różnicowe dla blizny chorioretinalnej plamki z towarzyszącym płynem:
- Toksoplazmoza (miałaby zapalenie ciała szklistego)
- Zwyrodnienie krótkowzroczne
- Smugi angiodowe
- Zwyrodnienie plamki żółtej
- Age-Related Macular Degeneration (AMD)
- Central Serous Chorioretinopathy (CSCR)
- Punctate Inner Choroidopathy (PIC)
- Multifocal Choroiditis (MFC)
- Idiopathic CNVM
- Prasad AG, Van Gelder RN. Przypuszczalny oczny zespół histoplazmozy. Curr Opin Ophthalmol 2005;16(6):364-368. https://www.ncbi.nlm.nih.gov/pubmed/16264347
- Oliver A, Ciulla TA, Comer GM. New and classic insights into presumed ocular histoplasmosis syndrome and its treatment. Curr Opin Ophthalmol 2005;16(3):160-165. https://www.ncbi.nlm.nih.gov/pubmed/15870572
- Rosenfeld PJ, Saperstein DA, Bressler NM, Reaves TA, Sickenberg M, Rosa RH, Jr., Sternberg P, Jr., Aaberg TM, Sr., Aaberg TM, Jr., Verteporfin in Ocular Histoplasmosis Study G. Photodynamic therapy with verteporfin in ocular histoplasmosis: uncontrolled, open-label 2-year study. Ophthalmology 2004;111(9):1725-1733. https://www.ncbi.nlm.nih.gov/pubmed/15350329
- Adan A, Navarro M, Casaroli-Marano RP, Ortiz S, Molina JJ. Intravitreal bevacizumab as initial treatment for choroidal neovascularization associated with presumed ocular histoplasmosis syndrome. Graefes Arch Clin Exp Ophthalmol 2007;245(12):1873-1875. https://www.ncbi.nlm.nih.gov/pubmed/17786466
- Schadlu R, Blinder KJ, Shah GK, Holekamp NM, Thomas MA, Grand MG, Engelbrecht NE, Apte RS, Joseph DP, Prasad AG, Smith BT, Sheybani A. Intravitreal bevacizumab for choroidal neovascularization in ocular histoplasmosis. Am J Ophthalmol 2008;145(5):875-878. https://www.ncbi.nlm.nih.gov/pubmed/18321466
- Weingeist TA, Watzke RC. Ocular involvement by histoplasma capsulatum. Int Ophthalmol Clin 1983;23(2):33-47. https://www.ncbi.nlm.nih.gov/pubmed/6189798
- Cionni DA, Lewis SA, Petersen MR, Foster RE, Riemann CD, Sisk RA, Hutchins RK, Miller DM. Analysis of outcomes for intravitreal bevacizumab in the treatment of choroidal neovascularization secondary to ocular histoplasmosis. Ophthalmology 2012;119(2):327-332. https://www.ncbi.nlm.nih.gov/pubmed/22133795
- Zwyrodnienie plamki związane z wiekiem i inne przyczyny neowaskularyzacji naczyniówkowej. Basic and clinical science course (BCSC) Section 12: Retina and Vitreous. San Francisco: American Academy of Ophthalmology; 2014-2015.
Sugerowany format cytowania
McConnell LK. Revision of ; EyeRounds.org. July 5, 2017; Available from: http://www.EyeRounds.org/cases/83-Presumed-Ocular-Histoplasmosis-POHS.htm.
.