US Pharm. 2009;34(11):26-39.
Niepewność jest duża, jeśli chodzi o wybór odpowiedniego leku przeciwdepresyjnego dla pacjentów z rozpoznaniem dużej depresji (major depressive disorder, MDD), nie tylko dlatego, że badania nie wykazały różnic w skuteczności poszczególnych leków, ale także dlatego, że tylko 11% do 30% pacjentów osiągnie remisję po zastosowaniu początkowego leczenia, nawet po roku.1,2 W konsekwencji doprowadziło to klinicystów do stosowania w leczeniu depresji metody prób i błędów.3 Ponadto ostatnią dużą rewizję podręcznika diagnostyczno-statystycznego zaburzeń psychicznych (DSM-IV-TR) przeprowadzono w 2000 roku.4 W 2005 roku opublikowano wytyczne, w których dokonano przeglądu istotnych obaw dotyczących bezpieczeństwa niektórych leków, takich jak nefazodon, a także przeglądu dwóch nowych leków przeciwdepresyjnych dopuszczonych do obrotu w tym samym roku – escitalopramu i duloksetyny.5 Rewizja i aktualizacja DSM-IV-TR (manuskrypt DSM-V) ma nastąpić dopiero w maju 2012 roku. Dlatego istnieje potrzeba aktualnego przeglądu, który pomoże klinicystom w podejmowaniu decyzji o wyborze odpowiednich środków do leczenia poszczególnych pacjentów.
W badaniu Sequenced Treatment Alternatives to Relieve Depression (STAR*D) z 2007 roku podjęto próbę opracowania i oceny możliwych do zastosowania strategii leczenia w celu poprawy wyników klinicznych u pacjentów z depresją oporną na leczenie, u których rozpoznano aktualny epizod dużej depresji.6 Celem badania STAR*D było w szczególności określenie, która z kilku metod leczenia jest najskuteczniejszym „kolejnym krokiem” dla pacjentów, u których nie uzyskano remisji po zastosowaniu początkowego lub kolejnego leczenia lub którzy nie tolerują leczenia. Ogólne wyniki tego badania wykazały, że różnice farmakologiczne między lekami psychotropowymi nie przekładały się na istotne różnice kliniczne, chociaż tolerancja była różna.6
Celem tego artykułu jest przegląd dostępnych w piśmiennictwie dowodów dotyczących leczenia w celu zapewnienia szybkiej informacji, która pomoże klinicystom w podjęciu decyzji o wyborze odpowiedniego środka, z uwzględnieniem działań niepożądanych, interakcji lekowych i bezpieczeństwa stosowania leków, a także charakterystyki pacjenta.
Czym jest depresja?
Depresja może być przewlekłym lub nawracającym zaburzeniem psychicznym, które objawia się kilkoma symptomami, takimi jak obniżony nastrój, utrata zainteresowań lub przyjemności, poczucie winy, zaburzenia snu lub apetytu, niski poziom energii oraz trudności w myśleniu.7 Depresja może prowadzić do znacznego upośledzenia zdolności danej osoby do wykonywania codziennych obowiązków. Depresja może również prowadzić do samobójstwa, które jest tragedią i każdego roku powoduje śmierć około 850 000 osób na całym świecie.7
Prevalence and At-Risk Populations
Oszacowano, że depresja dotyka 121 milionów osób na całym świecie.7 W 2000 roku depresja zajmowała czwarte miejsce wśród wszystkich chorób powodujących globalne obciążenie chorobami, a przewiduje się, że do 2020 roku stanie się drugim co do wielkości czynnikiem powodującym globalne obciążenie chorobami, ustępując jedynie chorobom serca.7
Populacje o podwyższonym ryzyku zachorowania na depresję to kobiety, osoby w wieku od 24 do 45 lat oraz osoby, których krewni pierwszego stopnia chorowali na depresję. Kobiety są narażone na zwiększone ryzyko zachorowania na depresję do 50. roku życia, a ich ryzyko w ciągu całego życia jest dwukrotnie większe niż mężczyzn. Największe ryzyko depresji występuje u osób w wieku od 24 do 45 lat. Wreszcie, u krewnych pierwszego stopnia pacjentów z depresją prawdopodobieństwo wystąpienia depresji jest od 1,5 do 3 razy większe niż u innych osób.4,8
Patofizjologia i farmakoterapia
Podjęto próbę opisania patofizjologii depresji na podstawie hipotez dotyczących przyczyn biologicznych i psychospołecznych. Środki farmakologiczne będą ukierunkowane na przyczyny biologiczne związane z dysregulacją neuroprzekaźników. Dysregulacja ta jest często opisywana jako niedobór poziomu neuroprzekaźników w mózgu. Poziomy noradrenaliny, serotoniny i dopaminy mogą być obniżone u pacjentów z depresją, co wiąże się z obniżoną ilością neuroprzekaźników z tym zaburzeniem.8 Przesłanką farmakoterapii jest zwiększenie tych niedoborów poprzez blokowanie wychwytu zwrotnego lub zapobieganie metabolizmowi enzymatycznemu neuroprzekaźników za pomocą leków przeciwdepresyjnych. Ogólnie rzecz biorąc, mechanizmy te mają na celu zwiększenie poziomu neuroprzekaźników albo poprzez zmuszenie neuronu do częstszego zapłonu i wytwarzania większej ilości neuroprzekaźników, albo poprzez zapobieganie degradacji samego neuroprzekaźnika.
Leki farmakologiczne
Wiele klas leków jest obecnie dostępnych w leczeniu depresji. Należą do nich między innymi selektywne inhibitory wychwytu zwrotnego serotoniny (SSRI), trójcykliczne leki przeciwdepresyjne (TCA), inhibitory monoaminooksydazy (MAOI) oraz inhibitory wychwytu zwrotnego serotoniny i noradrenaliny (SNRI).
Leki przeciwdepresyjne były związane ze zwiększonym ryzykiem myśli samobójczych i samobójstw u dzieci, młodzieży i młodych dorosłych w krótkoterminowych badaniach kontrolowanych placebo dotyczących MDD. Każdy, kto rozważa zastosowanie jakiegokolwiek leku przeciwdepresyjnego u dziecka, nastolatka lub młodego dorosłego, musi zrównoważyć to ryzyko z potrzebą kliniczną. W badaniach krótkoterminowych nie wykazano zwiększenia ryzyka samobójstwa w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo u osób dorosłych w wieku powyżej 24 lat, a u osób dorosłych w wieku 65 lat i starszych obserwowano zmniejszenie ryzyka w przypadku stosowania leków przeciwdepresyjnych w porównaniu z placebo. Depresja i inne zaburzenia psychiczne są same w sobie związane ze zwiększonym ryzykiem samobójstwa. Pacjenci w każdym wieku, u których rozpoczyna się leczenie przeciwdepresyjne, powinni być odpowiednio monitorowani i uważnie obserwowani pod kątem pogorszenia stanu klinicznego, myśli samobójczych lub nietypowych zmian w zachowaniu.9
Selektywne inhibitory wychwytu zwrotnego serotoniny4,10: SSRI są uważane za leki pierwszego rzutu w leczeniu pacjentów z depresją. Do leków tych należą citalopram, escitalopram, fluoksetyna, fluwoksamina, paroksetyna i sertralina (TABELA 1). Do głównych działań niepożądanych w tej klasie leków należą nudności, wymioty i biegunka, które są zależne od dawki i ustępują po pierwszych tygodniach leczenia. U niektórych pacjentów SSRI mogą powodować pobudzenie i zaburzenia snu, które również z czasem ustępują. Zaburzenia seksualne są działaniem niepożądanym występującym w przypadku wszystkich leków przeciwdepresyjnych, ale wydają się być najczęstsze w przypadku SSRI.
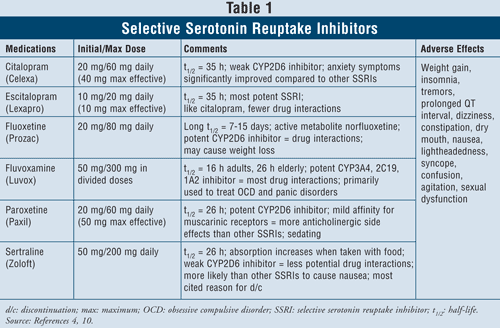
Zespół serotoninowy (tj. ból brzucha, biegunka, pocenie się, zmiana stanu psychicznego, niewydolność nerek, wstrząs sercowo-naczyniowy i prawdopodobnie zgon) jest rzadkim działaniem niepożądanym SSRI. Zespół serotoninowy może wystąpić w przypadku zwiększenia dawki SSRI lub przyjmowania SSRI z lekami ziołowymi, takimi jak dziurawiec zwyczajny, lub z nielegalnymi narkotykami. Wreszcie, łączenie SSRI z MAOI może również prowadzić do śmiertelnych interakcji lekowych z rozwojem zespołu serotoninowego. Gdy klinicyści odczuwają potrzebę przejścia z jednej klasy leków na drugą, sugeruje się, aby między odstawieniem SSRI a rozpoczęciem stosowania MAOI upłynęło co najmniej pięć półokresów.4 Spośród wszystkich leków tej klasy fluwoksa mina ma najwyższy wskaźnik interakcji lekowych, ponieważ hamuje kilka enzymów wątrobowych, takich jak CYP450 1A2, 2C19, 2C9, 2D6 i 3A4. Fluoksetyna, hamując CYP 2C9, 2D6 i 3A4, zbliża się do fluwoksaminy pod względem częstości interakcji z lekami. Wreszcie, citalopram i escitalopram mają najmniej interakcji lekowych, ponieważ w mniejszym stopniu hamują enzymy 2D6.
Rozważając charakterystykę i bezpieczeństwo pacjentów, SSRI są bezpieczne w stosowaniu w większości grup pacjentów, w tym u osób z istniejącą wcześniej chorobą serca, astmą, demencją i nadciśnieniem tętniczym. Osoby w podeszłym wieku, które są szczególnie podatne na niedociśnienie ortostatyczne oraz utratę masy ciała, mogą odnieść największe korzyści ze stosowania SSRI, ponieważ leki te powodują przyrost masy ciała i nie mają działania antycholinergicznego.
Trójcykliczne leki przeciwdepresyjne4,10: TCA blokują wychwyt zwrotny noradrenaliny i serotoniny, ale mają również powinowactwo do receptorów alfa1, H1 i muskarynowych, powodując w ten sposób antycholinergiczne działania niepożądane. Istnieją dwie podklasy środków dostępnych w tej klasie: TCA z aminami trzeciorzędowymi i drugorzędowymi (TABELA 2). TCA z aminami drugorzędowymi (desipramina, maprotylina, nortryptylina) mają mniejsze powinowactwo do receptorów alfa1, H1 i muskarynowych, dlatego powodują mniej działań niepożądanych o charakterze antycholinergicznym niż TCA z aminami trzeciorzędowymi (np. amitryptylina, amoksapina, klomipramina, doksepina, imipramina).
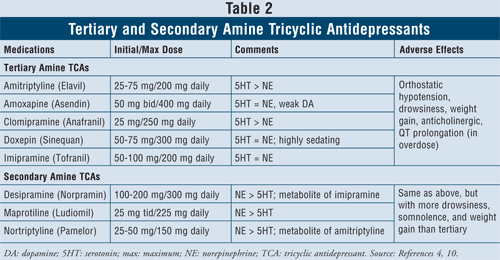
Głównymi działaniami niepożądanymi tej klasy leków są: niedociśnienie ortostatyczne, wydłużenie odstępu QT, senność, suchość w jamie ustnej, niewyraźne widzenie, zaparcia i zwiększenie masy ciała. Ogólnie rzecz biorąc, TCA z aminami trzeciorzędowymi mają większą aktywność serotoninową w porównaniu z TCA z aminami drugorzędowymi, które mają większą aktywność noradrenalinową, co powoduje mniejszą senność, senność i przyrost masy ciała.
Wiadomo, że TCA hamują zarówno enzymy CYP 2C19, jak i 2D6.11 Są one również metabolizowane w mniejszym stopniu przez enzymy CYP 1A2 i 3A4.12 Z tego powodu, mimo że interakcje lek-lek z tymi środkami mogą nie być głównym problemem, zaleca się ostrożność podczas łączenia TCA z SSRI, ponieważ stężenie leku w osoczu TCA może potencjalnie wzrosnąć nawet czterokrotnie, co może prowadzić do działań toksycznych.13,14
Rozważając charakterystykę pacjentów i bezpieczeństwo stosowania, TCA są przeciwwskazane w niektórych szczególnych schorzeniach kardiologicznych, takich jak pacjenci z zaburzeniami rytmu serca w wywiadzie, zaburzeniami czynności węzła zatokowego lub wadami przewodzenia. Zaleca się ostrożność w przypadku osób starszych, ponieważ są one bardziej wrażliwe na blokadę cholinergiczną i niedociśnienie ortostatyczne. Ponadto osoby cierpiące na demencję będą szczególnie podatne na toksyczny wpływ blokady muskarynowej na pamięć i skupienie uwagi i generalnie najlepiej by zrobiły, gdyby otrzymywały leki przeciwdepresyjne o najmniejszym stopniu działania antycholinergicznego. Wreszcie, należy zachować ostrożność, rozważając rozpoczęcie stosowania TCA u pacjentów z myślami samobójczymi, ze względu na wysokie ryzyko śmiertelności w przypadku przedawkowania. Dawka śmiertelna jest tylko osiem razy większa od dawki terapeutycznej, więc jeśli TCA zostaną przyjęte w nadmiernej dawce, mogą zablokować węzeł zatokowo-przedsionkowy w sercu.
Inhibitory oksydazy monoaminowej4,10: Dostępne MAOI obejmują izokarboksazyd, fenelzynę, selegilinę i tranylcyprominę (TABELA 3). Z wyjątkiem selegiliny, która jest selektywnym inhibitorem MAO B, wszystkie pozostałe środki hamują enzymy MAO A i B odpowiedzialne za metabolizm serotoniny, noradrenaliny i dopaminy w mózgu. Ze względu na poważne działania niepożądane i wymagane ograniczenia dietetyczne, MAOI są generalnie zarezerwowane dla pacjentów, u których zawiodły inne leki przeciwdepresyjne.
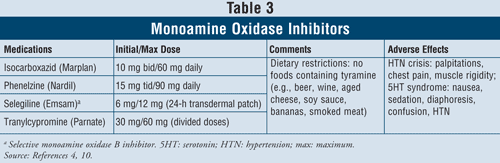
Kryzys nadciśnieniowy może wystąpić, gdy pacjenci przyjmujący MAOI spożyją pokarmy zawierające tyraminę, takie jak piwo, wino, dojrzałe sery i wędzone mięso. Reakcja ta objawia się jako ostry początek silnego bólu głowy, nudności, sztywność karku, kołatanie serca, ból w klatce piersiowej i dezorientacja. MAOI mogą również powodować zespół serotoninowy. Jak wspomniano wcześniej, zespół ten występuje najczęściej, gdy MAOI są przyjmowane jednocześnie z innymi lekami serotoninergicznymi, takimi jak SSRI lub gdy wenlafaksyna, SNRI, jest podawana wkrótce po MAOI. W przypadku zamiany SSRI o krótkim okresie półtrwania na MAOI, ważne jest, aby zachować 2-tygodniowy okres przerwy między odstawieniem SSRI a rozpoczęciem stosowania MAOI. Jeśli SSRI jest fluoksetyna, która ma długi okres półtrwania, okres przerwy powinien wynosić 5 tygodni.4 Podczas stosowania IMAO mogą wystąpić inne działania niepożądane, takie jak niedociśnienie ortostatyczne, zwiększenie masy ciała, zaburzenia czynności seksualnych i bezsenność.
Inhibitory wychwytu zwrotnego serotoniny i noradrenaliny4,10: Leki z grupy SNRI, takie jak desvenlafaksyna, duloksetyna i wenlafaksyna, mogą być również stosowane jako leki pierwszego rzutu (TABELA 4). Leki te są bezpieczniejsze niż TCA, a ich działania niepożądane są podobne jak w przypadku SSRI, w tym nudności, wymioty i zaburzenia funkcji seksualnych, a także podwyższone ciśnienie tętnicze.
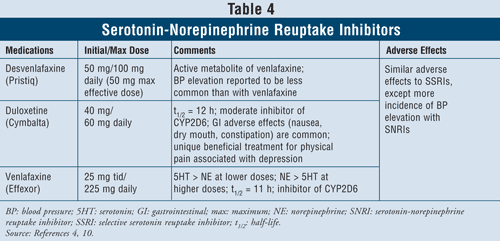
Wykazano, że wenlafaksyna powoduje wzrost ciśnienia tętniczego w 3% do 13% przypadków, natomiast wenlafaksyna powodowała wzrost ciśnienia tętniczego tylko w 1% do 2% przypadków.10 Dlatego zaleca się unikanie stosowania wenlafaksyny u pacjentów z niekontrolowanym nadciśnieniem tętniczym, ponieważ środek ten może nasilać ten stan. Duloksetyna ma większą aktywność noradrenalinową niż oba wyżej wymienione leki, dzięki czemu jest przydatna w przypadku objawów fizycznych, takich jak bóle mięśni, bóle głowy, problemy żołądkowe i uogólniony ból, często występujących u pacjentów z ciężką depresją. Ze względu na skuteczność duloksetyny w zakresie objawów bólowych została ona również zatwierdzona do stosowania w innych wskazaniach, takich jak fibromialgia i ból w obwodowej neuropatii cukrzycowej.15 Wreszcie, wszystkie trzy środki wykazują większą aktywność serotoniny niż noradrenaliny w mniejszych dawkach i większą aktywność noradrenaliny niż serotoniny w większych dawkach, a zatem ich działania niepożądane zależą od dawki.
Inne leki przeciwdepresyjne4,10: Dostępnych jest kilka innych leków przeciwdepresyjnych, które różnią się mechanizmem działania od klas leków opisanych wcześniej.
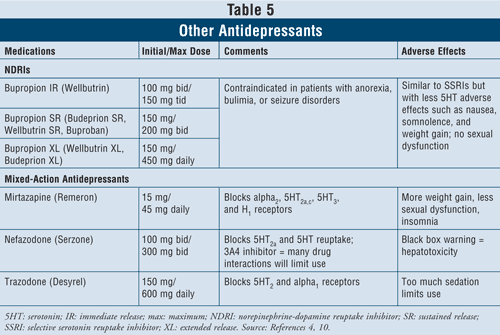
Inhibitory wychwytu zwrotnego noradrenaliny i dopaminy (NDRI), takie jak bupropion o natychmiastowym uwalnianiu (IR) marki Wellbutrin (dostępny również w długo działających postaciach dawkowania, takich jak Wellbutrin XL, Wellbutrin SR, Budeprion SR, Budeprion XL i Buproban) mogą być stosowane jako leki pierwszego rzutu w leczeniu depresji (TABELA 5). Ich działania niepożądane są podobne jak w przypadku SSRI, z minimalnym działaniem na układ serotoninowy, takim jak nudności i przyrost masy ciała oraz niewielkimi zaburzeniami funkcji seksualnych lub ich brakiem. Wykazano, że bupropion wywiera korzystny wpływ na objawy choroby Parkinsona u niektórych pacjentów, ale może również wywoływać pewne objawy psychotyczne, być może z powodu działania agonistycznego na układ dopaminergiczny.16
Wreszcie, dostępne są jeszcze trzy leki przeciwdepresyjne o mieszanym działaniu: mirtazapina, nefazodon i trazodon (TABELA 5). Wszystkie trzy środki blokują różne receptory serotoninowe, przez co mają odmienne działanie. Mirtazapina powoduje większy przyrost masy ciała poprzez zwiększenie apetytu. Nefazodon ma ograniczone zastosowanie ze względu na hepatotoksyczność i hamowanie enzymu CYP3A4, co prowadzi do interakcji lekowych. Trazodon w znacznym stopniu blokuje receptory serotoninowe, słabo wiąże się z receptorami muskarynowymi. Mogą wystąpić działania niepożądane, takie jak uspokojenie, ból głowy, zaburzenia pamięci, suchość w jamie ustnej i zaparcia. Zaleca się również ostrożność podczas stosowania trazodonu u mężczyzn z uwagi na ryzyko wystąpienia priapizmu.
Wnioski
Ogólnie wykazano, że leki przeciwdepresyjne są równie skuteczne; Dlatego wybór leku powinien być oparty na działaniach niepożądanych, interakcjach lekowych, bezpieczeństwie i preferencjach pacjenta. Dostępnych jest kilka algorytmów, które mogą być wskazówkami dla klinicysty podczas leczenia pacjenta, zwłaszcza niedawno zaktualizowany algorytm Texas Department of State Health Services dotyczący leczenia MDD (aktualizacja lipiec 2008 r.).17 Jeśli u pacjenta występuje częściowa odpowiedź, klinicyści mogą zdecydować się na zwiększenie dawki, zmianę leku na alternatywny lub podanie kombinacji leków przeciwdepresyjnych. Przeciwnie, jeśli pacjenci nie odpowiadają na leczenie lub nie tolerują leku, zmiana na lek alternatywny jest również wskazana, biorąc pod uwagę, że efekty terapeutyczne pojawią się zwykle między 4 a 6 tygodniem, nawet jeśli działania niepożądane mogą pojawić się po 1 tygodniu leczenia.4,17 Ponadto, chociaż działania niepożądane pojawiają się na początku leczenia, zwykle ustępują po 2 do 3 tygodniach.4,17 Niemniej jednak lek przeciwdepresyjny, który najprawdopodobniej zapewni pacjentowi poprawę i bezpieczeństwo, może być określony, przynajmniej częściowo, metodą prób i błędów. Ze względu na trudności w przewidzeniu, jaki lek będzie zarówno skuteczny, jak i tolerowany przez danego pacjenta, znajomość szerokiego spektrum leków przeciwdepresyjnych jest rozsądna i przydatna.
1. Song F, Freemantle N, Sheldon TA, et al. Selective serotonin reuptake inhibitors: meta-analysis of efficacy and acceptability. BMJ. 1993;306:683-687.
2. Geddes JR, Freemantle N, Mason J, et al. SSRIs versus other antidepressants for depressive disorder. Cochrane Database Syst Rev. 2000;(2):CD001851.
3. Rush AJ, Wisniewski SR, Warden D, et al. Selecting among second-step antidepressant medication monotherapies: predictive value of clinical, demographic, or first-step treatment features. Arch Gen Psychiatry. 2008;65:870-881.
4. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition, Text Revision (DSM-IV-TR). Washington, DC: Amerykańskie Towarzystwo Psychiatryczne; 2000.
5. Grupa Robocza ds. Większego Zaburzenia Depresyjnego. Guideline Watch: Practice Guidelines for the Treatment of Patients with Major Depressive Disorder (Wytyczne postępowania w leczeniu pacjentów z dużym zaburzeniem depresyjnym). 2nd ed. Washington, DC: American Psychiatric Association; 2005.
6. Cain RA. Navigating the Sequenced Treatment Alternatives to Relieve Depression (STAR*D) study: practical outcomes and implications for depression treatment in primary care. Prim Care Clin Office Pract. 2007;34:505-519.
7. Depression. Światowa Organizacja Zdrowia. www.who.int/mental_health/management/depression/definition/en. Dostęp 5 października 2009 r.
8. Dipiro JT, Talbert RL, Yee GC, et al. Pharmacotherapy: A Pathophysiologic Approach. 6th ed. New York, NY: McGraw-Hill; 2005.
9. Zmiany w oznakowaniu produktów. Suicydalność i leki przeciwdepresyjne. FDA. www.fda.gov/downloads/Drugs/DrugSafety/InformationbyDrugClass/UCM173233.pdf. Dostęp 5 października 2009 r.
10. Informacje o lekach. Micromedex Healthcare Series. Greenwood Village, CO: Thomson Micromedex. www.micromedex.com. Dostęp 5 października 2009 r.
11. Shin J-G, Park J-Y, Kim M-J, et al. Inhibitory effects of tricyclic antidepressants on human cytochrome P450 enzymes in vitro: mechanism of drug interaction between TCAs and phenytoin. Drug Metab Dispos. 2002;30:1102-1107.
12. Brown CH. Overview of drug-drug interactions with SSRIs. US Pharm. 2008;33(1):HS3-HS19.
13. Spina E, Scordo MG, D’Arrigo C. Metabolic drug interactions with new psychotropic agents. Fundam Clin Pharmacol. 2003;17:517-538.
14. Bergstrom RF, Peyton AL, Lemberger L. Quantification and mechanism of the fluoxetine and tricyclic antidepressant interaction. Clin Pharmacol Ther. 1992;51:239-248.
15. Cymbalta (chlorowodorek duloksetyny) ulotka dołączona do opakowania. Indianapolis, IN: Eli Lilly and Company; luty 2009. http://pi.lilly.com/us/cymbalta-pi.pdf. Dostęp 5 października 2009 r.
16. Goetz CG, Tanner CM, Klawans HL. Bupropion in Parkinson’s disease. Neurology. 1984;34:1092-1094.
17. Suehs B, Argo TR, Bendele SD, et al. Texas Medication Algorithm Project Procedural Manual. Algorytmy dla dużych zaburzeń depresyjnych. Texas Department of State Health Services; lipiec 2008. www.dshs.state.tx.us/mhprograms/pdf/TIMA_MDD_Manual_080608.pdf. Accessed October 5, 2009.
Aby skomentować ten artykuł, skontaktuj się z [email protected].
.