Vaginose bactérienne
La VB est une infection polymicrobienne, principalement anaérobie, associée à des pertes vaginales accrues parfois à odeur de poisson (figure 1), mais non accompagnées de leucorrhée, de brûlures vulvaires ou de prurit. L’infection à VB peut toutefois avoir des séquelles importantes. Elle a été associée à un risque accru d’avortement septique, de rupture prématurée des membranes amniotiques, de travail prématuré, d’accouchement prématuré, d’endomyométrite post-césarienne et de cellulite pelvienne post-hysterectomie.
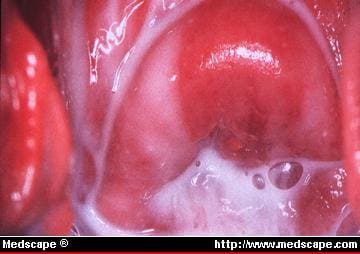
Figure 1. Les pertes vaginales laiteuses ou crémeuses caractéristiques de la vaginose bactérienne sont associées à un pH vaginal élevé et à une odeur de poisson. Figure reproduite avec l’aimable autorisation de James A. McGregor, MD, University of Colorado Health Sciences Center.
Sa présence représente un changement dans l’écosystème vaginal, plus précisément une diminution des lactobacilles, qui font partie de la flore normale, une prolifération des habitants pathogènes du vagin et une élévation du pH (>4,5). En dépit d’une recherche fondamentale exhaustive, on ne sait pas si le déclin des lactobacilles, la prolifération des agents pathogènes ou l’élévation du pH sont à l’origine de la cascade. Si la VB a été décrite à l’origine par Curtis en 1911, elle n’a gagné en notoriété qu’en 1955, après que Gardner et Dukes aient décrit l’organisme incriminé comme étant Haemophilus vaginalis ; l’organisme a depuis été rebaptisé Gardnerella vaginalis en l’honneur de son découvreur. Le terme actuel, vaginose bactérienne, plutôt que vaginite, indique l’absence de réaction inflammatoire (absence de GBM dans les écoulements) et reflète beaucoup mieux la véritable nature polymicrobienne de cette affection.
Bien que la majorité des agents pathogènes responsables de la VB proviennent de la flore endogène, un genre – Mobiluncus – est unique aux patientes atteintes de VB ; il n’a jamais été trouvé chez les patientes sans vaginose. Les Mobiluncus sont des bâtonnets anaérobies en forme de virgule, à Gram variable ou à Gram négatif, aux extrémités effilées, qui utilisent des flagelles subpolaires pour une motilité tumultueuse. G vaginalis est présent chez près de 100 % des femmes présentant des symptômes de VB. En fait, G vaginalis pourrait être l’organisme principalement responsable de la rupture prématurée des membranes chez les femmes atteintes de VB. Cet organisme possède une activité phospholipase A2, qui déclenche le travail. Cependant, d’autres facteurs peuvent également jouer un rôle dans le travail précoce, car le G vaginalis est également présent chez de nombreuses femmes normales dont la grossesse n’est pas compliquée.
La question de savoir si la VB est sexuellement transmissible reste incertaine. La majorité des observations, telles que celles énumérées ci-dessous, suggère que la VB n’est probablement pas sexuellement transmissible.
-
On a observé que les taux de colonisation urétrale des espèces Gardnerella et Mobiluncus chez les partenaires masculins de femmes atteintes de VB ne sont pas plus élevés que chez les partenaires de femmes normales.
-
Il n’a pas été documenté que l’incidence de la VB augmente avec le nombre croissant de partenaires sexuels au cours de la vie.
-
Il n’a pas été démontré que le traitement du partenaire masculin réduisait le risque de récidive chez les femmes (d’où la base de la recommandation actuelle de ne pas traiter le partenaire masculin).
Cependant, une preuve contraire, suggérant un aspect sexuellement transmissible, est que l’utilisation du préservatif est associée à une diminution de l’incidence de la VB chez les partenaires féminins. Par conséquent, si un patient présente des récidives de BV, il y a des raisons de traiter le partenaire.
La vaginose bactérienne identifiée sur un montage humide (figure 2) représente l’infection vaginale la plus courante identifiée chez les femmes présentant une inflammation ou une flore altérée sur le frottis de Papanicolaou.
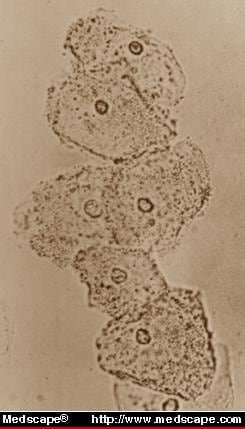
Figure 2. Sur la préparation humide du fluide vaginal, l’absence de GBM et les pointillés des cellules épithéliales soutiennent le diagnostic de vaginose bactérienne. Tiré de Infect Med 9(1):50, 1992. Copyright 1992, SCP Communications, Inc.
Diagnostic. Le diagnostic de la VB requiert la présence d’au moins 3 des 4 critères suivants (tableau I) :
-
Un écoulement homogène non inflammatoire (pas beaucoup de GBM).
-
Phosphore vaginal >4,5.
-
Cellules indicatrices (bactéries fixées aux bords des cellules épithéliales, >20 % des cellules épithéliales ; figure 3).
-
Test humectant positif pour une odeur de poisson ou de moisi lorsqu’une solution alcaline de KOH est ajoutée au frottis.
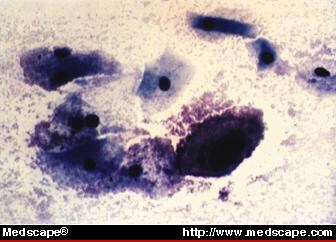
Figure 3. Frottis montrant des cellules clues compatibles avec une vaginose bactérienne. Avec l’aimable autorisation d’Abner P. Korn, MD. © Copyright 1996, SCP Communications, Inc.
L’application de ces critères diagnostiques permettra de diagnostiquer correctement la VB dans plus de 90 % des cas, avec un taux de faux positifs inférieur à 10 %. Il convient de noter que ni le frottis de Papanicolaou ni la culture ne constituent un diagnostic en soi. Le frottis de Papanicolaou peut indiquer un déplacement de la flore coccobacillaire, mais ce rapport doit inciter la patiente à évaluer les critères diagnostiques formels plutôt qu’à suivre un traitement empirique. La culture n’est pas utile puisque la flore de la BV est largement dérivée de la flore commensale normale.
Traitement. Pendant des années, le métronidazole oral a été le principal régime indiqué. Bien que très efficace, ce traitement comporte des effets secondaires graves tels que des crises convulsives et une neuropathie périphérique, ce qui amène de nombreux patients à interrompre leur traitement avant la fin de la période de 7 jours. D’autres options systémiques incluent la clindamycine par voie orale. Plus récemment, l’avènement des préparations intravaginales a offert des options topiques qui entraînent moins d’effets systémiques indésirables. La quantité de médicament absorbée et délivrée est également beaucoup plus faible. Par exemple, le métronidazole nécessite une dose orale de 500 mg, alors que seulement 37,5 mg de gel intravaginal de métronidazole sont nécessaires pour atteindre des niveaux thérapeutiques dans les tissus vaginaux. De même, les préparations orales et intravaginales de clindamycine atteignent une efficacité égale, bien qu’une dose plus faible soit délivrée par voie intravaginale.
Bien qu’il ait été démontré que les schémas thérapeutiques énumérés au tableau II offrent une efficacité de 90 % ou plus, la dose unique de 2 g de métronidazole n’offre qu’une efficacité de 70 % et entraîne plus d’effets indésirables gastro-intestinaux que la clindamycine. Le régime oral de la clindamycine est associé à une incidence plus élevée de diarrhée que le métronidazole oral. Il y a une dizaine d’années, l’ampicilline était traditionnellement approuvée comme traitement de première intention de la VB pendant la grossesse ; toutefois, cette conclusion était fondée davantage sur des préoccupations de sécurité que sur l’efficacité. Compte tenu des données plus récentes suggérant que la VB est associée à des issues obstétricales plus graves, un traitement plus efficace est justifié. Il a été démontré que le métronidazole oral, seul ou en association avec l’érythromycine orale, réduit les séquelles obstétricales indésirables chez les patientes à haut risque atteintes de VB. La crème à la clindamycine, tout en traitant efficacement la VB, a été associée, selon les critères d’Amsel, à de plus mauvaises issues obstétriques. Ce paradoxe peut s’expliquer par le fait que la clindamycine réduit la population de lactobacilles endogènes ou par la prolifération d’Escherichia coli et d’Enterococcus. Malgré l’opinion commune, des études exhaustives n’ont pas montré que le métronidazole était tératogène. Il est mutagène chez les bactéries et cancérigène chez les rongeurs, mais aucune donnée humaine n’a mis en évidence des effets indésirables lorsqu’elle a été soumise à un examen analytique. Cependant, plusieurs sources, bien que sans données probantes, affirment que le métronidazole est contre-indiqué au cours du premier trimestre de la grossesse.