Generisk navn: Neomycin sulfat, polymyxin b sulfat og hydrokortison
Doseringsform: Ophthalmisk suspension
Medicinsk gennemgået af Lægemidler.com. Sidst opdateret den 1. marts 2020.
- Overblik
- Bivirkninger
- Dosering
- Professionel
- Interaktioner
- Mere
Kun på recept
BESKRIVELSE
Neomycin og polymyxin B-sulfater og hydrokortison øjensuspension er en steril antimikrobiel og antiinflammatorisk suspension til oftalmisk brug.
Hver mL indeholder: Aktivstoffer: neomycinsulfat (svarende til 3,5 mg neomycinbase), polymyxin B-sulfat svarende til 10.000 polymyxin B-enheder og hydrokortison 10 mg (1%). Konserveringsmiddel: thimerosal 0,001 %. Inaktive stoffer: cetylalkohol, glycerylmonostearat, mineralolie, polyoxyl 40 stearat, propylenglycol, svovlsyre (til justering af pH) og vand til injektion.
Neomycinsulfat er sulfatsaltet af neomycin B og C, som produceres ved vækst af Streptomyces fradiae Waksman (Fam. Streptomycetacae). Det har en styrke svarende til ikke mindre end 600 μg neomycin standard pr. mg, beregnet på vandfri basis. Dens strukturformel er:
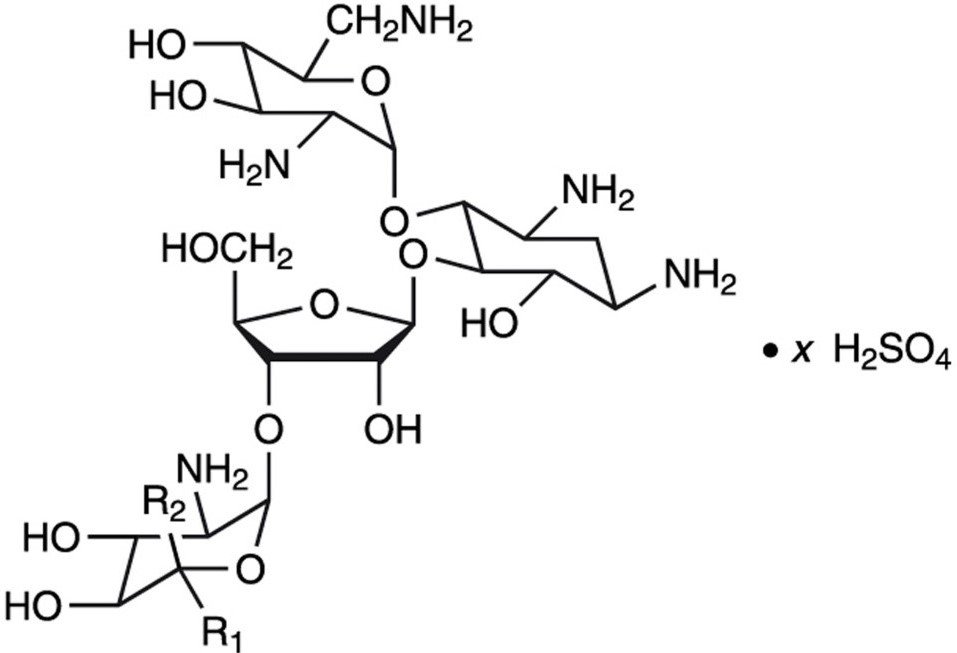
Neomycin B (R1=H, R2=CH2NH2)
Neomycin C (R1=CH2NH2, R2=H)
Polymyxin B sulfat er sulfatsaltet af Polymyxin, B1 og B2, som produceres ved vækst af Bacillus polymyxa (Prazmowski) Migula (Fam. Bacillaceae). Det har en styrke på ikke mindre end 6 000 polymyxin B-enheder pr. mg beregnet på vandfri basis. Dens strukturformel er:
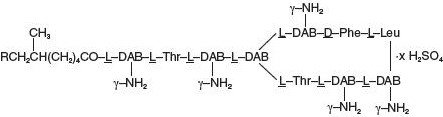

Hydrocortison, 11β, 17, 21-trihydroxypregn-4-ene-3, 20 dione, er et antiinflammatorisk hormon. Dens strukturformel er:
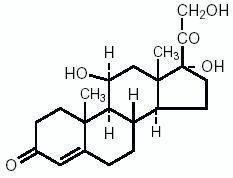
Neomycin, Polymyxin B, Hydrocortison Ophthalmic Suspension – Klinisk Farmakologi
Cortikosteroider undertrykker det inflammatoriske respons på en række stoffer, og de forsinker eller forsinker sandsynligvis helingen. Da kortikosteroider kan hæmme kroppens forsvarsmekanisme mod infektion, kan der anvendes sideløbende antimikrobielle lægemidler, når denne hæmning anses for at være klinisk betydningsfuld i et bestemt tilfælde.
Når det besluttes at administrere både et kortikosteroid og antimikrobielle lægemidler, har administration af sådanne lægemidler i kombination den fordel, at patienten i højere grad overholder reglerne og er mere bekvem, og der er desuden sikkerhed for, at den rette dosis af alle lægemidlerne bliver administreret. Når hver type lægemiddel er i samme formulering, er ingrediensernes kompatibilitet sikret, og den korrekte mængde af lægemidlet afgives og bevares.
Den relative styrke af kortikosteroider afhænger af den molekylære struktur, koncentration og frigivelse fra bærestoffet.
Mikrobiologi
De anti-infektiøse komponenter i Neomycin og Polymyxin B-sulfater og Hydrocortison oftalmisk suspension er inkluderet for at virke mod specifikke organismer, der er modtagelige herfor. Neomycinsulfat og polymyxin B-sulfat er in vitro aktive mod modtagelige stammer af følgende mikroorganismer: Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, Klebsiella/Enterobacter-arter, Neisseria-arter og Pseudomonas aeruginosa. Produktet giver ikke tilstrækkelig dækning mod Serratia marcescens og streptokokker, herunder Streptococcus pneumoniae .
Indikationer og anvendelse for Neomycin, Polymyxin B, Hydrocortison Ophthalmisk Suspension
Neomycin og Polymyxin B Sulfater og Hydrocortison Ophthalmisk Suspension er indiceret til steroidresponsive inflammatoriske okulære tilstande, hvor et kortikosteroid er indiceret, og hvor der er bakteriel infektion eller risiko for bakteriel okulær infektion.
Okulære kortikosteroider er indiceret ved inflammatoriske tilstande i den palpebrale og bulbære conjunctiva, cornea og det forreste segment af kloden, hvor den iboende risiko ved brug af kortikosteroider ved visse infektiøse konjunktivitider accepteres for at opnå en reduktion af ødem og inflammation. De er også indiceret ved kronisk anterior uveitis og cornealskader fra kemiske, strålings- eller termiske forbrændinger eller indtrængen af fremmedlegemer.
Brug af et kombinationslægemiddel med en anti-infektiøs komponent er indiceret, hvor risikoen for infektion er høj, eller hvor der er en forventning om, at der vil være et potentielt farligt antal bakterier til stede i øjet.
De særlige anti-infektiøse lægemidler i dette produkt er aktive mod følgende almindelige bakterielle øjenpatogener: Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, Klebsiella/Enterobacter-arter, Neisseria-arter og Pseudomonas aeruginosa.
Produktet giver ikke tilstrækkelig dækning mod Serratia marcescens og streptokokker, herunder Streptococcus pneumoniae.
Kontraindikationer
Neomycin og polymyxin B-sulfater og hydrokortison oftalmisk suspension er kontraindiceret ved de fleste virussygdomme i cornea og konjunktiva, herunder: epithelial herpes simplex keratitis (dendritisk keratitis), vaccinia og varicella, samt ved mykobakteriel infektion i øjet og svampesygdomme i okulære strukturer.
Neomycin og polymyxin B-sulfater og hydrokortison oftalmisk suspension er også kontraindiceret hos personer, der har vist overfølsomhed over for nogen af dets bestanddele. Overfølsomhed over for den antibiotiske komponent forekommer i højere grad end for de andre komponenter.
Varsler
IKKE TIL INJEKTION I ØJET. Neomycin- og polymyxin B-sulfater og hydrokortison øjensuspension må aldrig indføres direkte i øjets forreste kammer.
Langvarig brug af kortikosteroider kan resultere i okulær hypertension og/eller glaukom med skader på synsnerven, defekter i synsstyrke og synsfelt og dannelse af posterior subkapsulær katarakt.
Langvarig brug kan undertrykke værtsresponset og dermed øge risikoen for sekundære okulære infektioner. Ved de sygdomme, der forårsager udtynding af cornea eller sclera, er det kendt, at der er opstået perforationer ved brug af topiske kortikosteroider. Ved akut purulent tilstand i øjet kan kortikosteroider maskere infektion eller forstærke eksisterende infektion.
Hvis disse produkter anvendes i 10 dage eller længere, bør det intraokulære tryk rutinemæssigt overvåges, selv om det kan være vanskeligt hos ikke-samarbejdsvillige patienter. Kortikosteroider bør anvendes med forsigtighed ved tilstedeværelse af glaukom.
Brug af kortikosteroider efter kataraktoperation kan forsinke helingen og øge forekomsten af filtrerende blærer. Brug af okulære kortikosteroider kan forlænge forløbet og kan forværre sværhedsgraden af mange virale infektioner i øjet (herunder herpes simplex). Anvendelse af kortikosteroidmedicin til behandling af herpes simplex kræver stor forsigtighed.
Topiske antibiotika, især neomycinsulfat, kan forårsage kutan sensibilisering. En præcis forekomst af overfølsomhedsreaktioner (primært hududslæt) som følge af topiske antibiotika er ikke kendt. Manifestationerne af sensibilisering over for topiske antibiotika er normalt kløe, rødme og ødemer i konjunktiva og øjenlåg. En sensibiliseringsreaktion kan blot manifestere sig som en manglende heling. Ved langvarig brug af topiske antibiotika anbefales det at foretage regelmæssig undersøgelse for sådanne tegn, og patienten bør informeres om at afbryde brugen af produktet, hvis de observeres. Symptomerne aftager normalt hurtigt ved ophør af medicinen. Anvendelse af produkter, der indeholder disse ingredienser, bør undgås for patienten derefter.
Forholdsregler
Almen
Den første ordination og fornyelse af medicineringsordren ud over 20 ml bør kun foretages af en læge efter undersøgelse af patienten ved hjælp af forstørrelse, såsom spaltlampe-biomikroskopi og, hvor det er relevant, fluoresceinfarvning. Hvis tegn og symptomer ikke forbedres efter 2 dage, bør patienten revurderes.
Muligheden af svampeinfektioner i cornea bør overvejes efter langvarig kortikosteroiddosering. Der skal tages svampekulturer, når det er relevant.
Hvis dette produkt anvendes i 10 dage eller længere, skal det intraokulære tryk overvåges.
Der har været rapporteret om bakteriel keratitis i forbindelse med brug af aktuelle oftalmiske produkter i beholdere med flere doser, som utilsigtet er blevet forurenet af patienter, hvoraf de fleste havde en samtidig corneasygdom eller en forstyrrelse af den okulære epiteloverflade .
Der kan forekomme allergiske krydsreaktioner, som kan forhindre brugen af nogle af eller alle følgende antibiotika til behandling af fremtidige infektioner: kanamycin, paromomycin, streptomycin og muligvis gentamicin.
Informationer til patienter
Patienterne skal instrueres om at undgå at lade spidsen af dispenseringsbeholderen komme i kontakt med øjet, øjenlåget, fingrene eller andre overflader. Brug af dette produkt af mere end én person kan sprede infektion.
Patienterne skal også instrueres om, at okulære produkter, hvis de håndteres forkert, kan blive kontamineret af almindelige bakterier, der er kendt for at forårsage okulære infektioner. Alvorlig skade på øjet og efterfølgende tab af synet kan opstå ved brug af kontaminerede produkter.
Hvis tilstanden fortsætter eller forværres, eller hvis der opstår udslæt eller en allergisk reaktion, skal patienten rådes til at stoppe brugen og konsultere en læge. Brug ikke dette produkt, hvis du er allergisk over for nogen af de anførte ingredienser.
Hold det tæt lukket, når det ikke er i brug. Opbevares uden for børns rækkevidde.
Carcinogenese, mutagenese, forringet fertilitet
Langtidsundersøgelser på dyr til vurdering af det carcinogene eller mutagene potentiale er ikke blevet udført med polymyxin B sulfat. Behandling af dyrkede humane lymfocytter in vitro med neomycin øgede hyppigheden af kromosomaberrationer ved de højeste testede koncentrationer (80 ug/mL); virkningerne af neomycin på carcinogenese og mutagenese hos mennesker er imidlertid ukendte.
Langtidsundersøgelser på dyr (rotter, kaniner, mus) viste ingen tegn på carcinogenicitet eller mutagenicitet, der kan tilskrives oral indgift af kortikosteroider. Der er ikke udført langtidsforsøg på dyr for at vurdere det carcinogene potentiale af topiske kortikosteroider. Undersøgelser til bestemmelse af mutagenicitet med hydrocortison har givet negative resultater. Anvendelse af kortikosteroidmedicin i forbindelse med behandling af herpes simplex kræver stor forsigtighed. Polymyxin B er blevet rapporteret til at forringe motiliteten af hestens sædceller, men dets virkninger på mandlig eller kvindelig fertilitet er ukendt. Der er ikke udført langtidsforsøg på dyr for at vurdere virkningen på fertiliteten af topiske kortikosteroider.
Graviditet
Teratogene virkninger
Graviditetskategori C. Kortikosteroider har vist sig at være teratogene hos kaniner, når de anvendes topisk i koncentrationer på 0,5 % på dag 6-18 i drægtighedsperioden og hos mus, når de anvendes topisk i en koncentration på 15 % på dag 10-13 i drægtighedsperioden. Der findes ingen tilstrækkelige og velkontrollerede undersøgelser på gravide kvinder. Neomycin- og polymyxin B-sulfater og hydrokortison øjensuspension bør kun anvendes under graviditet, hvis den potentielle fordel retfærdiggør den potentielle risiko for fosteret.
Sygeplejersker
Det vides ikke, om topisk indgift af kortikosteroider kan resultere i tilstrækkelig systemisk absorption til at producere påviselige mængder i modermælk. Systemisk administrerede kortikosteroider forekommer i modermælk og kan undertrykke væksten, forstyrre den endogene kortikosteroidproduktion eller forårsage andre uheldige virkninger. På grund af potentialet for alvorlige bivirkninger hos ammende spædbørn fra Neomycin og Polymyxin B Sulfater og Hydrocortison Ophthalmisk Suspension bør der træffes en beslutning om at afbryde amningen eller ophøre med lægemidlet under hensyntagen til lægemidlets betydning for moderen.
Pædiatrisk brug
Sikkerheden og effektiviteten hos pædiatriske patienter er ikke blevet fastslået.
Geriatrisk brug
Der er ikke observeret nogen overordnede forskelle i sikkerhed eller effektivitet mellem ældre og yngre patienter.
Bivirkninger
Bivirkninger er forekommet med kortikosteroid/antiinfektiøse kombinationslægemidler, som kan tilskrives kortikosteroidkomponenten, den anti-infektiøse komponent eller kombinationen. Den nøjagtige incidens er ikke kendt.
Reaktioner, der oftest forekommer som følge af tilstedeværelsen af den anti-infektiøse bestanddel, er allergiske sensibiliseringsreaktioner, herunder kløe, hævelse og konjunktivalt erytem . Mere alvorlige overfølsomhedsreaktioner, herunder anafylaksi, er sjældent blevet rapporteret.
Reaktionerne som følge af kortikosteroidkomponenten er i faldende rækkefølge efter hyppighed: forhøjelse af det intraokulære tryk (IOP) med mulig udvikling af glaukom og sjældent skader på synsnerven; posteriore subkapsulær kataraktdannelse; og forsinket sårheling.
Sekundær infektion
Der er opstået sekundær infektion efter brug af kombinationer, der indeholder kortikosteroider og antimikrobielle stoffer. Svampe- og virusinfektioner i cornea er særligt tilbøjelige til at udvikle sig sammenfaldende med langvarig anvendelse af et kortikosteroid. Muligheden for svampeinvasion skal overvejes ved enhver vedvarende cornea-sulceration, hvor der har været anvendt kortikosteroidbehandling.
Lokal irritation ved instillation er også blevet rapporteret.
For at rapportere FORSÆTTE ADVERSE REAKTIONER skal du kontakte Sandoz Inc. på 1-800-525-8747 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
DOSERING OG ADMINISTRATION
Et eller to dråber i det berørte øje hver 3. eller 4. time, afhængigt af tilstandens sværhedsgrad. Suspensionen kan anvendes hyppigere om nødvendigt.
Der bør ikke ordineres mere end 20 mL i første omgang, og recepten bør ikke genopfyldes uden yderligere evaluering som beskrevet i FORSKNINGSANVISNINGER ovenfor.
Hvordan leveres
Neomycin- og polymyxin B-sulfater og hydrokortison øjensuspension fås i en flaske med 7,5 mL. NDC 61314-641-75
VARMER VEL INDEN BRUG.
Lagres ved 20° til 25°C (68° til 77°F).
Fremstillet af
Alcon Laboratories, Inc.
Fort Worth, Texas 76134 for
Sandoz Inc.
Princeton, NJ 08540
Rev. Juni 2020
PRINCIPAL DISPLAY PANEL
NDC 61314-641-75
Neomycin og
Polymyxin B Sulfater
og Hydrocortison
Ophthalmisk
Suspension, USP
KUN TIL TOPISK OPHTHALMISK ANVENDELSE
Kun på recept
STERILE
7.5 mL
SANDOZ
| NEOMYCIN OG POLYMYXIN B SULFATER OG HYDROCORTISON neomycinsulfat, polymyxin b sulfat og hydrokortison suspension |
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
|
|||||||||||||||||||||||
Mærkningssted – Sandoz Inc (005387188)
Mere om hydrocortison / neomycin / polymyxin b oftalmisk
- Bivirkninger
- Under graviditet
- Doseringsinformation
- Medikamentinteraktioner
- Priser & Kuponer
- En Español
- 1 anmeldelse
- Lægemiddelklasse: oftalmiske steroider med anti-infektiøse midler
Forbrugerressourcer
- Patientinformation
- Neomycin, polymyxin b, og hydrokortison oftalmisk (Avanceret læsning)
Faglige ressourcer
- Receptinformation
Andre mærker Cortisporin Ophthalmic Suspension
Relaterede behandlingsvejledninger
- Konjunktivitis, Bakteriel
- Blepharitis
- Keratitis
- Keratokonjunktivitis
- Uveitis
Medicinsk ansvarsfraskrivelse