Nome generico: neomicina solfato, polimixina b solfato e idrocortisone
Forma di dosaggio: sospensione oftalmica
Medicamente rivisto da Drugs.com. Ultimo aggiornamento il 1 marzo 2020.
- Panoramica
- Effetti collaterali
- Dosaggio
- Professionale
- Interazioni
- Altro
Solo Rx
DESCRIZIONE
Neomicina e polimixina B solfati e idrocortisone in sospensione oftalmica è una sospensione sterile antimicrobica e antinfiammatoriainfiammatoria per uso oftalmico.
Ogni mL contiene: Attivi: neomicina solfato (equivalente a 3,5 mg di neomicina base), polimixina B solfato equivalente a 10.000 unità di polimixina B e idrocortisone 10 mg (1%). Conservante: thimerosal 0,001%. Inattivi: alcool cetilico, gliceril monostearato, olio minerale, poliossile 40 stearato, glicole propilenico, acido solforico (per regolare il pH) e acqua per iniezione.
La neomicina solfato è il sale solfato della neomicina B e C, che sono prodotti dalla crescita di Streptomyces fradiae Waksman (Fam. Streptomycetacae). Ha una potenza equivalente a non meno di 600 μg di neomicina standard per mg, calcolata su base anidra. La sua formula strutturale è:
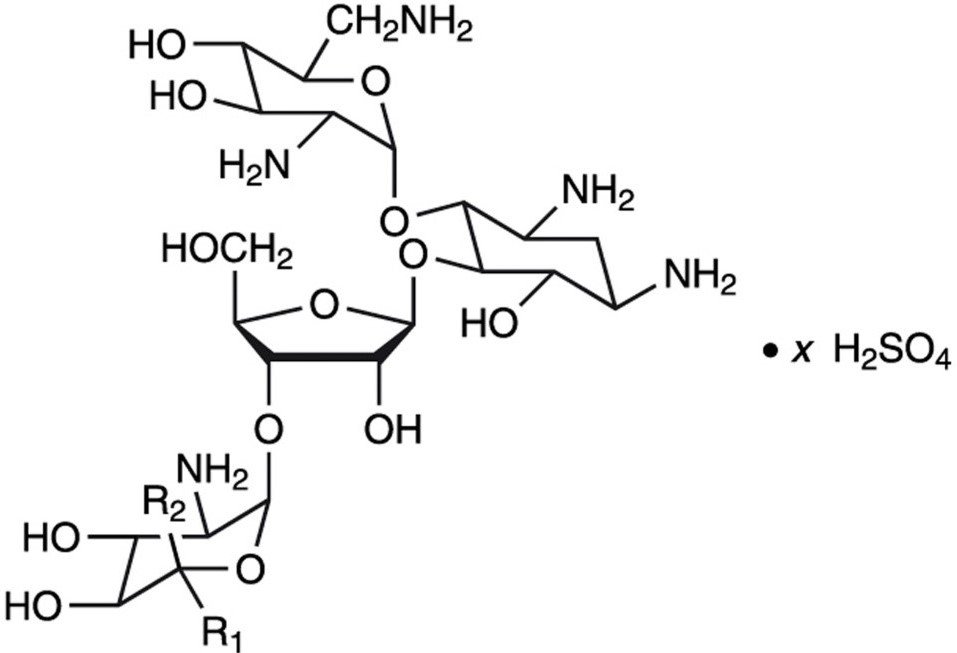
Neomicina B (R1=H, R2=CH2NH2)
Neomicina C (R1=CH2NH2, R2=H)
Polymyxin B solfato è il sale solfato di Polymyxin, B1 e B2, che sono prodotti dalla crescita di Bacillus polymyxa (Prazmowski) Migula (Fam. Bacillaceae). Ha una potenza non inferiore a 6.000 unità di polimixina B per mg calcolato su base anidra. La sua formula strutturale è:
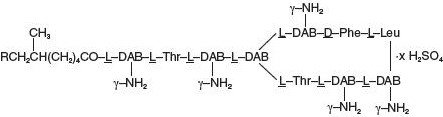

L’idrocortisone, 11β, 17, 21-triidrossipregn-4-ene-3, 20 dione, è un ormone antinfiammatorio. La sua formula strutturale è:
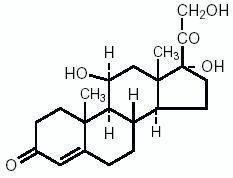
Neomycin, Polymyxin B, Hydrocortisone Ophthalmic Suspension – Clinical Pharmacology
I corticosteroidi sopprimono la risposta infiammatoria ad una varietà di agenti, e probabilmente ritardano o rallentano la guarigione. Poiché i corticosteroidi possono inibire il meccanismo di difesa del corpo contro le infezioni, i farmaci antimicrobici concomitanti possono essere utilizzati quando questa inibizione è considerata clinicamente significativa in un caso particolare.
Quando si decide di somministrare sia un corticosteroide che degli antimicrobici, la somministrazione di tali farmaci in combinazione ha il vantaggio di una maggiore conformità e convenienza del paziente, con l’ulteriore garanzia che venga somministrato il dosaggio appropriato di tutti i farmaci. Quando ogni tipo di farmaco è nella stessa formulazione, la compatibilità degli ingredienti è assicurata e il corretto volume di farmaco è consegnato e trattenuto.
La potenza relativa dei corticosteroidi dipende dalla struttura molecolare, dalla concentrazione e dal rilascio dal veicolo.
Microbiologia
I componenti anti-infettivi in Neomicina e polimixina B solfati e idrocortisone sospensione oftalmica sono inclusi per fornire azione contro specifici organismi suscettibili ad essa. Neomicina solfato e polimixina B solfato sono attivi in vitro contro i ceppi suscettibili dei seguenti microrganismi: Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, specie Klebsiella/Enterobacter, specie Neisseria e Pseudomonas aeruginosa. Il prodotto non fornisce una copertura adeguata contro Serratia marcescens e streptococchi, incluso Streptococcus pneumoniae.
Indicazioni e uso per Neomycin, Polymyxin B, Hydrocortisone Ophthalmic Suspension
Neomycin and Polymyxin B Sulfates and Hydrocortisone Ophthalmic Suspension è indicato per condizioni infiammatorie oculari steroido-responsive per le quali è indicato un corticosteroide e dove esiste infezione batterica o un rischio di infezione oculare batterica.
I corticosteroidi oculari sono indicati nelle condizioni infiammatorie della congiuntiva palpebrale e bulbare, della cornea e del segmento anteriore del globo dove il rischio inerente all’uso di corticosteroidi in alcune congiuntiviti infettive è accettato per ottenere una diminuzione dell’edema e dell’infiammazione. Sono anche indicati nell’uveite anteriore cronica e nelle lesioni corneali da ustioni chimiche, da radiazioni o termiche, o dalla penetrazione di corpi estranei.
L’uso di un farmaco combinato con un componente anti-infettivo è indicato dove il rischio di infezione è alto o dove ci si aspetta che un numero potenzialmente pericoloso di batteri sia presente nell’occhio.
I particolari farmaci anti-infettivi in questo prodotto sono attivi contro i seguenti patogeni oculari batterici comuni: Staphylococcus aureus, Escherichia coli, Haemophilus influenzae, specie Klebsiella/Enterobacter, specie Neisseria e Pseudomonas aeruginosa.
Il prodotto non fornisce una copertura adeguata contro Serratia marcescens e streptococchi, incluso Streptococcus pneumoniae.
Contraindicazioni
Neomicina e Polimixina B Solfati e Idrocortisone Sospensione Oftalmica è controindicata nella maggior parte delle malattie virali della cornea e della congiuntiva tra cui: cheratite epiteliale da herpes simplex (cheratite dendritica), vaccinia e varicella, e anche nelle infezioni micobatteriche dell’occhio e nelle malattie fungine delle strutture oculari.
Neomicina e polimixina B solfati e idrocortisone sospensione oftalmica è anche controindicato in individui che hanno mostrato ipersensibilità a uno qualsiasi dei suoi componenti. L’ipersensibilità al componente antibiotico si verifica ad un tasso più alto che per altri componenti.
Avvertenze
NON PER L’INIEZIONE NEGLI OCCHI. Neomicina e polimixina B solfati e idrocortisone sospensione oftalmica non devono mai essere introdotti direttamente nella camera anteriore dell’occhio.
L’uso prolungato di corticosteroidi può provocare ipertensione oculare e/o glaucoma, con danni al nervo ottico, difetti dell’acuità visiva e del campo visivo e formazione di cataratta subcapsulare posteriore.
L’uso prolungato può sopprimere la risposta dell’ospite e quindi aumentare il rischio di infezioni oculari secondarie. In quelle malattie che causano assottigliamento della cornea o della sclera, si sono verificate perforazioni con l’uso di corticosteroidi topici. In condizioni purulente acute dell’occhio, i corticosteroidi possono mascherare l’infezione o migliorare l’infezione esistente.
Se questi prodotti sono usati per 10 giorni o più, la pressione intraoculare dovrebbe essere monitorata di routine anche se può essere difficile in pazienti non cooperativi. I corticosteroidi devono essere usati con cautela in presenza di glaucoma.
L’uso di corticosteroidi dopo un intervento di cataratta può ritardare la guarigione e aumentare l’incidenza di blebs filtranti. L’uso di corticosteroidi oculari può prolungare il corso e può esacerbare la gravità di molte infezioni virali dell’occhio (incluso l’herpes simplex). L’impiego di farmaci corticosteroidi nel trattamento dell’herpes simplex richiede grande cautela.
Gli antibiotici topici, in particolare il solfato di neomicina, possono causare sensibilizzazione cutanea. Un’incidenza precisa delle reazioni di ipersensibilità (principalmente eruzione cutanea) dovute agli antibiotici topici non è nota. Le manifestazioni di sensibilizzazione agli antibiotici topici sono di solito prurito, arrossamento ed edema della congiuntiva e della palpebra. Una reazione di sensibilizzazione può manifestarsi semplicemente come una mancata guarigione. Durante l’uso a lungo termine di prodotti antibiotici topici, è consigliabile un esame periodico per questi segni, e al paziente dovrebbe essere detto di sospendere il prodotto se si osservano. I sintomi di solito si placano rapidamente quando si ritira il farmaco. L’applicazione di prodotti contenenti questi ingredienti dovrebbe essere evitata per il paziente in seguito.
Precauzioni
Generale
La prescrizione iniziale e il rinnovo dell’ordine del farmaco oltre i 20 mL dovrebbe essere fatto da un medico solo dopo l’esame del paziente con l’aiuto dell’ingrandimento, come la lampada a fessura biomicroscopia e, se del caso, la colorazione con fluoresceina. Se i segni e i sintomi non migliorano dopo 2 giorni, il paziente deve essere rivalutato.
La possibilità di infezioni fungine della cornea deve essere considerata dopo un dosaggio prolungato di corticosteroidi. Se questo prodotto viene usato per 10 giorni o più, la pressione intraoculare deve essere monitorata.
Sono stati riportati casi di cheratite batterica associati all’uso di prodotti oftalmici topici in contenitori a dosi multiple che sono stati inavvertitamente contaminati dai pazienti, la maggior parte dei quali aveva una malattia corneale concomitante o un’alterazione della superficie epiteliale oculare.
Possono verificarsi reazioni incrociate allergiche che potrebbero impedire l’uso di uno o tutti i seguenti antibiotici per il trattamento di infezioni future: kanamicina, paromomicina, streptomicina e possibilmente gentamicina.
Informazioni per i pazienti
I pazienti devono essere istruiti ad evitare che la punta del contenitore di erogazione venga a contatto con l’occhio, la palpebra, le dita o qualsiasi altra superficie. L’uso di questo prodotto da parte di più di una persona può diffondere l’infezione.
I pazienti devono anche essere istruiti sul fatto che i prodotti oculari, se manipolati in modo improprio, possono essere contaminati da batteri comuni noti per causare infezioni oculari. L’uso di prodotti contaminati può causare gravi danni agli occhi e la conseguente perdita della vista.
Se la condizione persiste o peggiora, o se si sviluppa un’eruzione cutanea o una reazione allergica, al paziente deve essere consigliato di interrompere l’uso e consultare un medico. Non usare questo prodotto se si è allergici a uno qualsiasi degli ingredienti elencati.
Tenere ben chiuso quando non si usa. Tenere fuori dalla portata dei bambini.
Carcinogenesi, mutagenesi, compromissione della fertilità
Studi a lungo termine sugli animali per valutare il potenziale cancerogeno o mutageno non sono stati condotti con polimixina B solfato. Il trattamento di linfociti umani coltivati in vitro con neomicina ha aumentato la frequenza di aberrazioni cromosomiche alle più alte concentrazioni (80 ug/mL) testate; tuttavia, gli effetti della neomicina sulla carcinogenesi e la mutagenesi negli esseri umani sono sconosciuti.
Studi a lungo termine negli animali (ratti, conigli, topi) non hanno mostrato alcuna evidenza di carcinogenicità o mutagenicità attribuibile alla somministrazione orale di corticosteroidi. Non sono stati eseguiti studi a lungo termine sugli animali per valutare il potenziale cancerogeno dei corticosteroidi topici. Gli studi per determinare la mutagenicità con l’idrocortisone hanno rivelato risultati negativi. L’uso di farmaci corticosteroidi nel trattamento dell’herpes simplex richiede grande cautela. È stato riportato che la polimixina B compromette la motilità dello sperma equino, ma i suoi effetti sulla fertilità maschile o femminile sono sconosciuti. Non sono stati eseguiti studi a lungo termine sugli animali per valutare l’effetto sulla fertilità dei corticosteroidi topici.
Gravidanza
Effetti teratogeni
Categoria di gravidanza C. I corticosteroidi sono risultati teratogeni nei conigli quando applicati topicamente a concentrazioni dello 0,5% nei giorni 6 -18 di gestazione e nei topi quando applicati topicamente a una concentrazione del 15% nei giorni 10 -13 di gestazione. Non ci sono studi adeguati e ben controllati in donne incinte. Neomicina e polimixina B solfati e idrocortisone sospensione oftalmica devono essere usati durante la gravidanza solo se il potenziale beneficio giustifica il potenziale rischio per il feto.
Madri che allattano
Non è noto se la somministrazione topica di corticosteroidi possa comportare un assorbimento sistemico sufficiente a produrre quantità rilevabili nel latte umano. I corticosteroidi somministrati per via sistemica appaiono nel latte umano e potrebbero sopprimere la crescita, interferire con la produzione endogena di corticosteroidi o causare altri effetti negativi. A causa del potenziale di gravi reazioni avverse nei neonati che allattano da Neomicina e Polimixina B Solfati e Idrocortisone Sospensione Oftalmica, deve essere presa una decisione se interrompere l’allattamento o interrompere il farmaco, tenendo conto dell’importanza del farmaco per la madre.
Uso pediatrico
Sicurezza ed efficacia in pazienti pediatrici non sono state stabilite.
Uso geriatrico
Non sono state osservate differenze complessive nella sicurezza o nell’efficacia tra pazienti anziani e giovani.
Reazioni avverse
Con i farmaci di combinazione corticosteroidi/anti-infettivi si sono verificate reazioni avverse che possono essere attribuite alla componente corticosteroide, alla componente anti-infettiva o alla combinazione. L’esatta incidenza non è nota.
Le reazioni che si verificano più spesso dalla presenza dell’ingrediente anti-infettivo sono reazioni di sensibilizzazione allergica che includono prurito, gonfiore ed eritema congiuntivale. Reazioni di ipersensibilità più gravi, compresa l’anafilassi, sono state riportate raramente.
Le reazioni dovute alla componente corticosteroidea in ordine decrescente di frequenza sono: aumento della pressione intraoculare (IOP) con possibile sviluppo di glaucoma, e danni al nervo ottico non frequenti; formazione di cataratta subcapsulare posteriore; e ritardata guarigione della ferita.
Infezione secondaria
Lo sviluppo di un’infezione secondaria si è verificato dopo l’uso di combinazioni contenenti corticosteroidi e antimicrobici. Le infezioni fungine e virali della cornea sono particolarmente inclini a svilupparsi in coincidenza con applicazioni a lungo termine di un corticosteroide. La possibilità di un’invasione fungina deve essere considerata in qualsiasi ulcerazione corneale persistente in cui sia stato utilizzato un trattamento con corticosteroidi.
Sono state inoltre riportate irritazioni locali all’instillazione.
Per segnalare SOSPETTE REAZIONI AVVERSE, contattare Sandoz Inc. al 1-800-525-8747 o la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch.
DOSAGGIO E AMMINISTRAZIONE
Una o due gocce nell’occhio interessato ogni 3 o 4 ore, a seconda della gravità della condizione. La sospensione può essere usata più frequentemente se necessario.
Non devono essere prescritti inizialmente più di 20 mL e la prescrizione non deve essere rinnovata senza un’ulteriore valutazione come indicato nelle PRECAUZIONI di cui sopra.
Come viene fornito
Neomicina e polimixina B solfati e idrocortisone sospensione oftalmica è disponibile in un flacone contenente 7,5 mL. NDC 61314-641-75
AVVOLGERE BENE PRIMA DELL’USO.
Conservare a 20°-25°C (68°-77°F).
Prodotto da
Alcon Laboratories, Inc.
Fort Worth, Texas 76134 per
Sandoz Inc.
Princeton, NJ 08540
Rev. Giugno 2020
Pannello di esposizione principale
NDC 61314-641-75
Neomicina e
Polimixina B solfati
e idrocortisone
Oftalmico
Sospensione, USP
SOLO PER USO OFTALMICO TOPICO
Solo Rx
STERILE
7.5 mL
SANDOZ
| SOLFATI DI NEOMICINA E POLIMIXINA B E IDROCORTISONE Solfato di neomicina, polimixina b solfato e idrocortisone sospensione |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Etichettatore – Sandoz Inc (005387188)
Più informazioni su idrocortisone / neomicina / polimixina b oftalmica
- Effetti collaterali
- Durante la gravidanza
- Informazioni sul dosaggio
- Interazioni farmacologiche
- Prezzi &Coupon
- En Español
- 1 Recensione
- Classe del farmaco: steroidi oftalmici con antinfettivi
Risorse per i consumatori
- Informazioni per i pazienti
- Neomicina, polimixina b, and hydrocortisone Ophthalmic (Advanced Reading)
Risorse professionali
- Informazioni per il paziente
Altre marche Cortisporin Ophthalmic Suspension
Guide correlate al trattamento
- Congiuntivite, Batterica
- Blefarite
- Ceratite
- Ceratocongiuntivite
- Uveite
Discorso medico