Palabras clave
Endosonografía; tumores neuroendocrinos; pancreatectomía
Abreviaturas
HDRBC: glóbulo rojo dañado por el calor; IPAS: bazo accesorio intrapancreático; PTI: púrpura trombocitopénica idiopática; SPECT: tomografía computarizada por emisión de fotón único; SPIO: óxido de hierro superparamagnético
INTRODUCCIÓN
El tejido esplénico accesorio ectópico puede encontrarse en cualquier lugar a lo largo de los vasos esplénicos, en la pared del yeyuno, en el mesenterio, en el epiplón mayor, en la pelvis o en el escroto izquierdo. Aunque rara vez se detecta radiológicamente, es relativamente frecuente, ya que se da en aproximadamente el 10% de la población según los estudios de autopsia. Los bazos accesorios se localizan en el hilio esplénico o cerca de él en el 80% de los casos. En el resto de los casos se encuentra en la cola del páncreas o cerca de ella. Los bazos accesorios no suelen suponer una amenaza clínica y los hallazgos radiológicos de las técnicas de imagen actualmente avanzadas son herramientas diagnósticas útiles para evitar la cirugía . El único método diagnóstico seguro es el muestreo directo, a menos que produzca falsamente células de islotes pancreáticos, como en nuestro caso. En este informe analizamos el caso de un bazo accesorio intrapancreático (BIP) tratado quirúrgicamente y que radiológica y citológicamente simulaba un tumor neuroendocrino de páncreas.
INFORME DE UN CASO
Un varón caucásico de 60 años fue remitido a nuestra clínica para la evaluación y tratamiento de una masa solitaria incidental, en el cuerpo del páncreas, que simulaba un tumor endocrino. En una revisión rutinaria, el paciente presentaba una ligera elevación del antígeno de carbohidratos (CA) 19-9 hasta 40 U/mL (rango de referencia: 0-37 U/mL). La tomografía computarizada (TC) con contraste mostró una lesión redonda y homogénea, de 1,2 cm de diámetro, localizada en la parte superior del cuerpo pancreático (Figura 1).
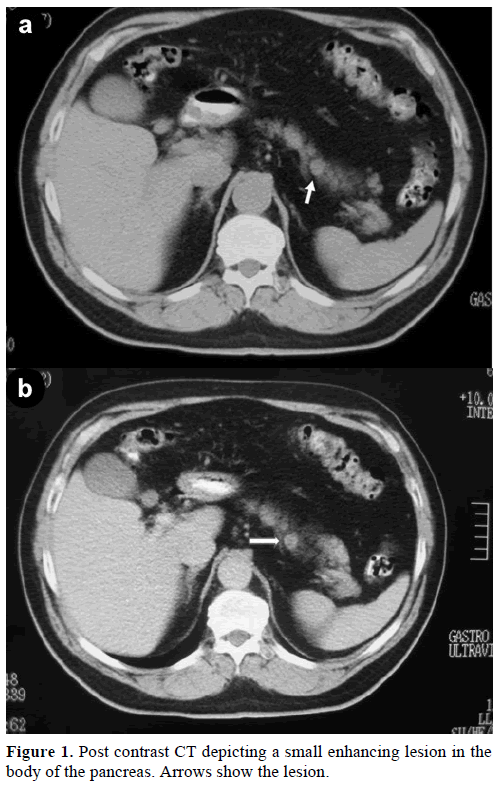
Figura 1. TC post-contraste que muestra una pequeña lesión que realza en el cuerpo del páncreas. Las flechas muestran la lesión.
La resonancia magnética (RM) con contraste reveló una masa redonda, bien definida, de 1 cm de diámetro, con baja intensidad de señal en las imágenes ponderadas en T1, realce heterogéneo de la lesión durante la fase arterial en las imágenes ponderadas en T con gadolinio e hiperintensidad en las imágenes ponderadas en T2 saturadas de grasa (figura 2).
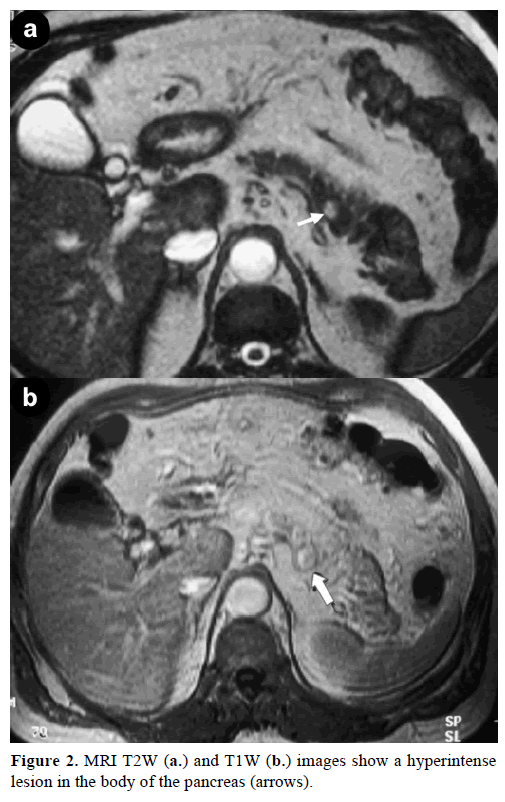
Figura 2. Las imágenes T2W (a.) y T1W (b.) de la RMN muestran un hiperintenselete en el cuerpo del páncreas (flechas).
La ecografía endoscópica (EUS) mostró un nódulo bien delineado, de aproximadamente 1,2 cm de tamaño, relativamente homogéneo, con márgenes bien definidos y lisos, mayor aporte sanguíneo y ecogenicidad mixta. Estos atributos eran compatibles con un tumor neuroendocrino. La masa estaba localizada en el cuerpo del páncreas, directamente periférica al tronco celíaco y entre el conducto pancreático y la pared gástrica. No se observaron ganglios linfáticos regionales ni otros hallazgos patológicos.
Una biopsia por aspiración con aguja fina (AAF) guiada por USE dio como resultado grupos celulares de diversos tamaños, inmunopositivos para cromogranina, glucagón, gastrina y somatostatina y con un índice de proliferación Ki-67 inferior al 2%; estos hallazgos eran morfológica e inmunohistoquímicamente característicos de una neoplasia neuroendocrina (figura 3).
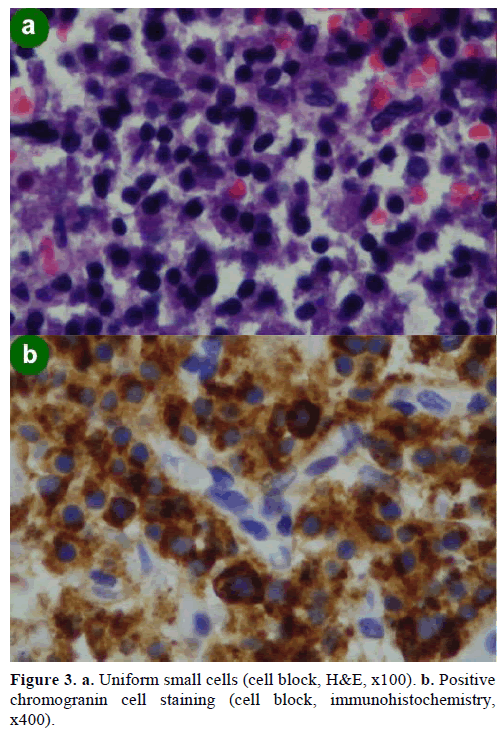
Figura 3. a. Células pequeñas uniformes (bloque celular, H&E, x100). b. Tinción celular positiva de cromogranina (bloque celular, inmunohistoquímica, x400).
La gammagrafía de cuerpo entero con 111indium-octreotide fue negativa para receptores de somatostatina.
Las pruebas de laboratorio no revelaron ningún hallazgo anormal ni había marcadores tumorales como el antígeno carcinoembrionario (CEA), la alfa-fetoproteína (AFP) y el CA 19-9 (15 U/mL). Los niveles séricos de glucagón, gastrina y somatostatina fueron de 77,2 pg/mL (rango de referencia: 30-210 pg/mL), 20 pg/mL (rango de referencia: 0-110 pg/mL) y 19,3 pg/mL (rango de referencia: 5-27 pg/mL) respectivamente. Para descartar el síndrome de neoplasia endocrina múltiple tipo 1 (MEN-1), se midieron los siguientes niveles hormonales séricos: parathormona (PTH) intacta (82,4 pg/mL; rango de referencia: 15-65 pg/mL), triyodotironina (T3: 0,9 ng/mL; rango de referencia: 0.7-1,5 ng/mL), tiroxina (T4: 7,4 μg/dL; rango de referencia: 4,5- 12 μg/dL), hormona estimulante del tiroides (TSH: 1,8 μIU/mL; rango de referencia: 0,4-4,5 μIU/mL), índice de tiroxina libre, (FTI: 9,7μg/dL; rango de referencia: 6,3- 12,4μg/dL). La resonancia magnética de la hipófisis no presentaba ningún signo.
Sobre la base de los resultados anteriores, se sospechó un tumor endocrino no funcional y se realizó una pancreatectomía distal con esplenectomía. La muestra quirúrgica contenía un nódulo redondo, bien delimitado, liso, de color rojo oscuro, de 1 cm de diámetro, rodeado de tejido pancreático. No se identificaron otras lesiones a nivel macroscópico, tras un meticuloso seccionamiento. Microscópicamente, el nódulo tenía la estructura de un bazo. Por lo tanto, la masa fue diagnosticada como un IPAS (Figuras 4 y 5). Ocho ganglios linfáticos, identificados en el hilio esplénico, eran benignos.
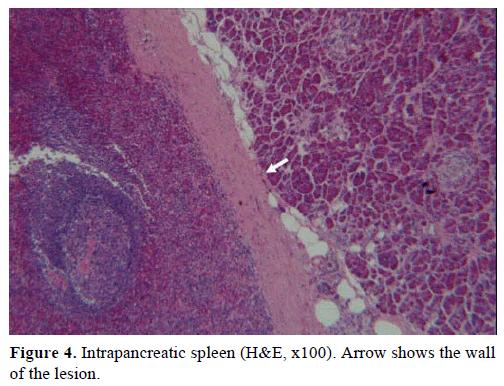
Figura 4. Bazo intrapancreático (H&E, x100). La flecha muestra la pared de la lesión.
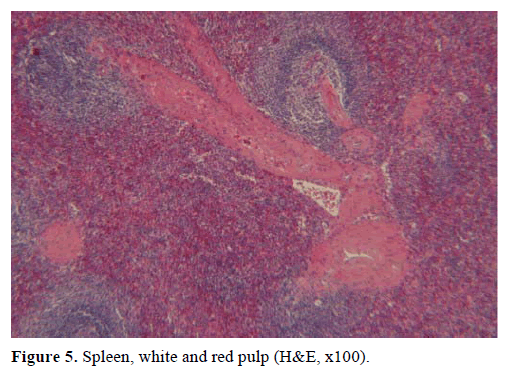
Figura 5. Bazo, pulpa blanca y roja (H&E, x100).
DISCUSIÓN
El tejido esplénico ectópico puede clasificarse en dos categorías: la esplenosis debida al autotransplante de tejido esplénico (normalmente tras una esplenectomía) y los bazos accesorios que constituyen focos congénitos de tejido esplénico sano separado del cuerpo principal del bazo . Embriológicamente, el bazo deriva del tejido mesenquimal que se encuentra entre las capas del mesogastrio dorsal. Durante las semanas 6 a 8 de vida, el bazo se encuentra muy cerca de la extensión más cefálica del mesonefros . Después de la fusión esplenorrenal, se puede encontrar un bazo accesorio en el parénquima y en el retroperitoneo o puede descender a la pelvis o al escroto. En el examen macroscópico, un IPAS suele estar rodeado por una cápsula fibrótica que lo separa del parénquima pancreático adyacente. Su histología es similar a la del bazo ortotópico . Las lesiones o procesos relativos al bazo, como la hemosiderosis, la leucemia, el linfoma y el hiperesplenismo pueden afectar al tejido esplénico accesorio. Por lo tanto, debe considerarse una búsqueda cuidadosa de bazos accesorios en el diagnóstico diferencial de las densidades nodulares demostradas por el estudio radiológico del páncreas.
La existencia de un IPAS debe considerarse cuando una masa pancreática tiene las densidades de la TC y/o las intensidades de la señal de la RMN similares a las del bazo, en las imágenes precontraste y realzadas con contraste de todas las modalidades de imagen. En particular, el realce no homogéneo de una IPAS en sus fases iniciales puede ser una pista diagnóstica. La demostración angiográfica de una irrigación sanguínea esplénica podría ser útil para excluir un tumor pancreático o suprarrenal.
El diagnóstico diferencial de los bazos accesorios intra y peripancreáticos podría incluir los tumores neuroendocrinos pancreáticos, los quistes linfoepiteliales, los linfomas, las metástasis hipervasculares, los tumores pseudopapilares sólidos y los adenocarcinomas pancreáticos . Actualmente, no existen criterios clínicos o radiográficos para el diagnóstico o la diferenciación de un IPAS de una neoplasia maligna.
Los hallazgos radiológicos y el diagnóstico preoperatorio de los IPAS referidos, resecados quirúrgicamente y confirmados patológicamente se resumen en la Tabla 1. La mayoría de los casos se consideraron inicialmente como tumores endocrinos no funcionales o tumores de células de los islotes y sólo uno de cada doce casos se diagnosticó de forma concluyente antes de la operación como un IPAS después de un tratamiento quirúrgico repetido sin éxito para la púrpura trombocitopénica idiopática (PTI). El tamaño osciló entre 1,0 y 2,5 cm, con una media de 1,55 cm. Los tumores endocrinos no funcionales representan el 15-41% de los tumores pancreáticos endocrinos y la tasa de su transformación maligna es del 62-92%, dependiendo del tipo de tumor . La resección total del tumor es el predictor definitivo de la supervivencia a largo plazo, independientemente del tamaño, la localización, la diferenciación histológica, la afectación de los ganglios linfáticos y otros parámetros .
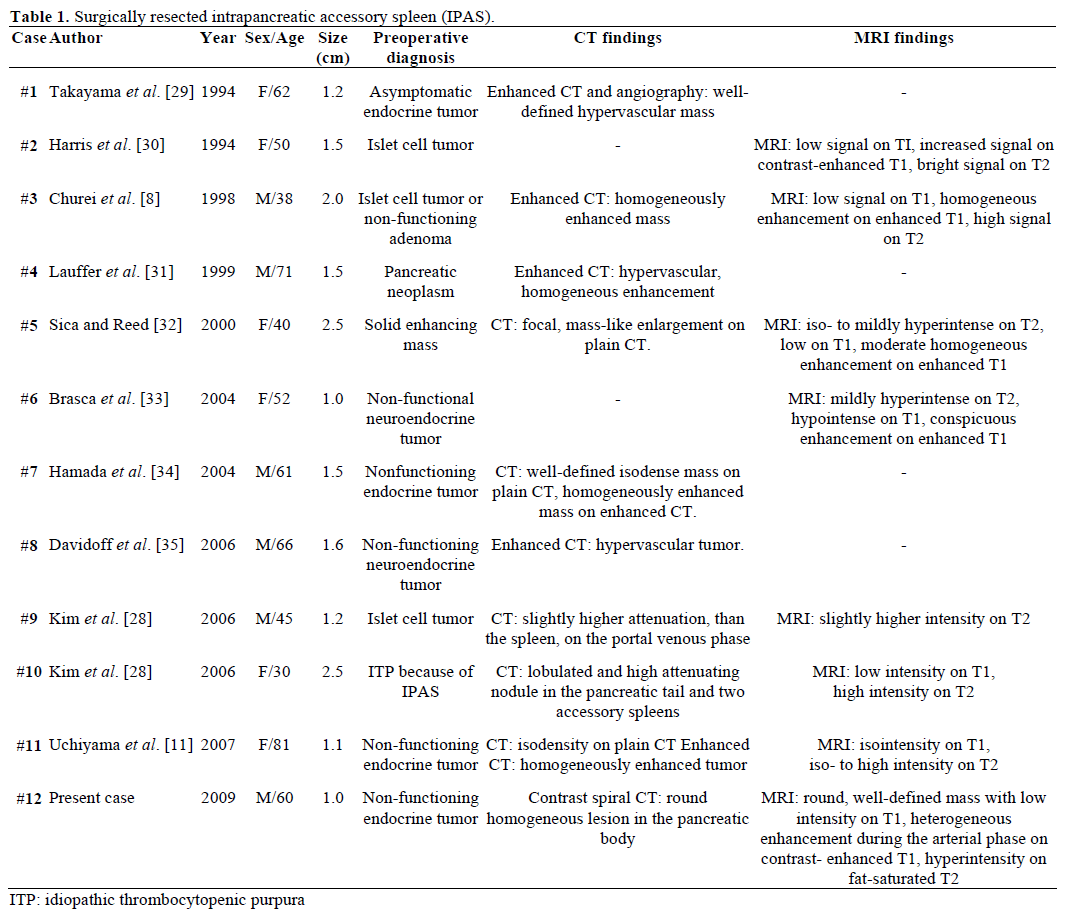
Dado que no se ha establecido un tamaño de corte para diferenciar entre los tumores neuroendocrinos malignos y los benignos no funcionales del páncreas, se ha sugerido que todos los tumores de este tipo mayores de 1 cm deben ser extirpados si el paciente es un buen candidato para la cirugía .
En la ecografía de base en escala de grises, un IPAS suele verse como una masa redonda u ovalada con una textura ligeramente ecogénica y homogénea, rodeada por una interfase de alta amplitud y mostrando realce detrás de la lesión. En la ecografía Doppler de color o de potencia, se ha informado de que un suministro de sangre característico (que representa el hilio vascular que entra en la masa), ofrece una sensibilidad del 90% en el diagnóstico de un IPAS . En la ecografía con contraste (CEUS) utilizando Levovist® (Schering, Berlín, Alemania), un IPAS muestra un realce no homogéneo en la fase vascular temprana, un realce similar al del bazo durante la fase postvascular y un realce prolongado en la fase parenquimatosa hepatoesplénica.
Los hallazgos en la EUS incluyen una lesión redonda a ovalada con márgenes regulares y nítidos y una textura de eco homogénea, que va de hipo a hiperecoica . La citología FNA guiada por EUS revela una población de linfocitos predominantemente pequeños y un infiltrado inflamatorio mixto que representa la pulpa blanca. También se observa un componente vascular conspicuo compuesto por vasos sanguíneos de paredes finas que representan los senos esplénicos.. Estos senos están bien visualizados en las secciones del bloque celular. Curiosamente, las células endoteliales de los senos esplénicos se caracterizan por la inmunotinción para CD8, que se reconoce más comúnmente como un marcador de células T. La tinción parece ser específica, porque las células endoteliales sistémicas y los hemangiomas son negativos para CD8 . En los casos en los que la PAF del bazo accesorio sólo produce linfocitos, sin otros elementos esplénicos, la citometría de flujo y la inmunohistoquímica pueden emplearse para excluir un trastorno linfoproliferativo, incluido el linfoma de Hodgkin, incluso si no puede confirmarse un diagnóstico definitivo de bazo accesorio . Schreiner et al. informaron de tres casos de IPAS diagnosticados mediante biopsia por aspiración con aguja fina guiada por USE. En nuestro caso, probablemente debido a la toma de muestras de grupos de células de los islotes del parénquima pancreático adyacente, el mismo procedimiento fue indicativo de un tumor neuroendocrino, lo que llevó a un sobretratamiento quirúrgico.
Un falso positivo similar de EUS-FNA, en el que un nódulo esplénico pancreático fue confundido con un tumor de células de los islotes también ha sido reportado por Ardengh et al. . En general, la EUS-FNA tiene una alta (80-90%) sensibilidad y especificidad para los tumores neuroendocrinos pancreáticos, aunque su precisión para dichos tumores se considera inferior a la del adenocarcinoma pancreático. Para minimizar los errores de diagnóstico, la EUS-FNA de los tumores neuroendocrinos pequeños debe ser realizada por un endoscopista experimentado y la evaluación citopatológica debe combinarse con la inmunohistoquímica .
La gammagrafía de hematíes dañados por el calor con 99mTc (HDRBC), combinada con la tomografía computarizada por emisión de fotón único (SPECT), es un método altamente sensible y específico para la detección del tejido esplénico, ya que hasta el 90% de los HDRBC inyectados son atrapados por este tejido . Aunque la gammagrafía permite una visualización selectiva del bazo con una excelente relación entre el bazo y el hígado, la visualización del bazo sigue siendo difícil en condiciones en las que hay un tejido esplénico mínimamente funcional, como en los casos de bazos accesorios . Además, la gammagrafía, incluso con SPECT, ofrece una resolución espacial inferior en comparación con otras modalidades de imagen transversal como la TC o la RM. Por lo tanto, la gammagrafía se utiliza con frecuencia junto con otras técnicas de imagen transversal. Además, la RM potenciada por óxido de hierro superparamagnético (SPIO) se considera una excelente alternativa a la gammagrafía con 99mTc-HDRBC cuando un IPAS presenta una caída de señal similar a la del bazo. Además de la caída de señal referida, otra diferencia entre los IPAS y las neoplasias pancreáticas hipervasculares es el realce heterogéneo en la tomografía computarizada en fase arterial.
Los bazos accesorios pueden necesitar tratamiento quirúrgico cuando simulan linfadenopatías o tumores, o cuando se vuelven sintomáticos debido a torsión, rotura espontánea, hemorragia o formación de quistes. Todo el tejido esplénico funcional también debe ser extirpado para el tratamiento de trastornos hematológicos como la PTI.
En conclusión, es probable que las modernas técnicas de imagen hagan que en el futuro se descubra un número cada vez mayor de bazos accesorios intrapancreáticos, lo que plantea importantes retos diagnósticos y terapéuticos. En estos casos deben utilizarse todos los medios diagnósticos no invasivos para evitar procedimientos quirúrgicos innecesarios y disminuir la morbilidad general del paciente.
Conflicto de intereses
Los autores no tienen ningún conflicto de intereses potencial
- Halpert B, Gyorkey F. Lesiones observadas en bazos accesorios de 311 pacientes. Am J Clin Pathol 1959; 32:165-8.
- Halpert B, Alden ZA. Bazos accesorios en o en la cola del páncreas: Un estudio de 2.700 necropsias adicionales. Arch Pathol 1964; 77:652-4.
- Kim SH, Lee JM, Han JK, Lee JY, Kim KW, Cho KC, Choi BI. Bazo accesorio intrapancreático: hallazgos en RMN, TC, US y gammagrafía, y el análisis patológico. Korean J Radiol 2008; 9:162-74.
- Moore K. The developing human. Philadelphia: Saunders, 1986: 225-8.
- Weiand G, Mangold G. Accessory spleen in the pancreatic tail — a neglected entity? Una contribución a la embriología, topografía y patología del tejido esplénico ectópico. Chirurg 2003; 74:1170-7.
- Davidson ED, Campbell WG, Hersh T. Epidermoid splenic cyst occurring in an intrapancreatic accessory spleen. Dig Dis Sci 1980; 25:964-7.
- Landry ML, Sarma DP. Bazo accesorio en la cabeza del páncreas. Hum Pathol 1989; 20:497.
- Churei H, Inoue H, Nakajo M. Intrapancreatic accessory spleen: case report. Abdom Imaging 1998; 23:191-3.
- Hayward I, Mindelzun RE, Jeffrey RB. Intrapancreatic accessory spleen mimicking pancreatic mass on CT. J Comput Assist Tomogr 1992; 16:984-5.
- Smith CD, Behrns KE, van Heerden JA, Sarr MG. Radical pancreatoduodenectomy for misdiagnosed pancreatic mass. Br J Surg 1994; 81:585-9.
- Uchiyama S, Chijiiwa K, Hiyoshi M, Ohuchida J, Imamura N, Nagano M, et al. Bazo accesorio intrapancreático que simula un tumor endocrino del páncreas: informe de un caso y revisión de la literatura. J Gastrointest Surg 2008; 12:1471-3.
- Eriksson B, Oberg K. PPomas y tumores endocrinos pancreáticos no funcionales: Presentación clínica, diagnóstico y avances en el manejo. En: Mignon M, Jensen RT, eds. Endocrine Tumors of the Pancreas: Recent Advances in Research and Management. Fronteras de la investigación gastrointestinal. Basilea, Suiza: Karger, 1995: 208-222.
- Oberg K, Eriksson B. Endocrine tumours of the pancreas. Best Pract Res Clin Gastroenterol 2005; 19:753-81.
- Chung JC, Choi DW, Jo SH, Heo JS, Choi SH, Kim YI. Tumores endocrinos malignos no funcionales del páncreas: factores de predicción de la supervivencia después del tratamiento quirúrgico. World J Surg 2007; 31:579-85.
- Dralle H, Krohn SL, Karges W, Boehm BO, Brauckhoff M, Gimm O. Surgery of resectable nonfunctioning neuroendocrine pancreatic tumors. World J Surg 2004; 28:1248-60.
- Subramanyam BR, Balthazar EJ, Horii SC. Sonografía del bazo accesorio. AJR Am J Roentgenol 1984; 143:47-9.
- Kim SH, Lee JM, Lee JY, Han JK, Choi BI. Contrast-enhanced sonography of intrapancreatic accessory spleen in six patients. AJR Am J Roentgenol 2007; 188:422-8.
- Barawi M, Bekal P, Gress F. Accessory spleen: a potential cause of misdiagnosis at EUS. Gastrointest Endosc 2000; 52:769-72.
- Syed S, Zaharopoulos P. Thoracic splenosis diagnosed by fineneedle aspiration cytology: a case report. Diagn Cytopathol 2001; 25:321-4.
- Carlson BR, McQueen S, Kimbrell F, Humphreys S, Gentry HL, Esbenshade A. Thoracic splenosis. Diagnóstico de un caso por citología de aspiración con aguja fina. Acta Cytol 1988; 32:91-3.
- Kraus MD. Histología e histopatología esplénica: una actualización. Semin Diagn Pathol 2003; 20:84-93.
- Renne G, Coci A, Biraghi T, Schmid C. Fine needle aspiration of thoracic splenosis. A case report. Acta Cytol 1999; 43:492-4.
- Pugh JL, Jhala NC, Eloubeidi MA, Chhieng DC, Eltoum IA, Crowe DR, et al. Diagnosis of deep-seated lymphoma and leukemia by endoscopic ultrasound-guided fine-needle aspiration biopsy. Am J Clin Pathol 2006; 125:703-9.
- Schreiner AM, Mansoor A, Faigel DO, Morgan TK. Intrapancreatic accessory spleen: mimic of pancreatic endocrine tumor diagnosed by endoscopic ultrasound-guided fine-needle aspiration biopsy. Diagn Cytopathol 2008; 36:262-5.
- Ardengh JC, de Paulo GA, Ferrari AP. FNA guiada por EUS en el diagnóstico de tumores neuroendocrinos pancreáticos antes de la cirugía. Gastrointest Endosc 2004; 60:378-84.
- Voss M, Hammel P, Molas G, Palazzo L, Dancour A, O’Toole D, et al. Value of endoscopic ultrasound guided fine needle aspiration biopsy in the diagnosis of solid pancreatic masses. Gut 2000; 46:244-9.
- Ota T, Tei M, Yoshioka A, Mizuno M, Watanabe S, Seki M, et al. Intrapancreatic accessory spleen diagnosed by technetium-99m heat-damaged red blood cell SPECT. J Nucl Med 1997; 38:494-5.
- Kim SH, Lee JM, Han JK, Lee JY, Kang WJ, Jang JY, et al. MDCT and superparamagnetic iron oxide (SPIO)-enhanced MR findings of intrapancreatic accessory spleen in seven patients. Eur Radiol 2006; 16:1887-97.
- Takayama T, Shimada K, Inoue K, Wakao F, Yamamoto J, Kosuge T. Intrapancreatic accessory spleen. Lancet. 1994; 344:957- 8.
- Harris GN, Kase DJ, Bradnock H, Mckinley MJ. Bazo accesorio que causa una masa en la cola del páncreas: Hallazgos de imágenes de RMN. AJR Am J Roentgenol 1994; 163:1120-1.
- Läuffer JM, Baer HU, Maurer CA, Wagner M, Zimmermann A, Büchler MW. Intrapancreatic accessory spleen.A rare cause of pancreatic mass. Int J Pancreatol 1999; 25:65-8.
- Sica GT, Reed MF. Intrapancreatic accessory spleen. Radiology 2000; 217:134-7.
- Brasca LE, Zanello A, De Gaspari A, De Cobelli F, Zerbi A, Fazio F, Del Maschio A. Intrapancreatic accessory spleen mimicking a neuroendocrine tumor: magnetic resonance findings and possible diagnostic role of different nuclear medicine tests. Eur Radiol. 2004; 14:1322-3.
- Hamada T, Isaji S, Mizuno S, Tabata M, Yamagiwa K, Yokoi H, Uemoto S. Laparoscopic spleen-preserving pancreatic tail resection for an intrapancreatic accessory spleen mimicking a nonfunctioning endocrine tumor: report of a case. Surg Today 2004; 34:878-81.
- Davidoff S, Fernandes A, Sideridis K, Gecelter G, Bragdon J, Bank S. Clinical challenges and images in GI. Bazo accesorio intrapancreático que simula un tumor neuroendocrino no funcional. Gastroenterología 2006; 131:350, 689.