Ocel je nejdůležitějším konstrukčním materiálem. Velmi důležité je kalení oceli.
Videa z přednášek
![]() Ocel vs. ocel
Ocel vs. ocel
(nesestříhaný záznam)
![]() Ocel: Část 1 ,
Ocel: Část 1 , ![]() Ocel: Část 2 ,
Ocel: Část 2 , ![]() Ocel: Část 3
Ocel: Část 3
![]() Vlastnosti a struktura zrna: (Starý, ale velmi dobrý)
Vlastnosti a struktura zrna: (Starý, ale velmi dobrý)
Železo je ve vesmíru hojně zastoupeno, nachází se ve Slunci a mnoha typech hvězd ve značném množství. Předpokládá se, že jádro Země je tvořeno niklem a železem a je žhavější než povrch Slunce. Toto intenzivní teplo z vnitřního jádra způsobuje pohyb materiálu ve vnějším jádře a plášti (konvekční proudy).
(Poznámka: Zvláštní, jak to vlastně nevíme, že? – Víme, že s hloubkou je tepleji, ale můžeme jen odhadovat, jak horké je ve středu Země. Dokonce i v hloubce 12 km pod zemí se výpočty vědců rozcházely o více než 100 % – bylo tam tepleji, než se předpokládalo. Při pokusu o vrtání do těchto hloubek se hornina rozžhaví natolik, že se stane plastickou, přitiskne se zpět na otvor a zasekne vrták. Krysy. Tolik o kopání do středu země.)
Uhlíková ocel
Ocel je slitina železa (Fe) a uhlíku (C) s 0,2 až 2,04 % hmotnosti uhlíku. Uhlík je cenově nejvýhodnějším legujícím materiálem železa, ale používají se i různé další legující prvky, například mangan, chrom, vanad a wolfram.
| Uhlíková ocel | ANSI def’n | General Def’n | Použití a vlastnosti | |
| Nízkouhlíková ocel | 0.05-0,15% | <0,1% | Měkká, tvárná. Snadno se tváří. | |
| Měkká ocel | 0,16-0,29 % | 0,1-0,25 % | Nízká pevnost v tahu, ale je levná a kujná; tvrdost povrchu lze zvýšit nauhličením. | |
| Středně uhlíkatá ocel | 0,30-0,59 % | 0,25-0,45 % | Vyvažuje tažnost a pevnost a má dobrou odolnost proti opotřebení; používá se pro velké díly, kování a automobilové součásti. | |
| Vysoko uhlíkatá ocel | 0,25-0,45 % | Vyvažuje tažnost a pevnost a má dobrou odolnost proti opotřebení; používá se pro velké díly, kování a automobilové součásti.6-0,99% | 0,45-1,0% | Velmi pevná, používá se na pružiny a vysokopevnostní dráty. |
| Ultra vysokouhlíková ocel | 1,0-2,0% | 1,0-1,50% (>1,5% vzácná) |
Velmi tvrdá – nože, razidla. Obvykle cokoli nad 1,2 % by vyžadovalo jiné slitiny, aby se zabránilo nadměrné křehkosti. Velmi vysokého obsahu uhlíku lze dosáhnout pomocí práškové metalurgie. | |
| Litina | – | 2,5-4,0 % | Nižší bod tání, snadné lití, nižší houževnatost a pevnost než ocel. |
Podíl uhlíku v různých ocelích;

Různé množství legujících prvků a způsob jejich zabudování do oceli (rozpustné prvky, vysrážená fáze) ovlivňuje takové vlastnosti, jako je tvrdost, tažnost a pevnost v tahu výsledné oceli. Se zvyšujícím se obsahem uhlíku se ocel stává tvrdší a pevnější než železo, ale také křehčí. Maximální rozpustnost uhlíku v železe (v oblasti austenitu) je 2,14 % hmotnostních a vyskytuje se při 1149 °C; při vyšších koncentracích uhlíku nebo nižších teplotách vzniká cementit (velmi křehký). Pokud přidáte více uhlíku, získáte litinu, která má nižší teplotu tání a snáze se odlévá.
Tavené železo obsahující jen velmi malé množství jiných prvků, ale obsahuje 1-3 % hmotnosti strusky ve formě částic protáhlých v jednom směru, což dává železu charakteristické zrno. Je odolnější proti korozi než ocel a snadněji se svařuje. Dnes se běžně hovoří o „železářském a ocelářském průmyslu“, jako by šlo o jeden celek, ale historicky šlo o samostatné produkty.
Ocel se vyrábí již tisíce let, ale rozšířila se až po vynalezení efektivnějších výrobních metod v 17. století. Bessemerův proces v polovině 19. století učinil ocel relativně levnou pro masově vyráběné zboží. Další zdokonalení procesu, například výroba oceli na bázi kyslíku, dále snížilo výrobní náklady a zároveň zvýšilo kvalitu kovu. Dnes je ocel jedním z nejběžnějších materiálů na světě a je hlavní součástí budov, nástrojů, automobilů a spotřebičů.

Získat pdf: XLER_International_Compare.pdf
VIDEO: Vlastnosti a struktura zrna. BBC 1973
Nesmějte se datu – toto video překonává všechna ta ubohá moderní videa, která vám nabídnou efektní úvod, ale nic víc než mluvící hlavu. Nikdy se neodváží opustit studio. Toto staré video je báječné pro přehledné seznámení se strukturou zrna oceli.
Díl 1: Co je to zrno? (Video 11MB)
- Skvrny viditelné na pozinkovaném předmětu jsou krystaly nebo zrnka zinku.
- Všechny kovy se skládají ze zrnek, ale obvykle jsou neviditelná (příliš malá, aby byla vidět, nebo mají stejný lesk/barvu).
- Proces leptání:
- V čistém kovu mají zrnka různé barvy, protože odrážejí světlo.
- Drobné krystalky rostou směrem ven, až se setkají. Každý plně vyvinutý krystal se nazývá zrno.
Část 2: Rekrystalizace (video 13MB)
- Před zpracováním za studena mají zrna podobnou velikost a tvar
- Zpracováním za studena se zrna prodlouží, zvýší se tvrdost a pevnost, sníží se tažnost.
- Při 350 °C se v Al tvoří nová zrna, která nahrazují stará. Nazývá se rekrystalizace
- Rekrystalizace změkčuje, snižuje pevnost, zvyšuje tažnost
- Nadměrná teplota rekrystalizace dává špatné mechanické vlastnosti
Část 3: Tepelné zpracování oceli (video 23MB)
- Ocelová zrna jsou příliš malá, aby byla vidět – je třeba mikroskop s cca 250násobným zvětšením.
- Ferit: Světle zbarvený. Vyroben ze železa. Tažný k oceli
- Perlit: tmavěji zbarvený. Vrstvy železa + karbid železa. Tvrdost a pevnost k oceli
- 100% perlit je asi 0,8%C. Perlit, teplota rekrystalizace 720C.
- Normalizace – ochlazení na vzduchu, zmenšení velikosti zrn a rovnoměrnější tvar, zvýšení houževnatosti
- Kalení – zvýšení tvrdosti. Není dostatek času na vytvoření perlitu, takže vzniká jehlicovitá struktura – martenzit. Velmi tvrdý a křehký.
- Kalení – (po kalení) obnovuje houževnatost. Modifikuje jehličky martenzitu malými vločkami uhlíku. Tím se získá tvrdost A houževnatost.
- 0,1%C ocel (měkká ocel). Rekrystalizace 900C. Nedostatek uhlíku pro vznik martenzitu.
Diagram rovnováhy železa a uhlíku
Vynikající odkaz (Cambridge University): http://www.msm.cam.ac.uk/phase-trans/2008/Steel_Microstructure/SM.html
Rovnovážný diagram je graf různých strukturních uspořádání, která se vyskytují v určitém rozsahu legujícího prvku.
Tento diagram ukazuje, jak se železo a uhlík spojují, POKUD se pomalu ochlazují (v rovnováze). Pod 2 % je ocel, nad 2 % směřuje do oblasti litiny, kde má uhlík tendenci koagulovat (shlukovat se). Cementit Fe3C má 6,67 %C a je to v podstatě keramika. Eutektoid (perlit) u E má 0,83 % C, méně uhlíku je hypoeutektoidní ocel (A) a větší je hypereutektoid (B). Alfa železo (ferit), gama železo (austenit, který existuje pouze při vysoké teplotě) a delta železo (další vysokoteplotní struktura).
Dvě velmi důležité fázové změny probíhají při teplotách 0,83 % C a 4,3 % C. Při teplotách 0,83 % C a 723 ºC dochází k přeměně na eutektoid, nazývaný perlit. Tyto 2 fáze se oddělují ve vrstvách. Z gama (austenit) –> alfa + Fe3C (cementit)
Při 4,3 % C a 1130 ºC je přeměna eutektická, nazývá se ledeburit. L(kapalina) –> gama (austenit) + Fe3C (cementit). Jedná se o litinu.
BTW. Protože uhlík (12) je mnohem lehčí než Fe (56), skutečné atomové % uhlíku (počítáním atomů) je ve skutečnosti asi 4,6krát vyšší než hmotnostní %C. Takže už to není tak úžasné, že? Třeba jak 0,5 % uhlíku dokáže úplně proměnit měkké železo… ve skutečnosti je to asi 2 %, pokud počítáme atomy – ne hmotnost.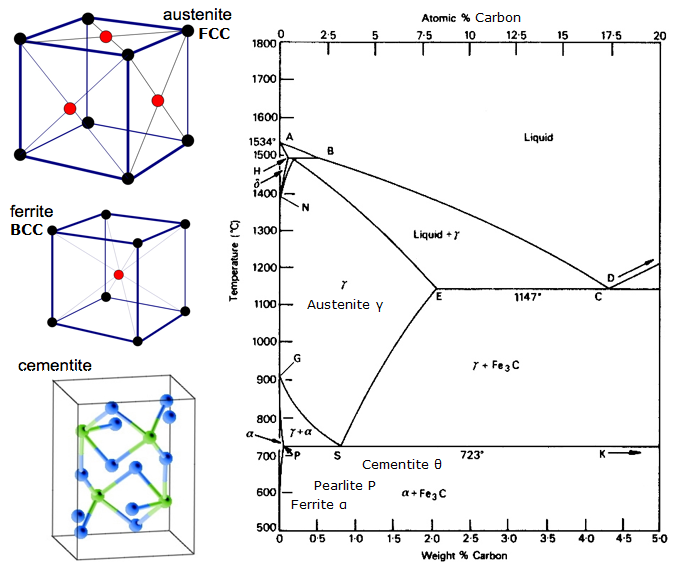
Souhrn struktur Fe-C (zrn)
- Austenit (γ-železo). Existuje pouze při teplotě nad 723C, kdy vzniká struktura FCC γ-železa. Může se rozpouštět až do 2,1 %C hmotnosti. Nemagnetický, měkký (proto máme zpracování za tepla). Austenit může existovat i při pokojové teplotě, pokud vyměníte některé atomy železa za něco jiného – například nikl. To je austenitická nerezová ocel – například 316. A stejně jako vysokoteplotní austenit jsou tyto nerezové oceli nemagnetické. Některé jiné typy nerezových ocelí jsou magnetické.
- Cementit (karbid železa Fe3C, 6,67 %C hmotnosti. V jednotkové buňce je dvanáct atomů železa a čtyři atomy uhlíku, tedy 33 % atomů uhlíku). Velmi tvrdý a křehký, protože je to keramika. Slyšeli jste někdy o karbidu wolframu? No, tohle je karbid železa.
- Ledeburit (eutektikum feritu a cementitu, 4,3 % uhlíku.)
- Ferit (α-železo, δ-železo; měkký). Bez uhlíku, BCC. Měkký a tvárný.
- Perlit (88 % feritu, 12 % cementitu, což je 0,83 % C) Pevnější než ferit
- Martenzit. Vzniká při příliš rychlém ochlazování na to, aby se vytvořil perlit, takže uzamyká hroty cementitu do zrna. K tomu dochází při kalení oceli s dostatečným obsahem uhlíku. Velmi tvrdý.
Mikrofotografie (fotografie z mikroskopu).
(A) = 0,1 %C ferit/perlit, (B) = 0,25 %C více perlitu, (C) = 0,83 %C celý perlit, (D) = 1,4 %C perlit/cementit
Pohled na perlit zblízka ukazující vrstvy feritu (bílá) a cementitu (tmavá).
Více o perlitu: https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Velký FC rovnovážný diagram

Velká verze pro tisk 2000x2658px
Smyk
Při deformaci kusu kovu se deformují právě zrna. Zrno je krystal, uspořádané uspořádání atomů v mřížce. Pokud se atomy od sebe roztáhnou, jedná se o pružnou deformaci, protože atomy jsou drženy pohromadě přitažlivostí elektronů – což působí jako pružina. Trvalá (nebo plastická) deformace však znamená, že atomy ve skutečnosti prokluzují kolem sebe ve vrstvách nebo rovinách.
Skutečné krystaly neprokluzují v celé rovině najednou. K tomu by byla zapotřebí velmi velká síla. Místo toho nedokonalosti krystalu umožňují prokluzování po jednotlivých atomech. Čím širší je rozsah zasažených atomů, tím je zrno tvárnější (snadno prokluzující). Zde je příklad nedokonalosti zvané dislokace, která může snadno procházet krystalem.
Tady je skutečný příklad prokluzu. (To si nevymýšlíme!)
Skenovací elektronový mikrofotografický snímek monokrystalu kadmia, který se deformuje skluzem dislokací na 100 rovinách a vytváří na povrchu stupně
.
Následující animace ukazuje mřížku atomů (například v kovu). Existují pouze 2 způsoby deformace atomů – axiální (v tahu a tlaku) a smyková (do stran).
Tato animace ukazuje pouze pružnou část křivky napětí/deformace, kde nedochází ke skluzu atomů.
Obsah této stránky vyžaduje novější verzi Adobe Flash Player.

Další informace najdete zde: http://www3.nd.edu/~manufact/MPEM_pdf_files/Ch03.pdf
Tak co to vlastně je BCC a FCC?
Krystalové struktury BCC (Body Centred Cubic) a FCC (Face Centred Cubic) jsou dva alternativní způsoby balení atomů železa.
- BCC je uspořádání při pokojové teplotě zvané ferit
- FCC je uspořádání při vysoké teplotě (>723oC) zvané austenit.
Stáhněte si soubory Inventoru: SC, BCC, FCC, všechny tři (SC+BCC+FCC)
![]()
SC je jednoduché kubické uspořádání a nevyskytuje se s atomy železa. Jedná se o mřížku soli – NaCl.
Nejmenší uspořádání (jednotka) je uvedeno níže. Všimněte si, jak se krychlová mřížka (vybarvená modře) rozšiřuje, když se mezi ně v mřížkách BCC a FCC vejdou další atomy.
![]()
V těchto níže uvedených diagramech často dochází k záměně.

Problém je v tom, že červené atomy vypadají jako atomy uhlíku a černé jako atomy železa. Ne, ne, ne!
Každý atom je železo! Jen obarvíme atomy železa, které nejsou v rozích, aby byly dobře vidět.
Dalším problémem těchto diagramů je to, že neexistuje žádný skutečný údaj o tom, že se vzdálenost rohových atomů ZVYŠUJE při přechodu od SC k BCC a FCC.
SC (jednoduchá kubická) struktura. NEŽELEZOPři SC (Simple Cubic) struktuře (kterou železo nemá) je vzdálenost mezi atomy D. (Kde D je průměr atomů) Takže objem této jednotky je D3 a objem atomu je 4/3Πr3. Takže hustota pevného atomu je 52 %. Není příliš kompaktní. |
 |
BCC (Body Centred Cubic) struktura. FERRITPři struktuře BCC (Body Centred Cubic) (kterou železo vytváří při teplotě 723oC) je vzdálenost mezi atomy železa 1,1547D. (Kde D je průměr atomů) Takže objem této jednotky je (1,1547D)3, a to se vejdou 2 atomy, takže objem atomů je 2×4/3Πr3. Hustota je tedy 68 % pevného atomu. Kompaktnější. Tato struktura se nazývá ferit. Uhlík se do této struktury vůbec nehodí (Tedy lžu. Může se v něm rozpustit ubohých 0,025 % C, což je prakticky nula, nebo 0,035 % při teplotě přechodu, což je pořád nic) |
 |
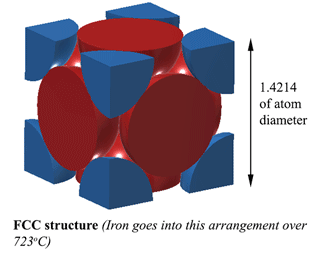
FCC (Face Centred Cubic) struktura. AUSTENITPři struktuře FCC (Face Centred Cubic) (kterou má železo při teplotě nad 723oC) je vzdálenost mezi atomy železa 1,4214D. (Kde D je průměr atomů) Takže objem této jednotky je (1,4214D)3, a to se vejdou 4 atomy, takže objem atomů je 4×4/3Πr3. Hustota je tedy 74 % pevného atomu. To je nejkompaktnější, takže má o 6 % větší hustotu než ferit!“ Tato struktura se nazývá austenit a může se v ní rozpustit 2 % uhlíku. Nezapomeňte, že to jsou 2 % hmotnosti, a protože železo (56) má 4,7násobek hmotnosti uhlíku (12), může rozpustit asi 21 % atomů uhlíku (Asi 1 atom uhlíku na každých 5 atomů železa). |
 |
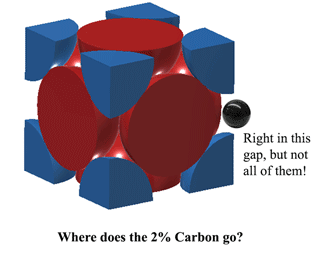
Takže kam se vejde uhlík v austenitu?Uhlík se vejde právě do toho prostoru uprostřed každé jednotkové hrany. To však způsobuje určité zkreslení, takže se atom uhlíku nevejde na KAŽDOU hranu. V nejlepším případě se při 1130oC do austenitu vejde něco přes 2 atomy uhlíku na každé 3 jednotky. (2C:12Fe nebo 1:6 podle atomů). Odtud pocházejí 2 % hmotnosti. Více zde (docela těžké) https://hal.archives-ouvertes.fr/jpa-00246587/document |
 |
Další informace o BCC a FCC zde:
https://www.nde-ed.org/EducationResources/CommunityCollege/Materials/Structure/metallic_structures.htm
http://lessons.chemistnate.com/simple-cubic-fcc-and-bcc.html
https://chem.libretexts.org/Courses/University_of_Arkansas_Little_Rock/Chem_1403%3A_General_Chemistry_2/Text/…
Video krystalových struktur Simple Cubic, Body-Centred Cubic a Face Centred Cubic. Atomy železa netvoří jednoduchou krychli.
Jednoduchá krychle, krychle s tělesovým středem a krychle s čelním středem
Kalení oceli
Kalení spočívá v zastavení prokluzu.
Jsou tři způsoby, jak toho dosáhnout.
- Zbavit se všech nedokonalostí (docela nemožný úkol, i když právě proto mohou velmi jemná vlákna dávat šílené pevnosti)
- Vyčerpat všechny skluzy, aby už k žádnému prokluzování nemohlo dojít. Tomu se říká zpevnění prací.
- Zabraňte skluzu, aby procházel celými zrny. Uhlík (a dusík) tvoří sloučeniny, které působí jako kalicí činidlo a brání dislokacím v krystalové mřížce železa (feritu) ve vzájemném klouzání. Martenzit to umí skvěle. Jedná se o kalení tepelným zpracováním.
Kalení oceli není na diagramu rovnováhy Fe-C znázorněno, protože kalení není v rovnováze! (Tj. ochlazení je příliš rychlé na to, aby se austenit s obsahem uhlíku dostal do složité struktury perlitu.

Z https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Rychlé ochlazení (kalení) vytváří jinou strukturu zrn, která se nazývá martenzit. Toto zrno je extrémně tvrdé a pevné a zároveň křehké. Hroty karbidu železa, které pronikají skrz zrno, nyní brání skluzu, takže se ztrácí tažnost.

Martenzit: University of Cambridge
Pro snížení křehkosti po kalení se používá popouštění, které oceli dodává houževnatost. Tím se upraví dendrity karbidu, aby získaly trochu houževnatosti – bez ztráty přílišné pevnosti a tvrdosti.
Kalení musí probíhat při teplotě nižší než rekrystalizace. K popouštění je nejlepší pec, ale lze ho provádět i plamenem podle barvy oceli. Barvy kalení lze použít jako vodítko pro určení teploty. Čím je popouštění teplejší, tím je ocel měkčí.
Slitiny, jako je nerezová ocel, tvoří pro danou teplotu tenčí vrstvy než uhlíkové oceli, a proto vytvářejí barvu nižší řady. Například světlá sláma odpovídá teplotě 300 °C pro SS, místo 230 °C pro CS. Barvy chladnější než červená (pod 500 °C) jsou ve skutečnosti zabarvením oxidů, nikoliv skutečným zářením samotné teploty. (Které by bylo infračervené a neviditelné. Všechno tedy září, jen to světlo není vidět!)
| Barva záření | Celcius | Záření | Temperační aplikace / ostatní |
| Žlutá-.Bílá | 1539°C | 2800°F | Nejvyšší bod tání (0%C čistého železa) |
| Jasně žlutá | 1130°C | 2066°F | Nejnižší teplota tání (4%C litina) |
| Žlutá | 1093°C | 2000°F | Měď taje při 1084°C, Zlato 1063°C |
| Tmavě žlutá | 1038°C | 1900°F | |
| Oranžově žlutá | 982°C | 1800°F | |
| Oranžová | 927°C | 1700°F | Mosaz se taví 930°C |
| Oranžově červená | 871°C | 1600°F | |
| Jasně červená | 816°C | 1500°F | |
| Červená | 760°C | 1400°F | Teplota rekrystalizace oceli 723°C |
| Středně červená | 704°C | 1300°F | |
| Tupě červená | 649°C | 1200°F | Hliník se taví 600-.660°C |
| Světle červená | 593°C | 1100°F | Kalení pro konstrukční oceli. |
| Velmi slabě červená, převážně šedá | 538°C | 1000°F | Kalení pro konstrukční oceli. |
| Tmavě šedá | 427°C | 0800°F | Kalení pro konstrukční oceli. Magnetická změna 410 |
| Oxidační barva | Celcius | Černá | Temperování Použití |
| Modrá | 302°C | 0575°F | Přípravky na dřevo, pružiny |
| Tmavě fialová | 282°C | 0540°F | Studená dláta, sety pro ocel |
| Fialová | 271°C | 0520°F | Tlačné nástroje, sekery |
| Hnědá/Fialová | 260°C | 0500°F | Děrovací nástroje, misky, západky, spirálové vrtáky, výstružníky |
| Hnědá | 249°C | 0480°F | Závitníky, střižné nože na kovy |
| Tmavá sláma | 241°C | 0465°F | Frézy, vrtáky |
| Světlá sláma | 229°C | 0445°F | Nástroje na hoblování a drážkování |
| Slabá sláma | 199°C | 0390°F |
Kalení:
Rychlost kalení: Oceli s vyšším obsahem uhlíku lze kalit pomaleji, ale ocel s nižším obsahem uhlíku bude třeba kalit rychle, aby se projevil kalicí účinek.
Rychlost kalení: (NEJRYCHLEJŠÍ) Slaná voda > voda > olej > vzduch > izolovaný. (SLOWEST)
Pro složitou a drahou práci je lepší pomalé kalení slitiny, protože je méně citlivá na změny teploty. Proto je většina nástrojových ocelí pro věci, jako jsou vstřikovací nástroje, kalená v oleji. Kalení vodou je vhodné pro jednoduché tvary, které lze snadněji kontrolovat, ale u silnějších profilů může způsobit praskání, protože povrch se smrští dříve než vnitřek.
Indukční kalení. Indukční kalení, při němž elektrická indukce (rychlé magnetické změny) zahřívá ocel, po níž rychle následuje kalení ve vodním paprsku. Alternativní způsob ohřevu místo plamene nebo pece.

Indukční kalení. http://www.thermobondflame.com/Services.page?i=4
Způsob kalení povrchu: Kalení CASE.
Tepelné zpracování = kalení > Martenzit (zadržuje prokluz).
Kalení vnějšího povrchu >kalení. Lokální kalení plamenem nebo indukční kalení vodou (ozubená kola).
Karbon pronikající vnějším povrchem > kalení. Karbonizace (zahřátí v uhlíkovém obalu nebo v plynném uhlíku nebo v zahřátých roztocích). Při nitridaci se místo uhlíku používá dusík, který má podobný účinek a snáze proniká do povrchu.

Kalení ocelových válců plamenem: http://www.thermobondflame.com/Services.page?i=2
Slitinové oceli
Vliv legujících prvků na vlastnosti nástrojové oceli: (Velmi zhruba)
- Uhlík: Zvyšování obsahu uhlíku mírně zvyšuje tvrdost a výrazně zvyšuje odolnost proti opotřebení. Dramatické zvýšení tvrdosti & pevnosti při tepelném zpracování.
- Mangan: Malé množství manganu snižuje křehkost a zlepšuje kujnost. Větší množství manganu zlepšují kalitelnost, umožňují kalení v oleji (je nutné méně silné kalení – což snižuje deformace při kalení).
- Křemík: Zlepšuje pevnost, houževnatost a odolnost proti nárazům.
- Wolfram: Zlepšuje „tvrdost za tepla“ – používá se u rychlořezných nástrojových ocelí. Velmi hustý (těžký)
- Vanad: Zjemňuje strukturu karbidu a zlepšuje kujnost, zlepšuje také tvrdost a odolnost proti opotřebení.
- Molybden: Zlepšuje hluboké kalení, houževnatost a ve větším množství i „tvrdost za tepla“. Používá se v rychlořezných nástrojových ocelích, protože je levnější než wolfram.
- Chrom: Zlepšuje kalitelnost, odolnost proti opotřebení a houževnatost.
- Nikl: V menší míře zlepšuje houževnatost a odolnost proti opotřebení.
Zapojení těchto prvků v různých kombinacích může působit synergicky, což zvyšuje účinky jejich samostatného použití. (Například cetain legující prvky mohou umožnit větší množství uhlíku tam, kde by tolik uhlíku bylo v oceli s čistým uhlíkem nezpracovatelné). Dalším příkladem je zajímavý způsob, jakým je nerezová ocel (chrom a nikl přidané k železu) poměrně odolná proti korozi.
Identifikační kódy ocelí
Kódovací systém AISI-SAE (American Iraon and Steel Institute – Society of Automotive Engineers). Čtyřmístný kód, první dvě číslice udávají obecný typ oceli a poslední dvě číslice jsou % uhlíku x 100. Například 1010 je obyčejná uhlíková srteel s 0,10 % C, 5120 je chromová ocel s 0,20 % C. Podrobněji zde

American Steel codes: Od Higginse: Materials for Engineers aand Technicians 5th Ed. 2010. str. 21
BSA (British Standards Association) používá šestimístný kód. Číslice jsou rozděleny do 3 skupin, jak je uvedeno níže. Například ocel s kódem 070M20 by byla 070 = uhlíková nebo uhlík-manganová ocel, M = specifikace mechanických vlastností, 20 = obsah uhlíku 0,20 %.

Kódy britských ocelí: Od Higginse: Materials for Engineers aand Technicians 5th Ed. 2010. s. 20
Číslo UNS (zkratka pro „Unified Numbering System for Metals and Alloys“) je systematické schéma, ve kterém je každý kov označen písmenem následovaným pěti čísly. Jedná se o systém založený na složení komerčních materiálů a nezaručuje žádné výkonnostní specifikace ani přesné složení s limity nečistot. Do systému číslování UNS byly začleněny další systémy názvosloví, aby se minimalizovaly nejasnosti. Například hliník 6061 (AA6061) se stává UNS A96061. Níže je uveden přehled systému UNS se zvláštním důrazem na běžné komerční slitiny. Jako u každého systému i zde existují nejasnosti, například rozdíl mezi superslitinou na bázi niklu a nerezovou ocelí s vysokým obsahem niklu.
-Axxxxx – slitiny hliníku
-Cxxxxx – slitiny mědi, včetně mosazi a bronzu
-Fxxxxx – železo, včetně tvárného železa a litiny
-Gxxxxx – Uhlíkové a legované oceli
-Hxxxxx – Oceli – oceli AISI H
-Jxxxxx – Oceli – lité
-Kxxxxx – Oceli, včetně maraging, nerezové oceli, HSLA, superslitin na bázi železa
-L5xxxx – Slitiny olova, včetně slitin Babbit a pájecích slitin
-M1xxxx – Slitiny hořčíku
-Nxxxxx – Slitiny niklu
-Rxxxxx – Žáruvzdorné slitiny ◦R03xxx- Slitiny molybdenu ◦R04xxx- Slitiny niobu (kolumbia) ◦R05xxx- Slitiny tantalu ◦R3xxxx- Slitiny kobaltu ◦R5xxxx- Slitiny titanu ◦R6xxxx- Slitiny zirkonia
-Sxxxxx – Nerezové oceli, včetně nerezové oceli kalené srážením a superslitin na bázi železa
-Txxxxx – Nástrojové oceli
-Zxxxxx – Zinkové slitiny
Nástrojové oceli
Nástrojové oceli jsou zahrnuty v australské normě AS1239 a prakticky se shodují s americkou klasifikací nástrojových ocelí AISI. (Podobně jako u britské normy 4659)
Např: AS 1239 jakost H13 nástrojová ocel pro práci za tepla obsahující 0,35 % uhlíku, 5,0 % chromu, 1,5 % molybdenu a 1 % vanadu by se v německé normě DIN psala jako X40CrMoV51. Rychlořezné oceli, např:
Výběr ocelí
Velká velikost (400kB): steel_types_large.jpg
Velikost pro tisk (1.7MB): steel_types_fullsize.jpg
Obvyklé druhy oceli v Austrálii (Edcon)
Litina
Když se do oceli přidá příliš mnoho uhlíku, nemůže se rozpustit v roztoku a vytvoří zcela jinou strukturu. Z diagramu Fe-C, který jsme viděli dříve, vyplývá, že litina se tvoří v rozmezí 2 % až 7 % uhlíku (hmotnostních).
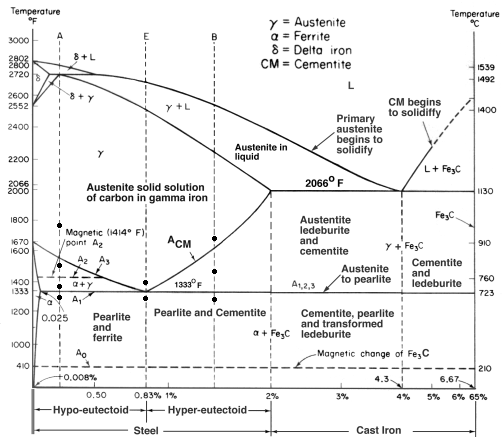
Existuje mnoho druhů litiny, ale nejznámější je šedá litina, která se často používá pro základny obráběcích strojů. Je užitečná a oblíbená z několika důvodů.
Za prvé, teplota tání je nižší, což usnadňuje její odlévání. Je to proto, že eutektikum má teplotu 4,3 % C, což dává teplotu tání pouze 1147oC. Toto eutektikum vytváří nové zrno zvané ledeburit, což je směs austenitu a cementitu. (Vzpomínáte si na perlit? Byl to eutektoid a skládal se z vrstev feritu a cementitu). Ale protože eutektoid je nízký bod přechodu kapalina – pevná látka, je to bod tání.
Druhé, šedá litina je skvělá pro základny strojů. Za normálních okolností by tolik uhlíku znamenalo noční můru v podobě křehkosti kvůli extrémnímu martenzitu a cementitu. Ale ukazuje se, že při správném ochlazení přebytečný uhlík tvoří vločky grafitu. To je něco úplně jiného než všechna ta zrna Fe-C, o kterých jsme mluvili – jako ferit a cementit a perlit a ledeburit. Místo toho je grafit jako inkluze v kovu a dodává šedé litině tlumicí vlastnosti vhodné pro základny strojů. Jedná se však o materiál s nízkou pevností v tahu, takže GCI se obvykle používá tam, kde je v tlaku. GCI je však náchylná ke ztvrdnutí v důsledku nadměrného tepla, takže není snadné ji svařovat. Častěji se bude pájet, ale i to je ve srovnání se spojováním oceli poněkud pochybné.

Mikrofotografie šedé litiny zobrazující grafitové vločky ve feritové matrici. Zdroj
| Název | Nominální složení | Tvar a stav | Mez pevnosti v tahu | Pevnost v tahu | Prodloužení | Tvrdost | Použití | |
|---|---|---|---|---|---|---|---|---|
| Šedá litina (ASTM A48) | C 3.4, Si 1,8, Mn 0.5 | Litina | – | 50 | 0,5 | 260 | Bloky válců motorů, setrvačníky, převody, základny obráběcích strojů | |
| Bílá litina | C 3.4, Si 0,7, Mn 0,6 | Litina (jako odlitek) | – | 25 | 0 | 450 | Nosné plochy | |
| Kovová litina (ASTM A47) | C 2.5, Si 1,0, Mn 0,55 | Lité (žíhané) | 33 | 52 | 12 | 130 | Ložiska náprav, ozubená kola, automobilové klikové hřídele | |
| Kujná nebo tvárná litina | C 3. Železo z tvárné nebo tvárné litiny | .4, P 0,1, Mn 0,4, Ni 1,0, Mg 0.06 | Lité | 53 | 70 | 18 | 170 | Převody, vačkové hřídele, klikové hřídele |
| Tvrdý typ 2 | C 2,7, Si 0,6, Mn 0,5, Ni 4.5, Cr 2,0 | Pískové odlitky | – | 55 | – | 550 | Vysokopevnostní použití |
Slitina
- Slitina: Kovová látka složená ze dvou nebo více prvků.
- Austenit: Austenit: Tvárně centrované kubické železo nebo slitina železa založená na této struktuře.
- Bainit: Produkt konečné přeměny rozkladu austenitu.
- Tělesně centrovaný: Struktura, v níž je každý atom obklopen osmi sousedními atomy, ať už se atom nachází v rohu nebo ve středu jednotkové buňky.
- Cementit: Druhá fáze, která vzniká při překročení meze rozpustnosti uhlíku.
- Kritický bod: Bod, kde se hustoty kapaliny a páry vyrovnávají a rozhraní mezi nimi mizí. Nad tímto bodem může existovat pouze jedna fáze.
- Delta železo: Fáze s tělesně soustředěnou kubickou strukturou, která vzniká, když austenit již není nejstabilnější formou železa. Existuje mezi 2802 a 2552 °C, má strukturu mřížky BCC a je magnetická.
- Eutektikum: Eutektický systém vzniká, když se kapalná fáze přímo tramsformuje na dvoufázovou pevnou látku.
- Eutektoid: K eutektoidní soustavě dochází, když jednofázová pevná látka přechází přímo ve dvoufázovou pevnou látku.
- Face-centrický: Struktura, ve které je atom v rohu každé jednotkové buňky a jeden ve středu každé stěny, ale žádný atom není ve středu krychle.
- Ferit: Frit: tělesově centrované krychlové železo nebo slitina železa založená na této struktuře.
- Drobný perlit: Vzniká z tenkých lamel při zrychleném ochlazování a omezení difuze na kratší vzdálenosti.
- Hypereutektoid: Hypereutektoidní systémy existují pod eutektoidní teplotou.
- Hypoeutektoid: Hypoeutektoidní systémy existují nad teplotou eutektoidu.
- Ledeburit: Eutektikum litiny. Existuje, když je obsah uhlíku větší než 2 %. Obsahuje 4,3 procenta uhlíku v kombinaci se železem.
- Likvidní čára: Na binárním fázovém diagramu je to čára nebo hranice oddělující oblasti kapalné a kapalné + pevné fáze. Pro slitinu je liquidus teplota, při které se za podmínek rovnovážného ochlazování poprvé vytvoří pevná fáze.
- Martenzit: Je to nestabilní polymorfní fáze železa, která se tvoří při teplotách nižších než eutektoid, protože kubická struktura austenitu s centrovaným povrchem se stává nestabilní. Mění se spontánně na tělesově centrovanou strukturu působením střihu, nikoliv difuzí.
- Mikrostruktura: Struktura fází v materiálu. Lze ji vidět pouze pomocí optického nebo elektronového zrcadlového přístroje.
- Perlit: Lamelární směs feritu a karbidu, která vzniká rozkladem austenitu eutektoidního složení.
- Fáze: Stejnorodá část systému, která má jednotné fyzikální a chemické vlastnosti.
- Fázový diagram: Grafické znázornění vztahů mezi omezeními prostředí, složením a oblastmi fázové stability, obvykle za podmínek rovnováhy.
- Polymorfní: Schopnost pevného materiálu existovat ve více než jedné formě nebo krystalové struktuře.
- Zchlazení: Rychlé ochlazení – obvykle když je příliš rychlé na to, aby se vytvořil perlit, a místo toho se vytvoří martenzit
- Solidní linie: Na fázovém diagramu je to místo bodů, v nichž dochází k úplnému ztuhnutí při rovnovážném ochlazení nebo v nichž začíná tání při rovnovážném ohřevu.
- Rozpustnost: Množství látky, které se rozpustí v daném množství jiné látky.
DVD:
Zadání:
Heat Treat

Dotazníky:
Zadání: