Stål är det viktigaste tekniska materialet. Härdningen av stål är mycket viktig.
Föreläsningsvideor
![]() Stål vs stål
Stål vs stål
(Obearbetat material)
![]() Stål: Del 1 ,
Stål: Del 1 , ![]() Stål: Del 2 ,
Stål: Del 2 , ![]() Steel: Del 3
Steel: Del 3
![]() Egenskaper och kornstruktur: BBC 1973 (Gammal men mycket bra)
Egenskaper och kornstruktur: BBC 1973 (Gammal men mycket bra)
Iron är rikligt förekommande i universum och finns i solen och många typer av stjärnor i betydande mängder. Jordens kärna tros bestå av nickel och järn och vara varmare än solens yta. Denna intensiva värme från den inre kärnan gör att material i den yttre kärnan och manteln rör sig runt (konvektionsströmmar).
(Anmärkning: Lustigt att vi inte riktigt vet, eller hur? – Vi vet att det blir varmare när man gräver djupare, men vi kan bara gissa hur varmt det är i jordens centrum. Till och med vid 12 km under jord var forskarnas beräkningar mer än 100 % fel – det var varmare än väntat. När man försöker borra på dessa djup blir berget så varmt att det blir plastiskt och pressas tillbaka till hålet och blockerar borren. Råttor. Så mycket för att gräva till jordens centrum).
Kolstål
Stål är en legering av järn (Fe) och kol (C), med 0,2 till 2,04 viktprocent kol. Kol är det mest kostnadseffektiva legeringsmaterialet för järn, men olika andra legeringselement används, t.ex. mangan, krom, vanadin och volfram.
| Kolstål | ANSI def’n | General Def’n | Användningar och egenskaper |
| Kolstål med lågt kolinnehåll | 0.05-0,15 % | <0,1 % | Mjuk, formbar. Lätt att forma. |
| Milt stål | 0,16-0,29% | 0,1-0,25% | Låg draghållfasthet, men det är billigt och formbart; ytans hårdhet kan ökas genom uppkolning. |
| Mediumkolstål | 0,30-0,59% | 0,25-0,45% | Balanserar duktilitet och hållfasthet och har god slitstyrka; används till stora delar, smide och fordonskomponenter. |
| Högkolstål | 0.6-0,99% | 0,45-1,0% | Mycket starkt, används till fjädrar och höghållfasta trådar. |
| Ultra högkolstål | 1,0-2,0% | 1,0-1,50% (>1,5% sällsynt) |
Mycket hårt – knivar, stansar. Vanligtvis kräver allt över 1,2 % andra legeringar för att förhindra överdriven sprödhet. Mycket hög kolhalt kan uppnås med hjälp av pulvermetallurgi. |
| Gjutjärn | – | 2,5-4,0 % | Lägre smältpunkt, enkel gjutning, lägre seghet och styrka än stål. |
Kolprocent i olika ståltillämpningar;

Varierande mängd legeringselement och hur de införlivas i stålet (lösta element, utfälld fas) påverkar sådana egenskaper som hårdhet, duktilitet och draghållfasthet hos det resulterande stålet. Med ökad kolhalt blir stål hårdare och starkare än järn, men också sprödare. Den maximala lösligheten av kol i järn (i austenitområdet) är 2,14 viktprocent och inträffar vid 1149 °C. Högre koncentrationer av kol eller lägre temperaturer ger cementit (mycket sprött). Om man lägger till mer kol får man gjutjärn, som har en lägre smältpunkt och är lättare att gjuta.
Smältjärn som endast innehåller en mycket liten mängd andra grundämnen, men innehåller 1-3 viktprocent slagg i form av partiklar som är långsträckta i en riktning, vilket ger järnet ett karakteristiskt korn. Det är mer rostbeständigt än stål och svetsar lättare. I dag är det vanligt att tala om ”järn- och stålindustrin” som om den vore en enda enhet, men historiskt sett var de separata produkter.
Stål har tillverkats i tusentals år, men det blev vanligt efter att effektivare produktionsmetoder utarbetades på 1600-talet. Bessemerprocessen i mitten av 1800-talet gjorde stålet relativt billigt för massproducerade varor. Ytterligare förfiningar av processen, t.ex. ståltillverkning med grundläggande syre, sänkte produktionskostnaden ytterligare samtidigt som metallens kvalitet ökade. I dag är stål ett av de vanligaste materialen i världen och är en viktig komponent i byggnader, verktyg, bilar och apparater.

Hämta pdf: XLER_International_Compare.pdf
VIDEO: Egenskaper och kornstruktur. BBC 1973
Skratta inte åt datumet – den här videon slår alla dessa patetiska moderna videor som ger dig ett tjusigt intro men inget annat än en talande huvudperson. De vågar aldrig lämna studion. Denna gamla video är fantastisk för en tydlig introduktion till stålets kornstruktur.
Del 1: Vad är ett korn? (Video 11MB)
- De fläckar som syns på ett galvaniserat föremål är kristaller eller korn av zink.
- Alla metaller består av korn, men de är vanligen osynliga (för små för att ses eller samma glans/färg).
- Etsningsprocessen: I en ren metall har kornen olika färger på grund av hur de reflekterar ljuset.
- Små kristaller växer utåt tills de möts. Varje fullvuxen kristall kallas för ett korn.
Del 2: Rekristallisering (Video 13MB)
- Före kallbearbetning har kornen liknande storlek och form
- Kallbearbetning förlänger kornen, ökar hårdheten och hållfastheten ökar, minskar duktiliteten.
- Vid 350C bildas nya korn i Al som ersätter gamla korn. Kallas rekristallisering
- Rekristallisering mjukar upp, sänker hållfastheten, duktiliteten ökar
- Överdriven rekristalliseringstemp ger dåliga mekaniska egenskaper
Del 3: Värmebehandling av stål (Video 23MB)
- Stålkorn är för små för att synas – det behövs ett mikroskop med ca 250 gångers förstoring.
- Ferrit: Ljusfärgad. Tillverkad av järn. Duktilitet till stål
- Pearlit: Mörkare färgad. Lager av järn + järnkarbid. Hårdhet och hållfasthet i förhållande till stål
- 100 % Pearlit är ca 0,8 % C. Pearlit, omkristalliseringstemperatur 720C.
- Normalisering – kyls i luft, minskad kornstorlek och jämnare form, ökad seghet
- Släckning – ökar hårdheten. Inte tillräckligt med tid för pärlit att bildas, så en nålliknande struktur bildas – martensit. Mycket hård och spröd.
- Härdning – (efter avkylning) återställer segheten. Modifierar martensitnålarna med små flingor av kol. Detta ger hårdhet OCH seghet.
- 0,1 % C-stål (mjukt stål). Omkristallisering 900C. Inte tillräckligt med kol för att producera martensit.
Iron-Carbon Equilibrium Diagram
Utmärkt länk (Cambridge University): http://www.msm.cam.ac.uk/phase-trans/2008/Steel_Microstructure/SM.html
Ett jämviktsdiagram är ett diagram över de olika strukturella arrangemang som förekommer inom ett intervall av ett legeringselement.
Detta diagram visar hur järn och kol kombineras OM det kyls långsamt (i jämvikt). Under 2 % är stål, över 2 % är på väg in i gjutjärnsområdet där kolet tenderar att koagulera (klumpa ihop sig). Cementit Fe3C har 6,67 % C och är i princip en keramik. Eutektoid (pearlite) vid E har 0,83 % C, mindre kol är hypoeutektoid stål (A) och mer är hypereutektoid (B). Alfajärn (ferrit), gammajärn (austenit, som endast existerar vid hög temperatur) och deltajärn (en annan struktur vid hög temperatur).
Två mycket viktiga fasförändringar äger rum vid 0,83 % C och vid 4,3 % C. Vid 0,83 % C och 723ºC är omvandlingen eutektoid, kallad pearlite. Dessa 2 faser separerar sig i lager. Från gamma (austenit) –> alfa + Fe3C (cementit)
Vid 4,3 % C och 1130ºC är omvandlingen eutektisk, kallad ledeburit. L(flytande) –> gamma (austenit) + Fe3C (cementit). Detta är gjutjärn.
BTW. Eftersom kol (12) är mycket lättare än Fe (56) är den faktiska atomära % kol (genom att räkna atomer) i själva verket cirka 4,6 gånger högre än % C i vikt. Så det är inte riktigt så fantastiskt nu, eller hur? Jag menar som att 0,5 % kol kan omvandla mjukt järn helt och hållet… det handlar egentligen om 2 % om man räknar atomer – inte massa.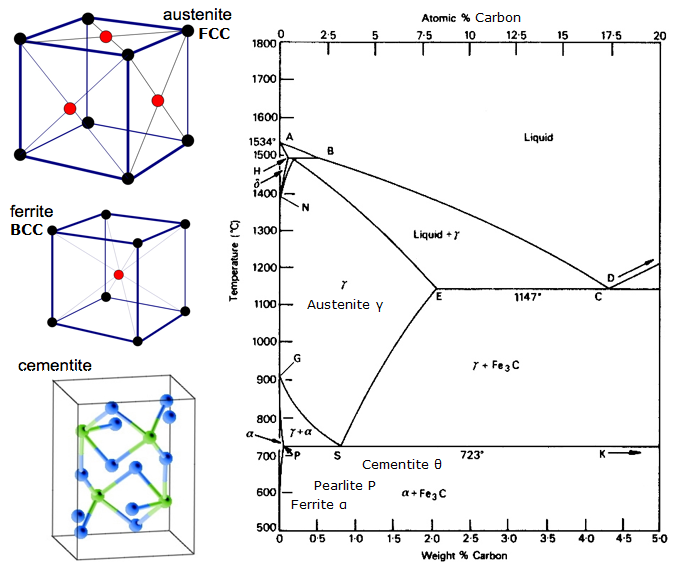
Sammanfattning av Fe-C-strukturer (korn)
- Austenit (γ-järn). Förekommer endast över 723C, vilket är när FCC γ-järnstrukturen uppstår. Kan lösa upp till 2,1 massprocent C. Icke-magnetiskt, mjukt (därav har vi varmbearbetning). Austenit kan också existera vid rumstemperatur om man byter ut några järnatomer mot något annat, t.ex. nickel. Detta är vad austenitiskt rostfritt stål är – till exempel 316. Liksom Austenit vid höga temperaturer är dessa rostfria stål icke-magnetiska. Vissa andra typer av rostfritt stål är magnetiska.
- Cementit (järnkarbid Fe3C, 6,67 viktprocent C). Det finns tolv järnatomer och fyra kolatomer per enhetscell, alltså 33 % kolatomer). Mycket hårt och sprött eftersom det är en keramik. Har du någonsin hört talas om volframkarbid? Tja, detta är järnkarbid.
- Ledeburit (det eutektiska ferrit-cementit-ekot, 4,3 % kol.)
- Ferrit (α-järn, δ-järn; mjukt). Inget kol, BCC. Mjuk och formbar.
- Pearlit (88 % ferrit, 12 % cementit, vilket är 0,83 % C) Starkare än ferrit
- Martensit. Uppstår när kylningen är för snabb för att bilda perlit, så att det låser in spikar av cementit i kornet. Detta inträffar vid släckhärdning av stål med tillräckligt mycket kol i stålet. Mycket hårt.
Mikrografer (bilder från ett mikroskop).
(A) = 0,1 %C ferrit/perlit, (B) = 0,25 %C mer perlit, (C) = 0,83 %C helt och hållet perlit, (D) = 1,4 %C perlit/cementit
Närbild av perlit som visar skikt av ferrit (vitt) och cementit (mörkt).
Mer om perlit: https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Stort FC jämviktsdiagram

Stor utskriftsversion 2000x2658px
Slip
När en bit metall deformeras är det kornen som deformeras. Ett korn är en kristall, ett ordnat arrangemang av atomer i ett rutnät. Om atomerna sträcks isär är detta en elastisk deformation eftersom atomerna hålls ihop av elektronernas attraktionskraft – vilket fungerar som en fjäder. Men permanent (eller plastisk) deformation innebär att atomerna faktiskt glider förbi varandra i lager eller plan.
Ekta kristaller glider inte i ett helt plan på en gång. Det skulle kräva en mycket stor kraft. Istället tillåter ofullkomligheterna i kristallen att glidningen sker en atom i taget. Ju bredare intervallet av påverkade atomer är, desto mer duktilt (lätt glidande) är kornet. Här är ett exempel på en imperfektion som kallas för en dislokation och som lätt kan förflytta sig genom kristallen.
Här är ett faktiskt exempel på glidning. (Vi hittar inte bara på det här!)
En svepelektronmikroskopisk bild av en enkelkristall av kadmium som deformeras genom dislokationsglidning på 100 plan och bildar steg
på ytan.
Den följande animationen visar ett gitter av atomer (t.ex. i en metall). Det finns bara två sätt att förvränga atomerna – axiellt (spänning och kompression) och skjuvning (i sidled).
Denna animation visar endast den elastiska delen av spännings-/förlängningskurvan, där det inte förekommer någon atomisk glidning.
Innehållet på den här sidan kräver en nyare version av Adobe Flash Player.

För ytterligare information här: http://www3.nd.edu/~manufact/MPEM_pdf_files/Ch03.pdf
Vad är BCC och FCC egentligen?
Kristallstrukturerna BCC (Body Centred Cubic) och FCC (Face Centred Cubic) är två alternativa sätt att packa järnatomer.
- BCC är det arrangemang vid rumstemperatur som kallas ferrit
- FCC är det arrangemang vid hög temperatur (>723oC) som kallas austenit.
Download Inventor-filer: SC, BCC, FCC, alla tre (SC+BCC+FCC)
![]()
SC är enkel kubisk och förekommer inte med järnatomer. Detta är saltets – NaCl:
Det minsta arrangemanget (enheten) visas nedan. Lägg märke till hur det kubiska nätet (färgat blått) expanderar när de andra atomerna passar in mellan dem i BCC- och FCC-gitter.
![]()
Det råder ofta viss förvirring kring dessa diagram nedan.

Problemet är att de röda atomerna ser ut som kol och de svarta atomerna ser ut som järn. Nej, nej, nej!
Alla atomer är järn! Vi färglägger bara de järnatomer som inte finns i hörnen för att göra dem lätta att se.
Det andra problemet med dessa diagram är att det inte finns någon riktig indikation på att avståndet mellan hörnatomerna ÖKAR när man går från SC till BCC till FCC.
SC-struktur (Simple Cubic). INTE JÄRNMed en SC (Simple Cubic) struktur (vilket järn inte gör) är avståndet mellan atomerna D. (Där D är atomernas diameter) Så volymen av denna enhet är D3, och atomens volym är 4/3Πr3. Därmed är densiteten 52 % av fast atom. Inte särskilt kompakt. |
 |
BCC-struktur (Body Centred Cubic). FERRITMed en BCC-struktur (Body Centred Cubic) (vilket järn gör under 723oC) är avståndet mellan järnatomerna 1,1547D. (Där D är atomernas diameter) Så volymen av denna enhet är (1,1547D)3, och detta passar 2 atomer så atomernas volym är 2×4/3Πr3. Densiteten är alltså 68 % av en fast atom. Mer kompakt. Denna struktur kallas ferrit. Kol passar inte alls in i denna struktur (Nåväl, jag ljuger. Det kan lösa upp patetiska 0,025 % C, vilket är praktiskt taget noll, eller 0,035 % vid övergångstemperaturen, vilket fortfarande är ingenting) |
 |
FCC-struktur (Face Centred Cubic). AUSTENITMed en FCC-struktur (Face Centred Cubic) (vilket järn gör över 723oC) är avståndet mellan järnatomerna 1,4214D. (Där D är atomernas diameter) Så volymen av denna enhet är (1,4214D)3, och detta passar 4 atomer så atomernas volym är 4×4/3Πr3. Densiteten är alltså 74 % av en fast atom. Detta är den mest kompakta, vilket gör den 6 % tätare än ferrit! Denna struktur kallas Austenit, och den kan lösa upp 2 % kol i sin struktur. Det är 2 % i vikt, glöm inte, och eftersom järn (56) väger 4,7 gånger mer än kol (12) kan det lösa upp cirka 21 % kolatomer (cirka 1 kol för varje 5 järnatomer). |
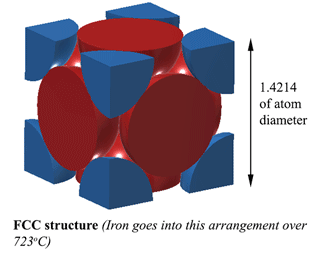 |
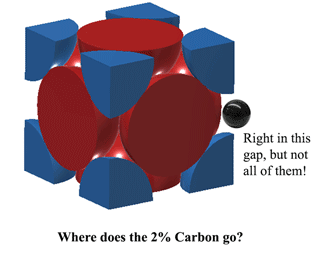
Så, var passar kolet in i austenit?Kol kan passa precis i det där utrymmet i mitten av varje enhetskant. Detta orsakar dock en viss snedvridning, så man kan inte få plats med en kolatom på VARJE kant. I bästa fall kan Austenit vid 1130oC få plats med drygt 2 kolatomer var tredje enhet. (2C:12Fe eller 1:6 med atomer). Det är därifrån 2 viktprocent kommer. Mer här (ganska tungt) https://hal.archives-ouvertes.fr/jpa-00246587/document |
 |
Fler information om BCC och FCC här:
https://www.nde-ed.org/EducationResources/CommunityCollege/Materials/Structure/metallic_structures.htm
http://lessons.chemistnate.com/simple-cubic-fcc-and-bcc.html
https://chem.libretexts.org/Courses/University_of_Arkansas_Little_Rock/Chem_1403%3A_General_Chemistry_2/Text/…
Video om enkla kubiska, kroppscentrerade kubiska och ansiktscentrerade kubiska kristallstrukturer. Järnatomer bildar inte Simple Cubic.
Simple Cubic, Body-Centred Cubic och Face Centred Cubic
Härdning av stål
Härdning handlar om att hindra glidning från att inträffa.
Det finns 3 sätt att göra detta.
- Göra sig av med alla ojämnheter (ganska omöjlig uppgift, även om det är därför som mycket fina fibrer kan ge vansinniga hållfastheter)
- Utnyttja alla glidningar så att inga fler glidningar kan uppstå. Detta kallas arbetshärdning.
- Blocka glidningen från att färdas hela vägen genom kornen. Kol (och kväve) bildar föreningar som fungerar som ett härdningsmedel och hindrar dislokationer i järnkristallgitteret (ferrit) från att glida förbi varandra. Martensit gör detta på ett utmärkt sätt. Detta är värmebehandlingshärdning.
Sköldning av stål visas inte på Fe-C-jämviktsdiagrammet, eftersom sköldning inte är i jämvikt! (D.v.s. avkylningen är för snabb för att austenit med kol i ska kunna få in sig själv i den komplicerade Pearlitstrukturen.

Från https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Den snabba avkylningen (avkylningen) ger upphov till en annan kornstruktur som kallas martensit. Detta korn är extremt hårt och starkt och sprött. Järnkarbidspikarna som tränger igenom kornet förhindrar nu glidning, så duktiliteten går förlorad.

Martensite: University of Cambridge
För att minska sprödheten efter släckning används anlöpning för att ge stålet seghet. Detta ändrar dendriterna av karbid för att ge dem lite duktilitet – utan att förlora för mycket styrka och hårdhet.
Temperering måste ske vid en temperatur under rekristallisering. En ugn är bäst för härdning, men det kan göras med flamman genom att bedöma stålets färg. Tempereringsfärger kan användas som en vägledning för temperaturen. Ju varmare anlöpning desto mjukare stål.
Legeringar som rostfritt stål bildar tunnare filmer än kolstål för en given temperatur och ger därför en färg som ligger lägre i serien. Till exempel motsvarar blek halmfärg 300 °C för SS i stället för 230 °C för CS. De färger som är kallare än de röda (under 500°C) är i själva verket missfärgningar av oxider, inte själva strålningsglödet från själva temperaturen. (Vilket skulle vara infrarött och osynligt. Så allting glöder, man kan bara inte se ljuset!)
| Strålningsfärg | Celcius | Farenht | Tempereringstillämpningar/annat |
| Gul-Vit | 1539°C | 2800°F | Högsta smältpunkt (0%C rent järn) |
| Bright Yellow | 1130°C | 2066°F | Lägsta smältpunkt (4%C gjutjärn) |
| Gul | 1093°C | 2000°F | Koppar smälter vid 1084°C, Guld 1063°C |
| Mörkgult | 1038°C | 1900°F | |
| Orangegult | 982°C | 1800°F | |
| Orange | 927°C | 1700°F | Mässing smälter 930°C |
| Orange röd | 871°C | 1600°F | |
| Högrött | 816°C | 1500°F | |
| Rött | 760°C | 1400°F | Stålets omkristalliseringstemperatur. 723°C |
| Medelröd | 704°C | 1300°F | |
| Mattröd | 649°C | 1200°F | Aluminium smälter 600-660°C |
| Ljusrött | 593°C | 1100°F | Härdning för konstruktionsstål. |
| Varje svagt rött, mestadels grått | 538°C | 1000°F | Härdning för konstruktionsstål. |
| Mörkgrått | 427°C | 0800°F | Härdning för konstruktionsstål. Magnetisk förändring 410 |
| Oxidationsfärg | Celcius | Farenht | Tempereringstillämpningar |
| Blå | 302°C | 0575°F | Sågar för trä, fjädrar |
| Mörklila | 282°C | 0540°F | Kallmejslar, stålsatser |
| lila | 271°C | 0520°F | Pressverktyg, yxor |
| brunt/lila | 260°C | 0500°F | stämplar, koppar, snapsar, spiralborrar, brotschar |
| brunt | 249°C | 0480°F | gängor, Skärblad för metaller |
| Dark Straw | 241°C | 0465°F | Fräsmaskiner, borrar |
| ljus halm | 229°C | 0445°F | Plan- och slitsverktyg |
| Faint Straw | 199°C | 0390°F |
Skydda:
Hastighet för släckning: Stål med högre kolhalt kan släckas långsammare, men ett stål med lägre kolhalt måste släckas snabbt för att få någon härdningseffekt.
Hastighet för släckning: (SNABBT) Saltvatten > vatten > olja > luft > isolerat. (LÄNGST)
För ett komplicerat och dyrt arbete är det bättre att ha en legering med långsam avkylning eftersom den är mindre känslig för temperaturvariationer. Detta är anledningen till att de flesta verktygsstål för t.ex. formsprutningsverktyg är oljeskyddade. Vattenavkylning är bra för enkla former som kan kontrolleras lättare, men det kan orsaka sprickbildning på tjockare sektioner eftersom ytan krymper innan insidan gör det.
Induktionshärdning. Induktionshärdning där elektrisk induktion (snabba magnetiska förändringar) värmer upp stålet som snabbt följs av släckning i vattenstråle. Alternativt uppvärmningssätt i stället för flamma eller ugn.

Induktionshärdning. http://www.thermobondflame.com/Services.page?i=4
Hur man härdar ytan:
Värmebehandling = släckning > Martensit (förhindrar glidning).
Värmning av ytterytan > släckning. Lokal flam- eller induktionsavstängning med vatten (kugghjul).
Kol som tränger in i ytterytan > avstängning. Uppkolning (Uppvärmning i kolförpackning eller kolgas eller upphettade lösningar). Nitrering använder kväve istället för kol för att få en liknande effekt, och det är lättare att få det att penetrera ytan.

Flamhärdning av stålrullar: http://www.thermobondflame.com/Services.page?i=2
Legerade stål
Effekter av legeringselement på verktygsstålsegenskaper: (Mycket grovt)
- Kol: Ökar kolhalten ökar hårdheten något och slitstyrkan avsevärt. Dramatisk ökning av hårdhet & hållfasthet vid värmebehandling.
- Mangan: Små mängder mangan minskar sprödheten och förbättrar smidigheten. Större mängder mangan förbättrar härdbarheten och möjliggör oljeskydd (mindre hård sköljning krävs – vilket minskar deformationen vid sköljning).
- Kisel: Förbättrar hållfasthet, seghet och stöttålighet.
- Volfram: Förbättrar ”heta hårdheten” – används i höghastighetsverktygsstål. Mycket tät (tung)
- Vanadin: Förfinar karbidstrukturen och förbättrar smidigheten, förbättrar även hårdhet och slitstyrka.
- Molybden: Förbättrar djuphärdning, seghet och, i större mängder, ”varmhårdhet”. Används i höghastighetsverktygsstål eftersom det är billigare än volfram.
- Krom: Förbättrar härdbarhet, slitstyrka och seghet.
- Nickel: Förbättrar seghet och slitstyrka i mindre grad.
Inkludering av dessa element i varierande kombinationer kan verka synergistiskt och öka effekterna av att använda dem ensamma. (Till exempel kan cetain legeringselement tillåta mer kol, där så mycket kol skulle vara oanvändbart i ett vanligt kolstål). Ett annat exempel är det intressanta sättet på vilket rostfritt stål (krom och nickel tillsatt till järn) är ganska korrosionsbeständigt.
Steels Identification Codes
AISI-SAE Coding system (American Iraon and Steel Institute – Society of Automotive Engineers). En fyrsiffrig kod, de två första siffrorna anger den allmänna ståltypen och de två sista siffrorna är % kol x 100. Till exempel 1010 är ett vanligt kolstål med 0,10 % C, 5120 är ett kromstål med 0,20 % C. Mer detaljer här

Amerikanska stålkoder: Från Higgins: Materials for Engineers aand Technicians 5th Ed. 2010. p21
BSA (British Standards Association) använder en sexsiffrig kod. Siffrorna är uppdelade i tre grupper enligt nedan. Ett stål med koden 070M20 skulle till exempel vara 070 = kol- eller kolmanganstål, M = specifikation av mekaniska egenskaper, 20 = kolhalt 0,20 %.

British Steel-koder: Från Higgins: Materials for Engineers aand Technicians 5th Ed. 2010. p20
Uns-nummer (förkortning för ”Unified Numbering System for Metals and Alloys”) är ett systematiskt system där varje metall betecknas med en bokstav följt av fem siffror. Det är ett sammansättningsbaserat system för kommersiella material och garanterar inga prestandaspecifikationer eller exakt sammansättning med gränsvärden för föroreningar. Andra nomenklatursystem har införlivats i UNS-nummereringssystemet för att minimera förvirring. Aluminium 6061 (AA6061) blir till exempel UNS A96061. Nedan följer en översikt över UNS-systemet, med särskild tonvikt på vanliga kommersiella legeringar. Som med alla system finns det tvetydigheter, t.ex. skillnaden mellan en nickelbaserad superlegering och ett rostfritt stål med hög nickelhalt.
-Axxxxx – Aluminiumlegeringar
-Cxxxxx – Kopparlegeringar, inklusive mässing och brons
-Fxxxxx – Järn, inklusive duktilt järn och gjutjärn
-Gxxxxx – Kol- och legeringsstål
-Hxxxxx – Stål – AISI H-stål
-Jxxxxx – Stål – gjutstål
-Kxxxxx – Stål, inklusive maråläggningsstål, rostfritt stål, HSLA, superlegeringar på järnbas
-L5xxxxx – Blylegeringar, inklusive Babbitlegeringar och lödlegeringar
-M1xxxx – Magnesiumlegeringar
-Nxxxxx – Nickellegeringar
-Rxxxxx – Eldfasta legeringar ◦R03xxx – Molybdenlegeringar ◦R04xxx- – Läderlegeringar Niobiumlegeringar ◦R05xxx- Tantallegeringar ◦R3xxxx- Koboltlegeringar ◦R5xxxx- Titanlegeringar ◦R6xxxx- Zirkoniumlegeringar
-Sxxxxx – Rostfritt stål, inklusive utfällningshärdande rostfritt stål och järnbaserade superlegeringar
-Txxxxx – Verktygsstål
-Zxxxxx – Zinklegeringar
Verktygsstål
Verktygsstål omfattas av den australiensiska standarden AS1239 och är i stort sett densamma som den amerikanska klassificeringen av verktygsstål AISI. (På samma sätt som British Standard 4659)
Till exempel: AS 1239 Grade H13 verktygsstål för varmbearbetning som innehåller 0,35 % kol, 5,0 % krom, 1,5 % molybden och 1 % vanadin skulle skrivas som X40CrMoV51 i DIN (tyska). Höghastighetsstål, till exempel: AS 1239 grade M2 Innehåller 0,85 % kol, 4,0 % krom, 5,0 % molybden, 6,0 % volfram och 2,0 % vanadin, skulle skrivas som S 6-5-2 i DIN.
Steels Selector
Stort format (400 kB): steel_types_large.jpg
Utskrivbart format (1.7MB): steel_types_fullsize.jpg
Gängse stålsorter i Australien (Edcon)
Gjutjärn
När för mycket kol tillsätts till stål kan kolet inte lösas upp i lösningen och skapar en helt annan struktur. Utifrån Fe-C-diagrammet som vi såg tidigare bildas gjutjärn i intervallet 2-7 % kol (i vikt).
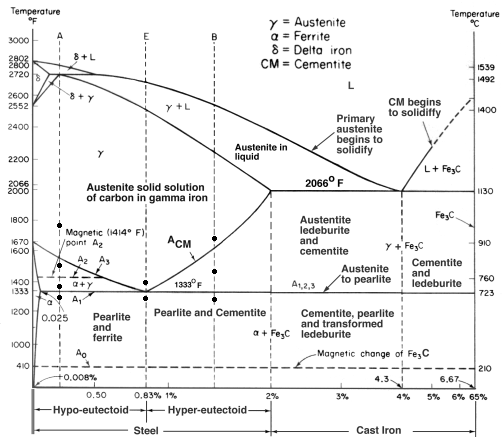
Det finns många typer av gjutjärn, men grått gjutjärn är det mest välkända, som ofta används till baser för verktygsmaskiner. Det är användbart och populärt av flera skäl.
För det första är smälttemperaturen lägre, vilket gör det lättare att gjuta. Detta beror på att eutektiken ligger vid 4,3 % C, vilket ger en smältpunkt på endast 1147oC. Denna eutektik producerar ett nytt korn som kallas ledeburit, som är en blandning av austenit och cementit. (Minns du pärliten? Det var en eutektoid och bestod av lager av ferrit och cementit). Men eftersom en eutektoid är en lågpunkt i övergången mellan vätska och fast ämne är det smältpunkten.
För det andra är grått gjutjärn utmärkt för maskinbaser. Normalt skulle så mycket kol vara en mardröm av sprödhet på grund av extrem martensit och cementit. Men det visar sig att med rätt kylning bildar överflödigt kol flingor av grafit. Detta är något helt annat än alla dessa Fe-C-korn som vi har talat om – som ferrit och cementit och pärlit och ledeburit. Istället är grafit som en inklusion i metallen, och det ger grått gjutjärn de dämpande egenskaper som är lämpliga för maskinbaser. Det är dock ett material med låg draghållfasthet, så GCI används vanligtvis där det är i kompression. GCI är dock benägen att hårdna på grund av överskottsvärme, så det är inte lätt att svetsa. Oftast lödsar man det, men även det är lite tveksamt jämfört med sammanfogning av stål.

Fotomikrografi av grått gjutjärn som visar grafitflingor i en ferritmatris. Källa
| Namn | Nominell sammansättning | Form och tillstånd | Brotthållfasthet | Tåghållfasthet | Förlängning | Hårdhet | Användningsområden |
|---|---|---|---|---|---|---|---|
| Gråt gjutjärn (ASTM A48) | C 3.4, Si 1.8, Mn 0.5 | Gjutning | – | 50 | 0,5 | 260 | Motorcylinderblock, svänghjul, kugghjul, verktygsmaskinunderlag |
| Vitt gjutjärn | C 3.4, Si 0,7, Mn 0,6 | Gjutet (som gjutgods) | – | 25 | 0 | 450 | Lagringsytor |
| Malbart järn (ASTM A47) | C 2.5, Si 1.0, Mn 0.55 | Gjutet (glödgat) | 33 | 52 | 12 | 130 | Axellager, spårhjul, vevaxlar för bilar |
| Duktilt eller nodulärt järn | C 3.4, P 0,1, Mn 0,4, Ni 1,0, Mg 0.06 | Gjutet | 53 | 70 | 18 | 170 | Kugghjul, kamaxlar, vevaxlar |
| Nihårt typ 2 | C 2.7, Si 0.6, Mn 0.5, Ni 4.5, Cr 2,0 | Sandgjutning | – | 55 | – | 550 | Användningar med hög hållfasthet |
Förklaringar
- Legering: Ett metalliskt ämne som består av två eller flera grundämnen.
- Austenit: Ytcentrerat kubiskt järn eller en järnlegering baserad på denna struktur.
- Bainit: Produkten av den sista omvandlingen av austenitnedbrytningen.
- Kroppscentrerad: En struktur där varje atom är omgiven av åtta intilliggande atomer, oavsett om atomen är placerad i ett hörn eller i mitten av en enhetscell.
- Cementit: Den andra fasen som bildas när kolet överskrider löslighetsgränsen.
- Kritisk punkt: Punkt där tätheterna hos vätska och ånga blir lika stora och gränssnittet mellan de två försvinner. Ovanför denna punkt kan endast en fas existera.
- Deltajärn: Den kroppscentrerade kubiska fasen som uppstår när austenit inte längre är den mest stabila formen av järn. Förekommer mellan 2802 och 2552 grader F, har BCC-gitterstruktur och är magnetisk.
- Eutektisk: Ett eutektiskt system uppstår när en flytande fas tramsformas direkt till ett tvåfasigt fast ämne.
- Eutektoid: Ett eutektoidt system uppstår när ett enfasigt fast ämne omvandlas direkt till ett tvåfasigt fast ämne.
- Face-centrerat: En struktur där det finns en atom i hörnet av varje enhetscell och en i mitten av varje yta, men ingen atom i kubens centrum.
- Ferrit: Kroppscentrerat kubiskt järn eller en järnlegering baserad på denna struktur.
- Fin pearlite: Resulterar i tunna lameller när kylningshastigheten påskyndas och diffusionen begränsas till kortare sträckor.
- Hypereutektoid: Hypereutektoida system existerar under den eutektoida temperaturen.
- Hypoeutektoid: Hypoeutektoida system existerar över den eutektoida temperaturen.
- Ledeburit: Eutektikum av gjutjärn. Det existerar när kolinnehållet är större än 2 procent. Den innehåller 4,3 procent kol i kombination med järn.
- Liquiduslinje: På ett binärt fasdiagram, den linje eller gräns som skiljer flytande och flytande + fasta fasområden åt. För en legering är liquidustemperaturen den temperatur vid vilken en fast fas först bildas under förhållanden med jämviktskylning.
- Martensite: En instabil polymorf fas av järn som bildas vid temperaturer under eutektoid eftersom den ytcentrerade kubiska strukturen hos austenit blir instabil. Den övergår spontant till en kroppscentrerad struktur genom skjuvning, inte genom diffusion.
- Mikrostruktur: Struktur av faserna i ett material. Kan endast ses med ett optiskt eller elektronmikroskop.
- Pearlite: En lamellär blandning av ferrit och karbid som bildas genom nedbrytning av austenit av eutektoid sammansättning.
- Fas: En homogen del av ett system som har enhetliga fysiska och kemiska egenskaper.
- Fasdiagram: En grafisk representation av sambanden mellan miljökrav, sammansättning och områden med fasstabilitet, vanligen under jämviktsförhållanden.
- Polymorf: Förmågan hos ett fast material att existera i mer än en form eller kristallstruktur.
- Skräck: Att snabbt svalna – vanligen när det går för fort för att bilda pärlit och i stället skapa martensit
- Soliduslinje: På ett fasdiagram, platsen för de punkter där stelningen är fullständig vid jämviktskylning, eller där smältningen börjar vid jämviktsuppvärmning.
- Löslighet: Den mängd ämne som löser sig i en given mängd av ett annat ämne.
DVD:
Assignment:
Heat Treat

Frågor:
Uppgift: