Oțelul este cel mai important material de inginerie. Călirea oțelului este foarte importantă.
Videoclipuri de curs
![]() Oțel vs. oțel
Oțel vs. oțel
(Secvențe nedifuzate)
![]() Oțel: Partea 1 ,
Oțel: Partea 1 , ![]() Oțelul: Partea 2 ,
Oțelul: Partea 2 , ![]() Oțelul: Partea 3
Oțelul: Partea 3
![]() Proprietăți și structura granulară: BBC 1973 (Vechi, dar foarte bun)
Proprietăți și structura granulară: BBC 1973 (Vechi, dar foarte bun)
Fierul este abundent în univers, se găsește în soare și în multe tipuri de stele în cantități considerabile. Se crede că nucleul Pământului este alcătuit din nichel și fier și că este mai fierbinte decât suprafața Soarelui. Această căldură intensă din miezul interior face ca materialul din miezul exterior și mantaua să se deplaseze (curenți de convecție).
(Notă: Ciudat cum nu știm cu adevărat, nu-i așa? – Știm că se încălzește tot mai mult pe măsură ce sapi mai adânc, dar putem doar să presupunem cât de fierbinte este în centrul Pământului. Chiar și la 12 km sub pământ, calculele oamenilor de știință au fost greșite cu mai mult de 100% – a fost mai cald decât se aștepta. Atunci când se încearcă să se foreze la aceste adâncimi, roca se încălzește atât de tare încât devine plastică și se strânge înapoi în gaură și blochează burghiul. Șobolani. Cam atât despre săparea până în centrul pământului).
Oțelul cu carbon
Oțelul este un aliaj de fier (Fe) și carbon (C), cu 0,2 până la 2,04% carbon în greutate. Carbonul este materialul de aliere cel mai rentabil pentru fier, dar se folosesc diverse alte elemente de aliere, cum ar fi manganul, cromul, vanadiul și tungstenul.
| Oțel carbon | ANSI def’n | Def’n general | Aplicații și proprietăți |
| Oțel cu conținut scăzut de carbon | 0.05-0,15% | <0,1% | Soft, ductil. Ușor de format. |
| Oțel moale | 0,16-0,29% | 0,1-0,25% | Rezistență scăzută la tracțiune, dar este ieftin și maleabil; duritatea suprafeței poate fi mărită prin carburare. |
| Oțel cu conținut mediu de carbon | 0,30-0,59% | 0,25-0,45% | Echilibrează ductilitatea și rezistența și are o bună rezistență la uzură; utilizat pentru piese mari, forjare și componente auto. |
| Oțel cu conținut ridicat de carbon | 0.6-0,99% | 0,45-1,0% | Mult rezistent, folosit pentru arcuri și sârme de înaltă rezistență. |
| Oțel cu carbon foarte ridicat | 1,0-2,0% | 1,0-1,50% (>1,5% rar) |
Mult dur – cuțite, pumni. De obicei, orice peste 1,2% ar necesita alte aliaje pentru a preveni fragilitatea excesivă. Un conținut foarte ridicat de carbon poate fi obținut cu ajutorul metalurgiei pulberilor. |
| Fierul turnat | – | 2,5-4,0% | Punct de topire mai scăzut, turnare ușoară, tenacitate și rezistență mai scăzute decât oțelul. |
Procentajele de carbon în diverse aplicații ale oțelului;


Variația cantității de elemente de aliere și a modului în care acestea sunt încorporate în oțel (elemente solubile, fază precipitată) influențează proprietăți precum duritatea, ductilitatea și rezistența la tracțiune a oțelului rezultat. Odată cu creșterea conținutului de carbon, oțelul devine mai dur și mai rezistent decât fierul, dar și mai fragil. Solubilitatea maximă a carbonului în fier (în regiunea austenită) este de 2,14% în greutate, care apare la 1149 °C; concentrații mai mari de carbon sau temperaturi mai scăzute vor produce cementită (foarte fragilă). Adăugați mai mult carbon și veți obține fontă, care are un punct de topire mai scăzut și este mai ușor de turnat.
Fierul forjat care conține doar o cantitate foarte mică de alte elemente, dar conține 1-3% în greutate de zgură sub formă de particule alungite într-o singură direcție, ceea ce conferă fierului o granulație caracteristică. Este mai rezistent la rugină decât oțelul și se sudează mai ușor. Astăzi se obișnuiește să se vorbească despre „industria fierului și a oțelului” ca și cum ar fi o singură entitate, însă, din punct de vedere istoric, acestea erau produse separate.
Oțelul a fost produs de mii de ani, dar a devenit comun după ce au fost concepute metode de producție mai eficiente în secolul al XVII-lea. Procesul Bessemer de la mijlocul anilor 1800 a făcut ca oțelul să fie relativ ieftin pentru bunurile produse în masă. Perfecționările ulterioare ale procesului, cum ar fi fabricarea oțelului cu oxigen de bază, au redus și mai mult costul de producție, crescând în același timp calitatea metalului. În prezent, oțelul este unul dintre cele mai răspândite materiale din lume și este o componentă majoră în clădiri, unelte, automobile și aparate.

Obțineți pdf: XLER_International_Compare.pdf
VIDEO: Proprietăți și structura granulară. BBC 1973
Nu râdeți de dată – acest videoclip le întrece pe toate cele moderne patetice care vă oferă o introducere fantezistă, dar nimic mai mult decât un cap vorbitor. Nu se aventurează niciodată să iasă din studio. Acest videoclip vechi este fabulos pentru o introducere clară în structura granulară a oțelului.
Partea 1: Ce este un grăunte? (Video 11MB)
- Petele care se văd pe un obiect galvanizat sunt cristale sau grăunțe de zinc.
- Toate metalele sunt alcătuite din grăunțe, dar acestea sunt de obicei invizibile (prea mici pentru a fi văzute sau de aceeași strălucire/culoare).
- Procesul de gravură: Finisaj oglindă, acid puternic, spălat și sigilat.
- Într-un metal pur, granulele au culori diferite din cauza modului în care reflectă lumina.
- Cristalele mici cresc spre exterior până când se întâlnesc. Fiecare cristal crescut complet se numește grăunte.
Partea 2: Recristalizarea (Video 13MB)
- Înainte de prelucrarea la rece, grăunții au dimensiuni și forme similare
- Prelucrarea la rece alungește grăunții, crește duritatea și rezistența crește, reduce ductilitatea.
- La 350C, în Al se formează grăunțe noi care înlocuiesc grăunțele vechi. Se numește recristalizare
- Recristalizarea se înmoaie, scade rezistența, crește ductilitatea
- Temperatura excesivă de recristalizare dă proprietăți mecanice slabe
Partea 3: Tratarea termică a oțelului (Video 23MB)
- Granulele de oțel sunt prea mici pentru a fi vizibile – este nevoie de un microscop cu mărire de aproximativ 250 de ori.
- Ferită: Culoare deschisă. Fabricată din fier. Ductilitate față de oțel
- Perlit: de culoare mai închisă. Straturi de fier + carbură de fier. Duritatea și rezistența la oțel
- 100% Pearlite este de aproximativ 0,8%C. Pearlita, temperatura de recristalizare 720C.
- Normalizare – răcit în aer, reducerea dimensiunii granulelor și o formă mai uniformă, creșterea durității
- Călire – crește duritatea. Nu este suficient timp pentru ca perlita să se formeze, așa că se formează o structură aciculară – martensită. Foarte dură și fragilă.
- Călire – (după călire) restabilește duritatea. Modifică acele de martensită cu mici fulgi de carbon. Aceasta conferă duritate ȘI tenacitate.
- Oțel 0,1%C (oțel moale). Recristalizare 900C. Nu este suficient carbon pentru a produce martensită.
Diagrama de echilibru fier-carbon
Legătură excelentă (Universitatea Cambridge): http://www.msm.cam.ac.uk/phase-trans/2008/Steel_Microstructure/SM.html
O diagramă de echilibru este un grafic al diferitelor aranjamente structurale care apar într-un interval al unui element de aliere.
Această diagramă arată cum se combină fierul și carbonul DACĂ este răcit lent (în echilibru). Sub 2% este oțel, peste 2% se îndreaptă spre domeniul fontei, unde carbonul tinde să se coaguleze (să se aglomereze). Cementita Fe3C are 6,67%C și este practic o ceramică. Eutectoidul (perlita) de la E are 0,83% C, mai puțin carbon este un oțel hipoeutectoid (A), iar mai mult este hipereutectoid (B). Fier alfa (ferită), fier gama (austenită, care există doar la temperaturi ridicate) și fier delta (o altă structură de temperatură ridicată).
Două schimbări de fază foarte importante au loc la 0,83%C și la 4,3% C. La 0,83%C și 723ºC, transformarea este eutectoidă, numită perlit. Aceste 2 faze se separă în straturi. Din gamma (austenită) –> alfa + Fe3C (cementită)
La 4,3% C și 1130ºC, transformarea este eutectică, numită ledeburită. L(lichid) –> gamma (austenită) + Fe3C (cementită). Aceasta este fonta.
BTW. Deoarece carbonul (12) este mult mai ușor decât Fe (56), % atomic real de carbon (prin numărarea atomilor) este de fapt de aproximativ 4,6 ori mai mare decât %C în greutate. Așadar, nu mai este atât de uimitor, nu-i așa? Adică, cum ar fi faptul că 0,5% carbon poate transforma total fierul moale… este de fapt aproximativ 2% dacă se numără atomii – nu masa.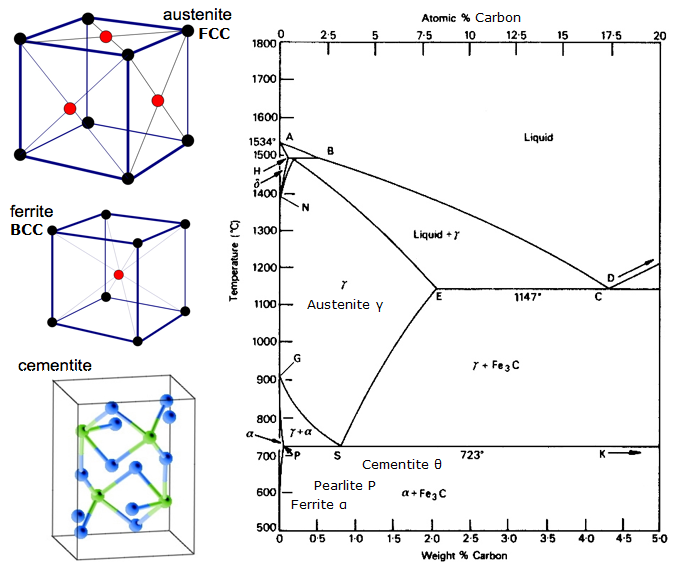
Sumarul structurilor Fe-C (grăunțe)
- Austenit (fier γ). Există numai la temperaturi de peste 723C, moment în care apare structura FCC de fier γ. Se poate dizolva până la 2,1%C în masă. Nemagnetic, moale (de unde și termenul de prelucrare la cald). Austenita poate exista, de asemenea, la temperatura camerei dacă se schimbă unii atomi de fier cu altceva – cum ar fi nichel. Aceasta este ceea ce este oțelul inoxidabil austenitic – cum ar fi 316, de exemplu. Și, ca și austenita la temperaturi ridicate, aceste oțeluri inoxidabile sunt nemagnetice. Unele alte tipuri de oțeluri inoxidabile sunt magnetice.
- Cementită (carbură de fier Fe3C, 6,67%C în masă. Există doisprezece atomi de fier și patru atomi de carbon pe celulă unitară, deci 33% atomi de carbon). Foarte dură și fragilă, deoarece este o ceramică. Ați auzit vreodată de carbură de tungsten? Ei bine, aceasta este carbură de fier.
- Ledeburit (eutecticul Ferită-Cementită, 4,3% carbon.)
- Ferită (α-fier, δ-fier; moale). Fără carbon, BCC. Moale și ductilă.
- Pearlite (88% ferită, 12% cementită, care are 0,83%C) Mai puternică decât ferita
- Martensită. Apare atunci când răcirea este prea rapidă pentru a forma Pearlite, astfel încât blochează vârfuri de Cementite în grăunte. Acest lucru apare la călirea prin călire a oțelului cu suficient carbon în el. Foarte dur.
Micrografii (fotografii la microscop).
(A) = 0,1%C ferită/perlită, (B) = 0,25%C mai multă perlită, (C) = 0,83%C numai perlită, (D) = 1,4%C perlită/ cementită
Vederea de aproape a perlitei care arată straturi de ferită (alb) și cementită (închis).
Mai multe despre perlită: https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Diagrama de echilibru FC mare

Versiunea pentru tipar mare 2000x2658px
Slip
Când o bucată de metal este deformată, granulele sunt cele care se deformează. Un grăunte este un cristal, un aranjament ordonat de atomi într-o rețea. Dacă atomii sunt întinși în afară, aceasta este o deformare elastică, deoarece atomii sunt ținuți împreună prin atracția electronilor – care acționează ca un resort. Cu toate acestea, deformarea permanentă (sau plastică) înseamnă că atomii alunecă efectiv unul pe lângă altul în straturi sau planuri.
Cristalele reale nu alunecă într-un plan întreg deodată. Pentru aceasta ar fi nevoie de o forță foarte mare. În schimb, imperfecțiunile din cristal permit alunecării să se deplaseze câte un atom pe rând. Cu cât este mai largă gama de atomi afectați, cu atât mai ductil (alunecare ușoară) este grăuntele. Iată un exemplu de imperfecțiune numită dislocare care se poate deplasa cu ușurință prin cristal.
Iată un exemplu real de alunecare. (nu inventăm!)
Micrografia electronică cu scanare a unui monocristal de cadmiu care se deformează prin alunecare a dislocațiilor pe 100 de planuri, formând trepte
pe suprafață.
Următoarea animație prezintă o rețea de atomi (ca de exemplu într-un metal). Există doar 2 moduri de deformare a atomilor – axial (întindere și compresie) și forfecare (lateral).
Această animație prezintă doar porțiunea elastică a curbei de tensiune/deformare, unde nu are loc alunecarea atomilor.
Contenutul acestei pagini necesită o versiune mai nouă a Adobe Flash Player.

Aceste informații suplimentare aici: http://www3.nd.edu/~manufact/MPEM_pdf_files/Ch03.pdf
De fapt, ce sunt BCC și FCC?
Structurile cristaline BCC (Body Centred Cubic) și FCC (Face Centred Cubic) sunt două moduri alternative de a împacheta atomii de fier.
- BCC este aranjamentul la temperatura camerei numit ferită
- FCC este aranjamentul la temperaturi ridicate (>723oC) numit austenită.
Descărcați fișierele Inventor: SC, BCC, FCC, Toate trei (SC+BCC+FCC)
![]()
SC este cubică simplă și nu apare cu atomi de fier. Aceasta este rețeaua de sare – NaCl.
Cel mai mic aranjament (unitate) este prezentat mai jos. Observați cum grila cubică (colorată în albastru) se extinde pe măsură ce ceilalți atomi sunt potriviți între ei în rețelele BCC și FCC.
![]()
Există adesea o anumită confuzie cu privire la aceste diagrame de mai jos.

Problema este că atomii roșii arată ca atomii de carbon și atomii negri arată ca atomii de fier. Nu, nu, nu, nu!
Care atom este fier! Noi doar colorăm atomii de fier care nu sunt pe colțuri pentru a-i face mai ușor de văzut.
O altă problemă cu aceste diagrame este că nu există nici o indicație reală că spațierea atomilor din colțuri CREȘTE pe măsură ce se trece de la SC la BCC la FCC.
Structura SC (cubică simplă). NU FIERULCu o structură SC (Cubic Simplu) (pe care fierul nu o face), distanța dintre atomi este D. (unde D este diametrul atomilor) Atunci volumul acestei unități este D3, iar volumul atomului este 4/3Πr3. Atunci densitatea este de 52% din atomul solid. Nu este foarte compact. |
 |
Structura BCC (Body Centred Cubic). FERRITACu o structură BCC (Body Centred Cubic) (pe care fierul o face la 723oC), distanța dintre atomii de fier este de 1,1547D. (unde D este diametrul atomilor) Atunci volumul acestei unități este (1,1547D)3, iar aici încap 2 atomi, deci volumul atomilor este 2×4/3Πr3. Deci densitatea este de 68% din atomul solid. Mai compact. Această structură se numește ferită. Carbonul nu se potrivește deloc în această structură (Bine, spun o minciună. El poate dizolva un patetic 0,025% C, ceea ce este practic zero, sau 0,035% la temperatura de tranziție, ceea ce este tot nimic) |
 |
Structura FCC (Face Centred Cubic). AUSTENITCu o structură FCC (Face Centred Cubic) (pe care fierul o face la 723oC), distanța dintre atomii de fier este de 1,4214D. (unde D este diametrul atomilor) Atunci volumul acestei unități este (1,4214D)3, iar aici încap 4 atomi, deci volumul atomilor este 4×4/3Πr3. Deci densitatea este de 74% din atomul solid. Aceasta este cea mai compactă, ceea ce o face cu 6% mai densă decât ferita! Această structură se numește austenită și poate dizolva 2% carbon în structura sa. Asta înseamnă 2% în greutate, nu uitați, și din moment ce fierul (56) este de 4,7 ori mai greu decât carbonul (12), poate dizolva aproximativ 21% atomi de carbon (Aproximativ 1 atom de carbon la fiecare 5 atomi de fier). |
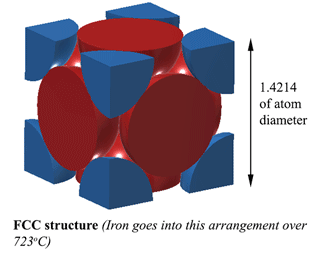 |
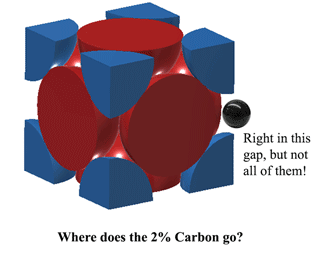
Atunci unde se potrivește carbonul în austenită?Carbonul poate încăpea chiar în acel spațiu din mijlocul fiecărei muchii unitare. Cu toate acestea, acest lucru provoacă o mică distorsiune, astfel încât nu se poate încadra un atom de carbon pe TOATE marginile. În cel mai bun caz, la 1130oC Austenitul poate încăpea puțin peste 2 atomi de carbon la fiecare 3 unități. (2C:12Fe sau 1:6 de atomi). De aici rezultă 2% în greutate. Mai multe aici (destul de greu) https://hal.archives-ouvertes.fr/jpa-00246587/document |
 |
Mai multe informații despre BCC și FCC aici:
https://www.nde-ed.org/EducationResources/CommunityCollege/Materials/Structure/metallic_structures.htm
http://lessons.chemistnate.com/simple-cubic-fcc-and-bcc.html
https://chem.libretexts.org/Courses/University_of_Arkansas_Little_Rock/Chem_1403%3A_General_Chemistry_2/Text/…
Video despre structurile cristaline cubice simple, cubice centrate pe corp și cubice centrate pe față. Atomii de fier nu formează structuri cubice simple.
Simple Cubic, Body-Centred Cubic și Face Centred Cubic
Întăritul oțelului
Întăritul constă în împiedicarea alunecării.
Există 3 moduri de a face acest lucru.
- Scăpați de toate imperfecțiunile (sarcină destul de imposibilă, deși acesta este motivul pentru care fibrele foarte fine pot da rezistențe nebănuite)
- Utilizați toate alunecările astfel încât să nu mai apară alunecări. Acest lucru se numește călire de lucru.
- Blocați alunecarea să nu se deplaseze până la capăt prin granule. Carbonul (și azotul) formează compuși care acționează ca un agent de întărire, împiedicând dislocările din rețeaua cristalină a fierului (ferită) să alunece unele pe lângă altele. Martensita face acest lucru de minune. Aceasta este călirea prin tratament termic.
- Carbon: Creșterea conținutului de carbon crește ușor duritatea și considerabil rezistența la uzură. Creșteri dramatice ale durității & rezistență la tratament termic.
- Mangan: Cantități mici de Manganense reduc fragilitatea și îmbunătățesc forjabilitatea. Cantități mai mari de mangan îmbunătățesc capacitatea de călire, permit călirea în ulei (este necesară o călire mai puțin severă – ceea ce reduce deformarea la călire).
- Siliciu: Îmbunătățește rezistența, tenacitatea și rezistența la șocuri.
- Tungsten: Îmbunătățește „duritatea la cald” – utilizat în oțelul pentru scule de mare viteză. Foarte dens (greu)
- Vanadiu: Rafinează structura carburilor și îmbunătățește forjabilitatea, îmbunătățind, de asemenea, duritatea și rezistența la uzură.
- Molibden: Îmbunătățește călirea profundă, tenacitatea și, în cantități mai mari, „duritatea la cald”. Folosit în oțelul pentru scule de mare viteză deoarece este mai ieftin decât tungstenul.
- Crom: Îmbunătățește capacitatea de călire, rezistența la uzură și duritatea.
- Nichel: Îmbunătățește duritatea și rezistența la uzură într-o măsură mai mică.
Încălzirea oțelului nu este prezentată pe diagrama de echilibru Fe-C, deoarece călirea nu este în echilibru! (adică răcirea este prea rapidă pentru ca austenita cu carbon în ea să se poată introduce în structura complicată Pearlite.

De la https://www.tf.uni-kiel.de/matwis/amat/iss/kap_7/backbone/r7_1_2.html
Răcirea rapidă (călire) produce o structură granulară diferită numită Martensită. Această granulație este extrem de dură și rezistentă, dar și fragilă. Vârfurile de carbură de fier care pătrund prin grăunte împiedică acum alunecarea, astfel încât ductilitatea este pierdută.

Martensită: University of Cambridge
Pentru a reduce fragilitatea după călire, se folosește călirea pentru a adăuga duritate oțelului. Acest lucru modifică dendritele de carbură pentru a le conferi puțină ductilitate – fără a pierde prea multă rezistență și duritate.
Încălzirea trebuie să se facă la o temperatură sub cea de recristalizare. Un cuptor este cel mai bun pentru călire, dar se poate face la flacără, judecând culoarea oțelului. Culorile de călire pot fi folosite ca un ghid pentru temperatură. Cu cât revenirea este mai caldă, cu atât oțelul este mai moale.
Aleliajele, cum ar fi oțelul inoxidabil, formează pelicule mai subțiri decât oțelurile cu carbon pentru o anumită temperatură și, prin urmare, produc o culoare mai jos în serie. De exemplu, paiul palid corespunde la 300°C pentru SS, în loc de 230°C pentru CS. Culorile mai reci decât cele roșii (sub 500°C) sunt, de fapt, decolorarea oxizilor, și nu strălucirea reală a radiației de la temperatura în sine. (Care ar fi în infraroșu, și ar fi invizibilă. Așadar, totul strălucește, doar că nu puteți vedea lumina!)
| Culoarea de radiație | Celcius | Farența | Aplicații de temperare / Altele |
| Galben-Alb | 1539°C | 2800°F | Cel mai înalt punct de topire (fier pur 0%C) |
| Galben strălucitor | 1130°C | 2066°F | Cel mai scăzut punct de topire (4%C fontă) |
| Galben | 1093°C | 2000°F | Cuprul se topește la 1084°C, Aur 1063°C |
| Galben închis | 1038°C | 1900°F | |
| Galben portocaliu | 982°C | 1800°F | |
| Aranja | 927°C | 1700°F | Orazul se topește la 930°C |
| Aranja roșu | 871°C | 1600°F | |
| Roșu aprins | 816°C | 1500°F | |
| Roșu | 760°C | 1400°F | Temperatura de recristalizare a oțelului 723°C |
| Roșu mediu | 704°C | 1300°F | |
| Roșu mat | 649°C | 1200°F | Aluminiul se topește la 600-660°C |
| Roșu deschis | 593°C | 1100°F | Tenuare pentru oțeluri de construcții. |
| Roșu foarte ușor, în cea mai mare parte gri | 538°C | 1000°F | Tăbăcire pentru oțeluri de construcții. |
| Griul închis | 427°C | 0800°F | Tăbăcire pentru oțeluri de construcții. Schimbare magnetică 410 |
| Culoarea de oxidare | Celcius | Farent | Aplicații de temperare |
| Albastru | 302°C | 0575°F | Șezătoare pentru lemn, arcuri |
| Purpuriu închis | 282°C | 0540°F | Dălți reci, seturi pentru oțel |
| Purpuriu | 271°C | 0520°F | Unelte de presare, topoare |
| Brun/Purpuriu | 260°C | 0500°F | Punți, cupe, capse, snap-uri, burghie de răsucire, alezoare |
| Brun | 249°C | 0480°F | Tapse, lamele de forfecare pentru metale |
| Căpșuni întunecate | 241°C | 0465°F | Fraze, burghie |
| Pajură deschisă | 229°C | 0445°F | Unelte de rindeluit și de găurit |
| Pajură slabă | 199°C | 0390°F |
Încălzire:
Viteza de călire: Oțelurile cu conținut mai ridicat de carbon pot fi călite mai lent, dar un oțel cu C mai mic va trebui să fie călit rapid pentru a avea un efect de călire.
Rata de călire: (CEL MAI RAPID) Apă sărată > apă > apă > ulei > aer > izolat. (CEL MAI LENT)
Pentru o lucrare complexă și costisitoare, este mai bine să aveți un aliaj cu călire lentă, deoarece este mai puțin sensibil la variațiile de temperatură. Acesta este motivul pentru care majoritatea oțelurilor pentru scule pentru lucruri precum sculele de turnare prin injecție sunt călite în ulei. Călirea în apă este bună pentru forme simple care pot fi controlate mai ușor, dar poate provoca fisuri pe secțiuni mai groase, deoarece suprafața se micșorează înaintea interiorului.
Încălzirea prin inducție. Călirea prin inducție în care inducția electrică (schimbări magnetice rapide) încălzește oțelul care este urmată rapid de călire în jet de apă. Mod alternativ de încălzire în locul flăcării sau a cuptorului.

Durificare prin inducție. http://www.thermobondflame.com/Services.page?i=4
Cum se întărește suprafața: Călire CASUALĂ.
Tratarea termică = călire > Martensită (oprește alunecarea).
Încălzirea suprafeței exterioare > călire. Călire locală la flacără sau prin inducție cu apă (angrenaje).
Carbon care pătrunde pe suprafața exterioară > călire. Carburare (Încălzire în garnitură de carbon sau gaz carbon sau soluții încălzite). Nitrurarea folosește azotul în loc de carbon pentru a avea un efect asemănător și este mai ușor să îl faci să pătrundă la suprafață.

Întăritul la flacără al rulourilor de oțel: http://www.thermobondflame.com/Services.page?i=2
Oțeluri aliate
Efectele elementelor de aliere asupra proprietăților oțelului pentru scule: (Foarte sumar)
Includerea acestor elemente în diferite combinații poate acționa sinergic, sporind efectele utilizării lor singure. (De exemplu, cetain elemente de aliere pot permite mai mult carbon, în cazul în care atât de mult carbon ar fi imposibil de prelucrat într-un oțel cu carbon simplu). Un alt exemplu este modul interesant în care oțelul inoxidabil (crom și nichel adăugate la fier) este destul de rezistent la coroziune.
Coduri de identificare a oțelurilor
Sistemul de codificare AISI-SAE (American Iraon and Steel Institute – Society of Automotive Engineers). Un cod de 4 cifre, primele 2 cifre dau tipul general de oțel, iar ultimele 2 cifre reprezintă % de carbon x 100. De exemplu, 1010 este un srteel cu carbon simplu cu 0,10% C, 5120 este un oțel cromat cu 0,20% C. Mai multe detalii aici

Coduri americane de oțel: De la Higgins: Materials for Engineers aand Technicians 5th Ed. 2010. p21
BSA (British Standards Association) folosește un cod din 6 cifre. Cifrele sunt separate în 3 grupe, după cum se arată mai jos. De exemplu, un oțel cu codul 070M20 ar fi 070 = oțel carbon sau carbon-mangan, M = specificație a proprietăților mecanice, 20 = conținut de carbon 0,20%.

Codurile British Steel: De la Higgins: Materials for Engineers aand Technicians 5th Ed. 2010. p20
Numele UNS (prescurtare de la „Unified Numbering System for Metals and Alloys”) este o schemă sistematică în care fiecare metal este desemnat printr-o literă urmată de cinci numere. Este un sistem bazat pe compoziția materialelor comerciale și nu garantează nicio specificație de performanță sau o compoziție exactă cu limite de impurități. Alte sisteme de nomenclatură au fost încorporate în sistemul de numerotare UNS pentru a minimiza confuzia. De exemplu, Aluminiul 6061 (AA6061) devine UNS A96061. Mai jos este prezentată o prezentare generală a sistemului UNS, cu accent special pe aliajele comerciale comune. Ca în cazul oricărui sistem, există ambiguități, cum ar fi distincția dintre un superaliaj pe bază de nichel și un oțel inoxidabil cu conținut ridicat de nichel.
-Axxxxx – Aliaje de aluminiu
-Cxxxxx – Aliaje de cupru, inclusiv alama și bronzul
-Fxxxxx – Fier, inclusiv fontă ductilă și fontă turnată
-Gxxxxx – Oțeluri carbon și oțeluri aliate
-Hxxxxx – Oțeluri – Oțeluri AISI H
-Jxxxxx – Oțeluri – turnate
-Kxxxxx – Oțeluri, inclusiv oțel maraging, oțel inoxidabil, HSLA, superaliaje pe bază de fier
-L5xxxxx – Aliaje de plumb, inclusiv aliaje Babbit și aliaje de lipit
-M1xxxxx – Aliaje de magneziu
-Nxxxxx – Aliaje de nichel
-Rxxxxx – Aliaje refractare ◦R03xxx- Aliaje de molibden ◦R04xxx- Aliaje de niobiu (columbiu) ◦R05xxx- Aliaje de tantal ◦R3xxxx- Aliaje de cobalt ◦R5xxxx- Aliaje de titan ◦R6xxxx- Aliaje de zirconiu
-Sxxxxx – Oțeluri inoxidabile, inclusiv oțeluri inoxidabile de călire prin precipitare și superaliaje pe bază de fier
-Txxxxx – Oțeluri pentru scule
-Zxxxxx – Aliaje de zinc
Oțeluri pentru scule
Oțelurile pentru scule sunt cuprinse în standardul australian AS1239 și sunt practic identice cu clasificarea americană AISI a oțelurilor pentru scule. (similar cu standardul britanic 4659)
De exemplu: Oțelul pentru scule pentru lucru la cald AS 1239 clasa H13 care conține 0,35% carbon, 5,0% crom, 1,5% molibden și 1% vanadiu ar fi scris ca X40CrMoV51 în DIN (germană). Oțelurile de mare viteză, de exemplu: AS 1239 grad M2 Conținând 0,85% carbon, 4,0% crom, 5,0% molibden, 6,0% tungsten, 2,0% vanadiu ar fi scris ca S 6-5-2 în DIN.
Steels Selector
Large Size (400kB): steel_types_large.jpg
Printable Size (1.7MB): steel_types_fullsize.jpg
Calificări comune ale oțelului în Australia (Edcon)
Fierul turnat
Când se adaugă prea mult carbon în oțel, carbonul nu se poate dizolva în soluție și creează o structură total diferită. Din diagrama Fe-C pe care am văzut-o mai devreme, fonta se formează în intervalul de 2% până la 7% carbon (în greutate).
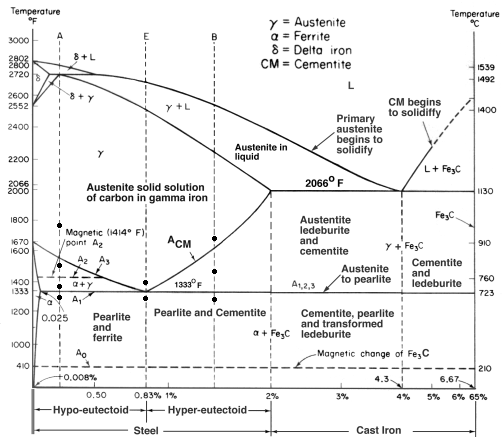
Există multe tipuri de fontă, dar fonta cenușie este cea mai cunoscută, fiind adesea folosită pentru bazele mașinilor-unelte. Este utilă și populară din mai multe motive.
În primul rând, temperatura de topire este mai scăzută, ceea ce o face mai ușor de turnat. Acest lucru se datorează faptului că eutecticul este la 4,3% C, ceea ce dă un punct de topire de numai 1147oC. Acest eutectic produce un nou grăunte numit ledeburit, care este un amestec de austenită și cementită. (Vă mai amintiți perlita? Era un eutectoid și era formată din straturi de ferită și cementită). Dar din moment ce un eutectoid este un punct scăzut în tranziția lichid-solid, acesta este punctul de topire.
În al doilea rând, fonta cenușie este excelentă pentru bazele mașinilor. În mod normal, atât de mult carbon ar fi un coșmar de fragilitate din cauza martensitei și cementitei extreme. Dar se pare că, la o răcire corectă, excesul de carbon formează fulgi de grafit. Acest lucru este complet diferit de toate aceste granule de Fe-C despre care am vorbit – cum ar fi ferita și cementita și perlita și ledeburita. În schimb, grafitul este ca o incluziune în metal și conferă fontei cenușii proprietățile de amortizare potrivite pentru bazele mașinilor. Cu toate acestea, este un material cu o rezistență scăzută la tracțiune, astfel încât GCI este de obicei utilizat acolo unde este în compresie. Cu toate acestea, GCI este predispus la întărire din cauza excesului de căldură, așa că nu este ușor de sudat. Cel mai adesea ar fi brazat, dar chiar și asta este puțin dubios în comparație cu îmbinarea oțelului.

Foto-micrografie de fontă cenușie care arată fulgi de grafit într-o matrice de ferită. Sursa
| Nume | Compoziție nominală | Formă și stare | Rezistența la curgere | Rezistența la tracțiune | Alungire | Duritate | Utilizări |
|---|---|---|---|---|---|---|---|
| Fierul turnat gri (ASTM A48) | C 3.4, Si 1,8, Mn 0.5 | Fundare | – | 50 | 0,5 | 260 | Blocuri de cilindri de motoare, volane, angrenaje, baze de mașini-unelte |
| Fundare albă | C 3.4, Si 0,7, Mn 0,6 | Fundate (ca și turnate) | – | 25 | 0 | 450 | Suprafețe de rulmenți |
| Fierrăgea maleabilă (ASTM A47) | C 2.5, Si 1,0, Mn 0,55 | Fundate (recoapte) | 33 | 52 | 12 | 130 | Rulmenți de osii, roți de șenile, arbori de manivelă pentru autovehicule |
| Fier durduliu sau nodular | C 3.4, P 0,1, Mn 0,4, Ni 1,0, Mg 0.06 | Fier turnat | 53 | 70 | 18 | 170 | Unități de transmisie, arbori cu came, arbori cotiți |
| Ni-dur tip 2 | C 2,7, Si 0,6, Mn 0,5, Ni 4.5, Cr 2,0 | Tăiat în nisip | – | 55 | – | 550 | Aplicații de înaltă rezistență |
Glosar
- Aleag: Substanță metalică care este compusă din două sau mai multe elemente.
- Austenit: Fier cubic cu fețe centrate sau un aliaj de fier bazat pe această structură.
- Bainit: Produsul transformării finale a descompunerii austenitei.
- Body-centrat: O structură în care fiecare atom este înconjurat de opt atomi adiacenți, indiferent dacă atomul este situat într-un colț sau în centrul celulei unitare.
- Cementită: A doua fază care se formează atunci când carbonul este în exces față de limita de solubilitate.
- Punctul critic: Punctul în care densitățile lichidului și a vaporilor devin egale, iar interfața dintre cele două dispare. Deasupra acestui punct, nu poate exista decât o singură fază.
- Delta de fier: Faza cubică centrată pe corp care rezultă atunci când austenita nu mai este cea mai stabilă formă de fier. Există între 2802 și 2552 grade F, are structura rețelei BCC și este magnetică.
- Eutectic: Un sistem eutectic apare atunci când o fază lichidă se traformă direct într-un solid bifazic.
- Eutectoid: Un sistem eutectoid apare atunci când un solid monofazat se transformă direct într-un solid bifazic.
- Face-centrat: O structură în care există un atom în colțul fiecărei celule unitare și unul în centrul fiecărei fețe, dar niciun atom în centrul cubului.
- Ferită: Fier cubic centrat pe corp sau un aliaj de fier bazat pe această structură.
- Perlită fină: Rezultă din lameluri subțiri atunci când ratele de răcire sunt accelerate și difuzia este limitată la distanțe mai scurte.
- Hipereutectoid: Sistemele hipereutectoide există sub temperatura de eutectoid.
- Hipoeutectoid: Sistemele hipoeutectoide există deasupra temperaturii eutectoide.
- Ledeburit: Eutectic al fontei. Există atunci când conținutul de carbon este mai mare de 2 %. Conține 4,3 la sută carbon în combinație cu fierul.
- Linia Lichidus: Pe o diagramă de fază binară, acea linie sau graniță care separă regiunile de fază lichidă și lichidă + solidă. Pentru un aliaj, temperatura de lichidus este acea temperatură la care se formează pentru prima dată o fază solidă în condiții de răcire de echilibru.
- Martensit: O fază polimorfă instabilă a fierului care se formează la temperaturi sub eutectoid deoarece structura cubică cu fețe centrate a austenitei devine instabilă. Se transformă spontan într-o structură centrată pe corp prin acțiune de forfecare, nu prin difuzie.
- Microstructură: Structură a fazelor dintr-un material. Poate fi observată numai cu ajutorul unui mircoscop optic sau electronic.
- Pearlit: Un amestec lamelar de ferită și carbură format prin descompunerea austenitei de compoziție eutectoidă.
- Fază: O porțiune omogenă a unui sistem care are caracteristici fizice și chimice uniforme.
- Diagramă de fază: O reprezentare grafică a relațiilor dintre constrângerile de mediu, compoziția și regiunile de stabilitate a fazelor, în mod obișnuit în condiții de echilibru.
- Polimorfic: Capacitatea unui material solid de a exista în mai multe forme sau structuri cristaline.
- Încălzire: Răcirea rapidă – de obicei atunci când este prea rapidă pentru a forma perlită, creând în schimb martensită
- Linia Solidus: Pe o diagramă de fază, locul punctelor la care solidificarea este completă la răcirea de echilibru sau la care începe topirea la încălzirea de echilibru.
- Solubilitate: Cantitatea de substanță care se dizolvă într-o anumită cantitate de altă substanță.
DVD-uri:
Assignment:
Tratament termic

Întrebări:
Act: